15. února 2010 (Roč. 30, č. 4)
Scott B. Mohler
Jednoduché kroky pro úspěšné bioluminiscenční zobrazování zvířat
Luciferin je základním substrátem bioluminiscenčních testů. Bioluminiscence je založena na jednoduché reakci, kdy ATP pohání luciferázovou katalýzu luciferinu světlušek (brouků) za vzniku světla a má široké využití. Její využití jako indikátoru biomasy umožňuje detekovat mikroorganismy ve spotřebních výrobcích, na povrchu výrobních zařízení a dokonce byla použita ke zjištění, zda existuje život na Měsíci a Marsu.
Bioluminiscence se používá při sledování biologických procesů in vitro a in vivo, včetně genové exprese a interakcí mezi proteiny a proteiny. Luciferin se používá například v testech reportérových genů pro studium regulace a funkce genů, kde je exprese reportéru označeného luciferinem markerem indikujícím úspěšné přijetí zájmového genu v technikách rekombinantní DNA. Jako detekční činidlo se luciferin-luciferázová reakce využívá při pyrosekvenování k dosažení rychlé detekce bází v dnešních vysoce výkonných systémech sekvenování DNA.
V poslední době se bioluminiscenční zobrazování objevilo jako výkonná technika pro přímé studium různých buněčných populací u živých malých zvířat, jako jsou myši. Při této technice jsou buňky (např. nádorové buňky, kmenové buňky, T-buňky) navrženy tak, aby exprimovaly luciferázu a svítily. Neinvazivní vizualizace u živých zvířat pomocí citlivé kamery s nábojovou dvojicí tak umožňuje v reálném čase sledovat progresi a regresi onemocnění v různých obdobích v průběhu terapeutické léčby. Tato technika, využívaná k pochopení molekulární podstaty patologických stavů, jako jsou neurodegenerativní poruchy, kardiovaskulární poruchy, obezita a rakovina, má nesmírnou hodnotu pro klinický, diagnostický a farmaceutický vývoj.
Vědci ze společnosti Regis Technologies identifikovali běžné nedostatky luciferázových testů. Problémy se často objevují ještě před zahájením testu. Světluška luciferin je citlivá molekula a i dobře naplánované experimenty mohou poskytnout chybné výsledky, pokud se s luciferinem před použitím špatně zachází a poškodí se. V tomto článku popisujeme optimální sůl, čistotu, manipulaci a skladování luciferinu, abychom zajistili úspěšné a konzistentní výsledky při zobrazování zvířat a dalších testech.
Úvahy o nákupu
Výzkumníci se často ptají, jakou formu luciferinu použít. Draselné a sodné soli luciferinu se obvykle používají zaměnitelně. Rozpustnost molekuly je však pro některé testy důležitým faktorem, který je třeba zvážit. Sodná sůl je ve vodě rozpustnější (>100 mg/ml) než draselná sůl (55 mg/ml). Volná forma kyseliny, i když je stále k dispozici, se často nepoužívá kvůli obtížnému rozpouštění.
Protože několik nečistot může různým způsobem ovlivnit experimenty, může být důležitým faktorem počáteční čistota činidla.
L-luciferin, enantiomer D-luciferinu (obrázek 1), je známou nečistotou v syntetickém luciferinu. Ačkoli je prokázáno, že funguje v luciferázových reakcích, je pravděpodobné, že v závislosti na použitých parametrech sběru dat dojde k významnému posunu vrcholu světelné emise. L-luciferin lze snadno detekovat a kvantifikovat pomocí chirální HPLC a měl by být uveden v certifikátu analýzy výrobce. Většina luciferinu by měla obsahovat méně než 0,5 % L-luciferinu, ačkoli lze pravděpodobně tolerovat i vyšší limity, pokud hladina L-luciferinu zůstane v průběhu experimentu konstantní.
Dehydroluciferin (obrázek 1) je nečistota, která působí jako inhibitor luciferázy a potlačuje výšku záblesku a celkovou integraci. Vzorek dopovaný 1 % dehydroluciferinu vykazuje méně než poloviční výšku záblesku a méně než 25 % celkové integrace po dobu 15 minut. Dehydroluciferin může vznikat při syntéze nebo skladování luciferinu. Výběr výrobce, který dodává nízké množství dehydroluciferinu, pomůže zajistit spolehlivé a opakovatelné výsledky.
Mnoho běžných stopových nečistot ze syntézy luciferinu může inhibovat jiné enzymy ve složitých systémech a může způsobit experimentální variabilitu v důsledku rozdílů mezi jednotlivými šaržemi nebo výrobci.
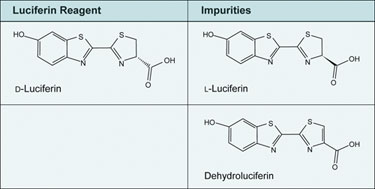
Obrázek 1. Strukturní srovnání D-luciferinu a nečistot
Skladování
Luciferin je citlivý na světlo, kyslík a vlhkost a musí být chráněn. Světlo a kyslík mohou katalyzovat oxidaci luciferinu na dehydroluciferin. Ponechán v jantarové láhvi pod dusíkem při pokojové teplotě se luciferin začne rozkládat na dehydroluciferin po měsíci (obrázek 2), ale v neotevřené láhvi je stabilní nejméně dva roky v mrazáku. Rozpuštěný ve vodě s dostatečným množstvím kyslíku se luciferin přemění na dehydroluciferin za pouhých několik dní.
Luciferin by měl být zakoupen a skladován v co nejmenším množství, aby se zabránilo jeho rozkladu na dehydroluciferin v důsledku opakovaných cyklů zmrazení a rozmrazení. Pokud je zakoupeno ve velkém, pomůže stabilitu zajistit rozdělení luciferinového činidla do jantarových lahviček na jedno použití. Dlouhodobé skladování ve formě zmraženého roztoku se nedoporučuje pro citlivé aplikace, jako jsou studie na celých zvířatech. Abyste zpomalili rozklad ve zmrazených roztocích, před zmrazením roztok prolijte dusíkem nebo argonem.

Obrázek 2. Rozklad luciferinu na dehydroluciferin v závislosti na čase při 25ºC a -20ºC
Manipulace
Kdykoli se lahvička s luciferinem otevře, musí se nechat zcela zchladnout na pokojovou teplotu a poté se před opětovným uzavřením propláchne dusíkem nebo argonem. Pokud mají být roztoky luciferinu použity během několika hodin, je zapotřebí jen málo bezpečnostních opatření. Roztoky, které budou použity v průběhu jednoho dne, by měly být propláchnuty dusíkem nebo argonem. Roztoky by se neměly používat déle než několik dní, protože by docházelo k tvorbě dehydroluciferinu.
Scott B. Mohler ([email protected]) je produktový manažer ve společnosti Regis Technologies. Webové stránky: www.registech.com.