はじめに
胆道上皮に発生する新生物、胆管癌(CC)は肝胆道腫瘍の10%、悪性腫瘍の2%を占める1、2。 この腫瘍は、胆管内の解剖学的起源によって、肝内CCまたは末梢CC(ICC)、肝周囲CCまたはクラツキン腫瘍(PHC)、遠位CCの3つのサブタイプに分けることができます。 唯一利用可能な治癒の選択肢である手術は、診断の時点で約47%の患者さんにおいてのみ可能です。5-8 この腫瘍の最も重要な予後因子は、通常手術の選択肢と関連しており、腫瘍のステージ、サイズ、神経節および血管の関与、肝内転移、組織型が最も重要な因子です9。-11
Anatomical Space
PHC が占める解剖学的空間は、遠位では嚢胞管への入り口、近位では右肝管と左肝管の分岐部で区切られる。1,12 最も広く使われている分類では、胆道合流部またはその周辺に発生するすべての CC が含まれる。 一部のグループは、肝実質内に発生したCCが時に胆道合流部に浸潤することがあり、右門脈後枝のソースと鎌状靭帯で区切られた解剖学的空間内に発生すると指摘している。13-15 これらの胆道合流部を含むICCは肝外由来の腫瘍と同様に扱われ、生存率は同じステージのPHCと同様であると考えられる。 これらは通常、局所的な血管およびリンパ節への浸潤を伴う高度に発達した腫瘍である。 これらの腫瘍の生物学的挙動に関する疑問から、多くのグループがこれらを肝周囲腫瘍から除外している。 江端らによって発表された研究13,15では、合流部に病変を有するCCを切除した250人の患者について、腫瘍が合流部に病変を有する肝内腫瘍(ICC)であるか、腫瘍起源が肝外胆管にあるかによって病期と生存率が分析された。 合計83人の患者がICCを、167人の患者がPHCを呈した。 ステージを比較すると、ICC患者は血管とリンパ節への転移の頻度が高く、TNMはPHC群より高く、59%の症例でステージIIIとIVを呈し、PHC群では38%であった。 しかし、両群の生存期間を病期によって分けると、5年では統計的に有意な差はなく、全生存率はPHC群がわずかに高い(それぞれ20%対29%、P=.057)ため、治療と生存の点では両者は同等であると判断された。 診断検査や病理組織学的な知識の向上により、将来的には、両者が異なる2つの存在なのか、それとも臨床的、生物学的に同じものなのか、より明確に定義できるようになるかもしれません。 10%は腺扁平上皮癌または扁平上皮癌であり、石灰化、嚢胞または胆管の異常の既往を伴う症例もある。 腫瘍の外観、成長のタイプ、PHCの生物学的および臨床的挙動により、以下のように分類される16,17:
- –
腫瘍または「塊状」CC:これは、多数のPHCにも見られるが、ICCで最も一般的な表示形式である。 はっきりとした断端のある腫瘍塊の形成が特徴である。 大きな線維化反応を示し、中心部の壊死も頻繁に見られる。 この腫瘍は胆管開口部から発生し、壁に侵入し、三次元的に成長することで播種し、閉塞症状をもたらす結節性塊を形成する16-19
- –
管周囲浸潤性腫瘍:このタイプの腫瘍は胆管周囲の結合組織を通じて同心の縦方向の肥厚という形で胆管に沿って成長し、患部の胆管の狭窄または完全閉塞を引き起こす19。 17
- –
乳管内型または管内乳頭型CC:この品種は、胆管内の表層および管内腫瘍の存在により特徴付けられる。 この腫瘍は悪性度が低く、通常は小さいが、胆汁粘液を介して広がり、複数の腫瘍(乳頭腫症または乳頭癌腫症)を生じることがある20
この分化の重要性は、問題のサブタイプによって生存率が異なることにある。 いくつかの研究により、乳管内型は強膜結節型よりも予後が良いことが示されており21、平均生存期間はそれぞれ55ヶ月と33ヶ月であった22、血管や神経節への浸潤は乳管内型では少ないことが示されている。
要するに、PHCの大半は、予後不良の管周囲進展型腺癌であり、管内進展型は予後良好であるが、頻度は最も低いということである。 前者は手術計画時に使用され、最も重要なのはBismuth-Corlette分類である。 これは、どの葉が優先的に侵されているかを示すもので、したがって、どのような肝切除を行うべきかを示している(Fig. 1)。23 この分類は1970年代に考案されたもので、リンパ節転移を考慮しないため、現在では予後予測としての価値は低くなっています。
Bismuth-Corlette23分類.
米国で用いられているもう一つの術前分類は、ニューヨークのメモリアルスローンケタリングがんセンターのJarnaginら10が発表したものである。 この分類は、3つの局所進展因子を考慮して腫瘍の切除可能性を予測することを目的としている。 これらは、胆汁性進展、血管病変、葉の萎縮である。 この分類ではリンパ節転移は考慮されていないため、予後予測としての価値は低い。 切除可能性は各グループで異なり、一方では積極的な治療が行われる傾向にあるため、その価値は各施設の切除不能の基準に依存すると思われる。 術後分類のうち、最も広く用いられているのは国際癌連合(UICC)第7版のTNM分類である
12。 この分類は、局所進展、血管病変、リンパ節転移などの病理学的データを考慮し、腫瘍の進展度や予後を考慮した分類を確立しています。
最近、「日本毛髪周囲胆管癌研究会」(JSGPH)は、「国際癌制御連合」の分類を修正した研究を発表し提案しています。 基本的な相違点は表1のとおりで,主に13:
-
Bismuth IVをT4と見なさないというものであった。 したがって、JSGPHの分類では、R0切除が達成された場合、予後不良として両側胆道進展を考慮しない。
-
ステージに関しては、予後不良としてリンパ節転移を優先している。 そのため、リンパ節転移はiiib(TNM7)ではなくiva期とみなしています。
UICC TNM 7分類とJSGPHによる提案の基本的な相違点の比較。
| 腫瘍分類 | UICC | JSGPH 提案 |
|---|---|---|
| Tisについて | 非浸潤癌 | |
| T1 | 胆管に限局した腫瘍 | |
| T2a | 管壁を越えて肝周囲脂肪組織に侵入 | |
| T2b | 肝実質内に侵入 | |
| T3 | 肝動脈/静脈の片側侵襲 | |
| T4 | HA/PV主枝の侵襲。 ビスマスIV またはA/Vの対側侵襲を伴うBismuth III | HA/PVの主ブランドの血管侵襲。 両側血管または対側侵襲を伴うもの |
| TNM stage | ||
| 0 | Tis N0 M0 | |
| I | ||
| II | T2 N0 M0 | |
| IIIa | T3 N0 M0 | |
| IIIb | T1-…3 N1 M0 | T4 N0 M0 |
| イバ | T4 N×M0 | T× N1 M0 |
| Ivb | T×N×M1 | |
HA.B.B.B.B.B.B.B.B.B.B.B.B.B.B, 肝動脈。 JSGPH、肝門部胆管癌に関する日本研究グループ、TNM、腫瘍リンパ節転移、UICC、国際癌対策連合、PV、門脈。
欧州レベルでは、「国際胆管癌グループ」主導で、外科的治療を受けた門脈周囲腫瘍の国際レジストリが作成されてきた。 このグループは、腫瘍の大きさに加え、胆道、静脈、動脈、ガングリオン、転移を考慮した新しい分類を術前、術後に発表している1。 しかし、この分類は、単に腫瘍の特徴や手術の方法を説明するだけで、患者をこれらの変数に従ってグループやステージに分類することができないという制約がある。
過去の論文によると、現在最も広く使われている術前分類はBismuth-Corletteで、長期予後の定義にはTNM7分類が使われています。
診断戦略
PHCに多く見られる症状は、黄疸(90%)、体重減少および腹痛(35%)、そう痒症(26%)および急性胆管炎(10%)である17。 この種の腫瘍に対する他の診断検査は以下の通り:
- –
腹部ドップラー超音波検査:これは動脈および門脈透過性(血栓)を評価することができ、腫瘍の切除率および治療方針を決定することができるが、血管病変の評価には選ばれた検査ではない.
- –
腹部コンピューター断層撮影:原発巣と病巣拡大の診断に有用で、胆道拡大の評価では80%の感度を有する。 血管解剖の術前評価に適した手法であり,動脈病変と門脈病変の評価ではそれぞれ93%と87%の感度がある。 リンパ節転移の術前評価では感度が低い(50%)。14,24 体積検査を行い、外科的切除後に残る肝容積を算出するのにも有用である。 また、術前病期分類のための最も経済的な検査である。
- –
磁気共鳴・磁気共鳴胆管造影(RM-cholangiography):原発腫瘍の診断と胆道進展度の評価に最も適した検査である。 感度は86%-100%で,直接胆管造影より優れており,非侵襲的な検査であることも特徴である25。 一方、血管侵襲の評価では感度が低く(73%)、肝実質への浸潤の評価では感度が80%である。
- –
直接胆管造影:内視鏡的逆行性胆管造影(ERCP)と肝門脈管造影(TPHC):これらは胆道閉塞のレベルを知らせ、細胞診のために病巣からサンプルを採取できるようにするが、感度は20%であった。 現在ではMR-胆管造影に取って代わられている。 術前の胆道ドレナージやPHCの緩和治療に非常に有用であり、優先的に金属コーティングされたステントを挿入することができる26。-28
- –
内視鏡超音波検査:腹腔動脈および膵周囲領域の神経節転移の評価、術前ステージの確立、細針吸引生検の可能性に有用である。
- –
Positron Emission Tomography:腹腔幹の腺病変だけでなく、転移性病変が疑われる患者の研究に有用である。 14,24,29
- –
腫瘍マーカー:これらの有用性は限られており、CA19.9が最もよく使用されている。 多くの研究では,膵臓新生物とCCを対象に,部位や特徴を特定することなく評価されている。 これらのマーカーの血清中濃度は、胆汁排泄のため胆道閉塞や黄疸に強く影響される。 正常値は、肝障害(300U/ml)や黄疸(1000U/ml)の有無によって異なる値が提案されているが、膵臓癌では70%以上の感度が得られ、95%以上の特異度が得られている。 これらの患者における濃度は大きく変化し、腫瘍の大きさとは相関しないが、転移性病変とは相関する。 30
上記のデータから推測すると、PHCの診断には通常、超音波スキャンを使用して研究を開始する。 これは黄疸のある患者に対して行われる。一方、コンピュータ断層撮影とMR-胆管造影は最良の病期診断検査であり、手術前に最も推奨される検査である。 MRやコンピュータ断層撮影は、各病院で利用できる装置やコンピュータプログラムの種類によって、体積検査に使用することができる。 手術の禁忌となるリンパ節への転移が疑われる場合は、陽電子放射断層撮影または細針吸引内視鏡検査が推奨される。
非再建性基準
手術はPHCに対する唯一の治癒的治療であり、最高の長期生存率を提供する。 外科的切除に採用される基準は、1998年にメモリアル・スローン・ケタリングがんセンターのBurkeら31のチームが最初に述べたものから、最近では血管切除や拡大肝切除を用いたアプローチが導入されるまで、近年拡大している3,5,32。-34 切除不能の基準は病院によって異なり、最も普及しているのは、片側に血管病変があり対側の胆道病変が第2レベル根治術の分割まで、遠隔肝転移、両肝葉の血管病変、肝外または腹膜病変、腹腔幹、上腸間膜動脈またはパラ大動脈領域の腺病変である。3,5,8,31
穿刺部での腫瘍播種はCTPH使用例の5~10%で報告されているが、これらの研究では外・内・外ドレナージの使用は特定せず、手術までの経過も考慮されていない。 穿刺点での播種を防ぐために、内視鏡的に配置された経鼻胆道ドレナージの使用を推奨する著者もおり、CPREの場合よりも胆管炎やステント閉塞の発生率が低くなる41。 しかし、同じ研究で、このシステムを用いた術前両側胆汁ドレナージの難しさが認められ、これが片側ドレナージが失敗した患者の手術前のビリルビン値の正常化の妨げになっている42
術前胆汁ドレナージ後の感染症に伴う罹患率を減らすために、ドレナージ後と手術中に胆汁を系統的に培養することが示唆されている。 いくつかの研究によると、ドレナージした患者のこれらの培養の78%~94%が陽性であるのに対し、ドレナージしていない患者では20%~30%であり、43~45%が腸球菌が最もよく分離される菌であることが分かっている。 これらのグループは予防的抗生物質の使用を推奨しているが、分離された菌種の抗生物質耐性を高めるものの、発表された研究では、術後感染症の罹患率はドレーンなしと同程度であることが示されている。 選択される抗生物質は培養と抗体像によるが、培養ができない場合や陰性の場合は、少なくとも第3世代セファロスポリンまたはフルオロキノロン+メトロニダゾールを使用するグループが大半であった43, 44, 46
切除ができない患者には、緩和胆汁ドレナージが用いられる。 8157>
このように、ビリルビンが10mg/dL以上の患者、および肝切除量が50%以上の患者には、術前に胆道ドレナージを行うことが決定的に重要である。 どのような方法で行うかは病院によって異なるが、腫瘍の操作を避けるため、また胆管炎の発生率が低いことから、外部ドレナージによるCTPHが推奨される。
術前門脈塞栓術
術前門脈塞栓術は1980年代に幕内ら47、木下ら48によって報告された。門脈塞栓術の目的は、術前の容積測定で残肝量が不十分と思われた症例に対して残肝量を増やし、術後の肝不全の確率を下げることである。 最近発表されたHiguchi and Yamamoto49によるメタアナリシスでは、術前に門脈塞栓術を行ったPHC患者836人を対象とし、罹患率は1%、死亡率は0.09%であった。 手術の妨げとなった術中の腫瘍の進行は19.4%であった。 8157>ステージング腹腔鏡検査<9316>近年、非侵襲的画像検査の感度と特異度が向上したことにより、ステージング腹腔鏡検査は使われなくなりつつある。 切除不能の最も重要な基準は、リンパ節転移、胆道進展、脈管侵襲である。 これらは腹腔鏡検査では評価が難しく、その精度や有効性はここ数年低下している。 RotellarとPardoによる最近の改訂版50では、2002年の研究では精度が41%、有効性が72%であったが、2011年に発表された研究では14%、32%となっている。 この低下は主にMR-cholangiographyのような非侵襲的な検査が進歩したためである。 腹膜播種や肝転移のリスクが高い患者を選択すれば、その有効性は高まり、不必要な開腹手術を防ぐことができる。50-52 進行した腹膜やリンパ節転移の可能性があり、術前の胆道ドレナージ作成前にエコー内視鏡で穿刺できない進行期(T2/3/4)では非侵襲的画像技術が勧められる。 我々は常に術中超音波検査で病期分類を行い、局所病変やリンパ節転移の感度を高めている53
手術療法
手術はPHCの唯一の根治療法であり、3、14 5年後の生存率は20~40%である(表2)10、11 R0切除が可能であれば常に外科的切除を行う必要がある。 手術後の生存率に影響を与える主な要因は、顕微鏡的に(R1)またはマクロ的に(R2)の切除断端への浸潤と、リンパ節転移(N1およびN2)である14、17、44、54。 尾状節切除による拡大肝切除、胆道切除、腹腔幹までの肝門部リンパ節切除、肝切除術による再建などが提案されている
Survival Following Resection of the PHC According to the Series Published.(発表されたシリーズによると、PHCの切除後の生存率。
| 著者 | 年 | 症例 | Survival at 5 years (%) |
|---|---|---|---|
| デオリヴェイラら(1991)、 DeOliveira et al. | 2007 | 35 | 10 |
| Lladó et al. | 2008 | 62 | 43 |
| Figueras et al. | 2009 | 19 | 63a |
| 宇野ら | 2010 | 125 | 35 |
| ヤングら。 | 2010 | 51 | 29 |
| イガミら | 298 | 42 | |
| Van Gulikら. | 2011 | 38 | 33 |
| De Jong et al. | 2012 | 305 | 20.2 |
| Neuhausら | 100 | 43 | |
| Regimbeauら. | 2014 | 331 | 53 |
肝周囲胆管癌による肝切除後の生存率について。
2年間の追跡調査のみ
Neuhausらによって最初に報告された「ノータッチテクニック」32。 3,33,34,55 この方法は基本的に、門脈と右肝動脈が腫瘍に近い場合は切除し、腫瘍の操作を伴う場合はその解離を防ぐとともに、腹腔動脈根までの広いリンパ節切除と肝静脈造影による再建を伴う胆道完全切除から構成される。 腫瘍の進展により腫瘍に最も近い右肝動脈を含めることが可能であれば、右肝葉を選択することが望ましい(Neuhausによれば、必須の「ノンタッチテクニック」)33。 このような根治的手術は、術後合併症の割合が50%~70%と許容範囲であり、死亡率は10%~20%である(対象症例による)。3,5 PHC患者の5年生存率は20%~40%であるが、門脈切除を含む研究および「ノータッチ法」を用いたシリーズでは5年生存率は58%である(図2および図3) 3,5,33
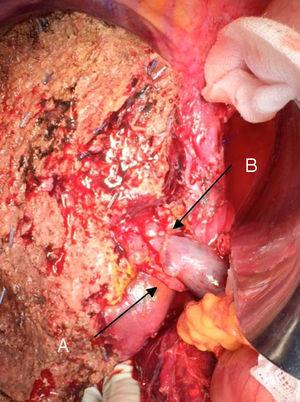
クラツキン腫瘍に対する左肝切除術、門脈の切除を伴う。 (A)上腸間膜の右肝動脈、(B)門脈.
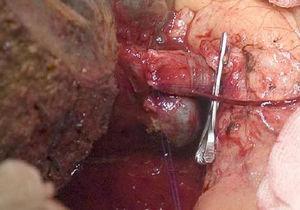
門脈再建を伴う右肝切除術.
また、術前に血管病変があった患者さんの門脈切除後の生存率が上昇している最近の研究についても強調しておきたい点である。 33,56,57 これらの研究では、肝および血管合併症の発生率は、動脈切除を受けた患者が他の患者より病的死亡率が高いことを除いて、門脈切除を受けなかったグループのものと同様である。 これらのことから、術前検査で片側門脈浸潤または合流部浸潤を認めた患者には、一括切除と血管再建を行う手術が推奨される。 動脈が明らかに侵されていない限り、動脈切除と再建は推奨されない。これは術後成績が悪くなるためで、そのような場合は右肝切除が望ましい。
要約すると、従うべき手術の原則は、門脈や肝動脈の切除と再建を伴う場合でも、腫瘍を操作せず、R0マージンで胆道切除と尾状リンパ節切除を行う根治手術とすることである。 根治的な一括切除と血管再建は、長期生存率が最も高い術式である。 術後の罹患率を下げるために、肝不全予防のために胆道ドレナージを行い、ドレナージ後に抗生剤の予防投与を行い、将来の残存肝容量が30%以下になる場合には門脈塞栓術を行うことが推奨されます。 R0切除、リンパ節転移、遠隔転移は依然として最も重要な予後因子である。
利益相反
この改訂は、いかなる雑誌または学会においても、一部または全部が発表または掲載されていない
。