Communiqué de presse
Lundi 28 décembre 2020
L’essai financé par le NIH et la BARDA recrutera jusqu’à 30 000 volontaires.
Les personnes âgées de 18 ans et plus qui souhaitent participer à cet essai peuvent visiter coronaviruspreventionnetwork.org, ClinicalTrials.gov et rechercher l’identifiant NCT04611802, ou Novavax.com/PREVENT-19 pour plus de détails. Veuillez ne pas contacter le numéro de téléphone ou l’email des médias du NIAID pour vous inscrire à cet essai.
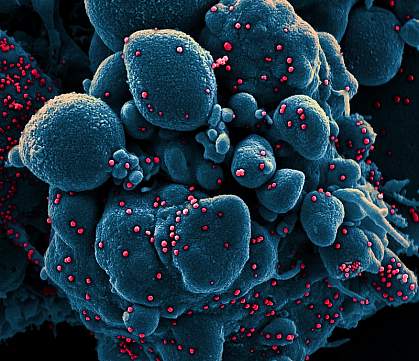 Micrographie électronique à balayage colorisée d’une cellule apoptotique (bleu) infectée par des particules de virus SRAS-COV-2 (rouge), isolée d’un échantillon de patient.NIAID
Micrographie électronique à balayage colorisée d’une cellule apoptotique (bleu) infectée par des particules de virus SRAS-COV-2 (rouge), isolée d’un échantillon de patient.NIAID L’essai de phase 3 d’un autre vaccin expérimental contre le coronavirus 2019 (COVID-19) a commencé à recruter des volontaires adultes. L’essai randomisé, contrôlé par placebo, recrutera environ 30 000 personnes sur environ 115 sites aux États-Unis et au Mexique. Elle évaluera la sécurité et l’efficacité du NVX-CoV2373, un candidat vaccin développé par Novavax, Inc. de Gaithersburg, Maryland. Novavax dirige l’essai en tant que sponsor réglementaire. Le National Institute of Allergy and Infectious Diseases (NIAID), qui fait partie des National Institutes of Health, et la Biomedical Advanced Research and Development Authority (BARDA), qui fait partie du U.S. Department of Health and Human Services Office of the Assistant Secretary for Preparedness and Response, financent l’essai.
« S’attaquer à la crise sanitaire sans précédent du COVID-19 a nécessité des efforts extraordinaires de la part du gouvernement, des universités, de l’industrie et de la communauté », a déclaré le directeur du NIAID Anthony S. Fauci, M.D. « Le lancement de cette étude – le cinquième candidat vaccin expérimental COVID-19 à être testé dans un essai de phase 3 aux États-Unis – démontre notre détermination à mettre fin à la pandémie par le développement de plusieurs vaccins sûrs et efficaces. »
L’essai est mené en collaboration avec Operation Warp Speed (OWS), une collaboration multi-agences supervisée par le HHS et le Département de la Défense qui vise à accélérer le développement, la fabrication et la distribution de contre-mesures médicales pour le COVID-19. Certains des sites d’essai américains participants font partie du réseau de prévention du COVID-19 (CoVPN) soutenu par le NIAID. Le CoVPN comprend des réseaux de recherche clinique existants soutenus par le NIAID et possédant une expertise en matière de maladies infectieuses et a été conçu pour une évaluation rapide et approfondie des candidats vaccins et des anticorps monoclonaux pour la prévention du COVID-19.
Les volontaires devront donner leur consentement éclairé avant de participer à l’essai. Ils seront regroupés en deux cohortes : les individus âgés de 18 à 64 ans et ceux âgés de 65 ans et plus, l’objectif étant de recruter au moins 25% de tous les volontaires âgés de 65 ans ou plus. Les organisateurs de l’essai mettent également l’accent sur le recrutement de personnes qui présentent un risque plus élevé de maladie grave liée au COVID-19, notamment celles qui sont noires (y compris les Afro-Américains), amérindiennes ou d’ethnie latino ou hispanique, et les personnes qui présentent des problèmes de santé sous-jacents tels que l’obésité, une maladie rénale chronique ou le diabète.
« Nous sommes allés aussi loin, aussi vite, mais nous devons atteindre la ligne d’arrivée », a déclaré le directeur du NIH, Francis S. Collins, M.D., Cela nécessitera de multiples vaccins utilisant différentes approches pour s’assurer que tout le monde est protégé de manière sûre et efficace contre cette maladie mortelle ».
Après avoir fourni un échantillon nasopharyngé et sanguin de base, les participants seront assignés au hasard pour recevoir une injection intramusculaire du vaccin expérimental ou d’un placebo salin. La randomisation se fera dans un rapport 2:1, avec deux volontaires recevant le vaccin expérimental pour chaque volontaire recevant le placebo. Comme l’essai est réalisé en aveugle, ni les investigateurs ni les participants ne sauront qui reçoit le vaccin expérimental. Une deuxième injection sera administrée 21 jours après la première.
Les participants seront suivis de près pour détecter les effets secondaires potentiels du vaccin et devront fournir des échantillons de sang à des moments précis après chaque injection et pendant les deux années suivantes. Les scientifiques analyseront les échantillons de sang pour détecter et quantifier les réponses immunitaires au SRAS-CoV-2, le virus à l’origine du COVID-19. Il est à noter que des tests spécialisés seront utilisés pour distinguer l’immunité résultant de l’infection naturelle de l’immunité induite par le vaccin. Le critère principal de l’essai est de déterminer si le NVX-CoV2373 peut prévenir la maladie symptomatique du COVID-19 sept jours ou plus après la deuxième injection par rapport au placebo.
Le vaccin expérimental de Novavax, le NVX-CoV2373, est fabriqué à partir d’une forme stabilisée de la protéine de pointe du coronavirus en utilisant la technologie des nanoparticules de protéines recombinantes de la société. Les antigènes protéiques purifiés du vaccin ne peuvent pas se répliquer et ne peuvent pas causer le COVID-19. Le vaccin contient également un adjuvant breveté, MatrixM™. Les adjuvants sont des additifs qui améliorent les réponses souhaitées du système immunitaire au vaccin. Le NVX-CoV2373 est administré sous forme liquide et peut être conservé, manipulé et distribué à des températures supérieures au point de congélation (35° à 46°F). Une dose unique de vaccin contient 5 microgrammes (mcg) de protéine et 50 mcg d’adjuvant.
Dans les tests sur animaux, la vaccination par le NVX-CoV2373 a produit des anticorps qui ont empêché la protéine de pointe du coronavirus de se lier aux récepteurs de surface cellulaire ciblés par le virus, empêchant ainsi l’infection virale. Dans les résultats d’un essai clinique de phase 1 publiés dans le New England Journal of Medicine, le NVX-CoV2373 a été généralement bien toléré et a provoqué des niveaux d’anticorps plus élevés que ceux observés dans les échantillons de sang prélevés chez des personnes qui s’étaient remises d’une infection par le COVID-19 cliniquement significative. Le NVX-CoV2373 est également en cours d’évaluation dans un essai de phase 2b en Afrique du Sud, qui compte maintenant 4 422 volontaires, et les données d’un essai de continuation de phase 1/2 aux Etats-Unis et en Australie sont attendues dès le premier trimestre 2021. Novavax a également récemment terminé le recrutement de plus de 15 000 volontaires dans un essai de phase 3 du candidat-vaccin au Royaume-Uni, qui teste également deux injections de 5 mcg de protéine et 50 mcg d’adjuvant Matrix-M administrées à 21 jours d’intervalle.
Un comité indépendant de surveillance des données et de la sécurité (DSMB) assurera la surveillance pour garantir la conduite sûre et éthique de l’étude. Tous les essais cliniques de phase 3 des vaccins candidats soutenus par OWS sont supervisés par un DSMB commun développé en consultation avec l’initiative NIH Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV).
Les adultes qui souhaitent participer à cette étude peuvent visiter Coronaviruspreventionnetwork.org, Novavax.com/PREVENT-19 ou ClinicalTrials.gov et rechercher l’identifiant NCT04611802.
A propos du réseau de prévention COVID-19 : Le réseau de prévention COVID-19 (CoVPN) a été formé par l’Institut national des allergies et des maladies infectieuses (NIAID) des Instituts nationaux de la santé des États-Unis pour répondre à la pandémie mondiale. Grâce au CoVPN, le NIAID tire parti de l’expertise en matière de maladies infectieuses de ses réseaux de recherche existants et de ses partenaires mondiaux pour répondre au besoin urgent de vaccins et d’anticorps contre le SRAS-CoV-2. Le CoVPN s’efforcera de développer et de mener des études pour assurer une évaluation rapide et approfondie des vaccins et des anticorps pour la prévention du COVID-19. Le CoVPN a son siège au Fred Hutchinson Cancer Research Center. Pour plus d’informations sur le CoVPN, visitez : coronaviruspreventionnetwork.org.
A propos de HHS, ASPR et BARDA : Le HHS s’efforce d’améliorer et de protéger la santé et le bien-être de tous les Américains, en fournissant des services de santé et des services humains efficaces et en favorisant les progrès en médecine, en santé publique et en services sociaux. La mission de l’ASPR est de sauver des vies et de protéger les Américains contre les menaces de sécurité sanitaire du 21e siècle. Au sein de l’ASPR, la BARDA investit dans l’innovation, la recherche et le développement avancés, l’acquisition et la fabrication de contre-mesures médicales – vaccins, médicaments, produits thérapeutiques, outils de diagnostic et produits non pharmaceutiques nécessaires pour combattre les menaces pour la sécurité sanitaire. À ce jour, les produits soutenus par le BARDA ont obtenu 55 approbations, licences ou autorisations de la FDA. Pour en savoir plus sur le soutien fédéral à la réponse nationale au COVID-19, visitez www.coronavirus.gov.
A propos de l’Operation Warp Speed : OWS est un partenariat entre les composantes du Département de la santé et des services sociaux et du Département de la défense, s’engageant avec des entreprises privées et d’autres agences fédérales, et coordonnant les efforts existants à l’échelle du HHS pour accélérer le développement, la fabrication et la distribution des vaccins, des thérapeutiques et des diagnostics du COVID-19.
A propos de l’Institut national des allergies et des maladies infectieuses : Le NIAID mène et soutient des recherches – au NIH, dans tous les États-Unis et dans le monde entier – pour étudier les causes des maladies infectieuses et à médiation immunitaire, et pour développer de meilleurs moyens de prévenir, de diagnostiquer et de traiter ces maladies. Des communiqués de presse, des fiches d’information et d’autres documents relatifs au NIAID sont disponibles sur le site Web du NIAID.
A propos des National Institutes of Health (NIH):NIH, l’agence de recherche médicale de la nation, comprend 27 instituts et centres et est une composante du département américain de la santé et des services sociaux. Le NIH est la principale agence fédérale qui mène et soutient la recherche médicale fondamentale, clinique et translationnelle. Il recherche les causes, les traitements et les remèdes pour les maladies communes et rares. Pour plus d’informations sur le NIH et ses programmes, visitez le site www.nih.gov.
NIH…Turning Discovery Into Health®
####