Neprilysiini on noussut kardiologian kiinnostuksen kohteeksi, koska neprilysiinin eston ja angiotensiinireseptorin salpauksen yhdistämisestä on saatu vaikuttavia hyötyjä, jotka osoitettiin äskettäisessä PARADIGM-HF-tutkimuksessa, jossa testattiin LCZ696:ta (joka tunnetaan nykyisin nimellä sacubitril/valsartaani ja jota Novartis markkinoi nimellä Entresto) systolisen sydämen vajaatoiminnan hoidossa, kun sydämen ejektiofraktio on pienentynyt (HFrEF).1 Neprilysiini EC 3.4.24.11 (tunnetaan myös nimillä neutraali endopeptidaasi, endoproteaasi 24.11, NEP, yhteinen akuutin lymfoblastileukemian antigeeni , neutrofiiliantigeenin klusterin erilaistumisantigeeni 10 , membraanimetalloendopeptidaasi EC 3.4.24.11 ja enkefalinaasi) on kuitenkin erittäin monipuolinen entsyymi, joka on palannut takaisin huomion keskipisteeseen tapahtumarikkaan uran jälkeen, jonka kesto on ollut > 40 vuotta.2 .
Kardiovaskulaarisessa järjestelmässä neprilysiini pilkkoo lukuisia vasoaktiivisia peptidejä. Joillakin näistä peptideistä on verisuonia laajentavia vaikutuksia (mukaan lukien natriureettiset peptidit, adrenomedulliini ja bradykiniini), ja toisilla on verisuonia supistavia vaikutuksia (muun muassa angiotensiini I ja II sekä endoteliini-1). Sen suurin affiniteetti on eteisnatriureettiseen peptidiin, C-tyypin natriureettiseen peptidiin ja angiotensiini I:een ja II:een, ja pienin affiniteetti on B-tyypin natriureettiseen peptidiin (BNP), endoteliini-1:een ja bradykiniiniin.3
Napriilysiini on ollut vuosikymmenien ajan tärkeä biokohde. Akateemiset ja teolliset toimijat ovat yhdistäneet aktiiviset ponnistelunsa etsiäkseen neprilysiinin estäjiä (NEPI), joista voisi olla hyötyä kliinisessä käytännössä. Aluksi 1980-luvun lopulla ja 1990-luvun alussa testattiin NEPI-monoterapiaa. Candoksatriililla oli lupaavia alustavia vaikutuksia hemodynaamisiin parametreihin. Toinen NEPI, ekadotriili, johti kuitenkin korkeampaan kuolleisuuteen, eikä sen kliinisestä tehosta ollut näyttöä lumelääkkeeseen verrattuna sydämen vajaatoimintapotilailla.4,5 Tämän vuoksi NEPI-monoterapian kehittäminen sydämen vajaatoiminnan hoitoon lopetettiin. Myöhemmin joissakin tutkimuksissa saatiin näyttöä reniini-angiotensiini-aldosteronijärjestelmän samanaikaisesta aktivoitumisesta ja natriureettisen peptidin bioaktiivisuuden lisääntymisestä. Nämä havainnot innoittivat kehittämään ja testaamaan aineita, jotka yhdistivät NEPI:n ja angiotensiinikonvertaasientsyymin estäjän (ACEI) aktiivisuuden, mikä johti vasopeptidaasin estäjinä tunnettujen lääkkeiden kehittämiseen. Useita vasopeptidaasin estäjiä on kehitetty, mukaan lukien omapatriilaatti, fasidotriili, sampatriilaatti ja mixanpril. Lukuisten tutkimusten jälkeen alan ammattilaiset olivat hyvin pettyneitä havaitessaan, että omapatrilaatti aiheutti yhä useammin kliinisesti merkityksellisiä angioödeemaepisodeja.6 Yli vuosikymmenen aavikolla vaeltelun jälkeen kehitettiin uusi konsepti, NEPI:n ja angiotensiini II -reseptorin salpaajien (ARB:t) yhdistelmä, joka johti uuteen lääkeryhmään, jota kutsutaan nimellä angiotensiinireseptori-neprilysiinin estäjät. Sacubitriili/valsartaani on luokkansa ensimmäinen angiotensiinireseptori-neprilysiinin estäjä, joka osoitti odotettua parempia tuloksia PARADIGM-HF-tutkimuksessa1 (kuva).
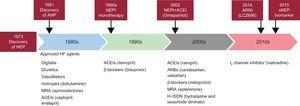
Kaavio historiallisista neprilysiinin kohokohdista. ACEI, angiotensiinikonvertaasientsyymin estäjä; ANP, eteisnatriureettinen peptidi; ARB, angiotensiini II -reseptorin salpaaja; ARNI, angiotensiinireseptori-neprilysiinin estäjä; HF, sydämen vajaatoiminta; MRA, mineralokortikoidireseptoriantagonisti; NEP, neprilysiini; NEPI, neprilysiinin estäjä; sNEP, liukoinen neprilysiini.
PARADIGM-HF oli monikansallinen, satunnaistettu, kaksoissokkotutkimus, johon osallistui 8442 potilasta. Tavoitteena oli verrata sakubitriilia/valsartaania enalapriiliin aikuispotilailla, joilla oli krooninen sydämen vajaatoiminta (New York Heart Associationin luokka II-IV) ja pienentynyt vasemman kammion ejektiofraktio (LVEF ≤ 40 %, myöhemmin muutettu ≤ 35 %:ksi) muun sydämen vajaatoimintalääkityksen lisäksi.1 Ensisijainen päätetapahtuma oli sydän- ja verisuonitautikuoleman tai sydämen vajaatoiminnan aiheuttaman sairaalahoidon yhdistelmä. Ennen tutkimukseen osallistumista potilaita hoidettiin tavanomaisella hoidolla, johon kuuluivat ACEI/ARB-lääkkeet (> 99 %), beetasalpaajat (94 %), mineralokortikoidiantagonistit (58 %) ja diureetit (82 %). Seurannan mediaanikesto oli 27 kuukautta, ja potilaita hoidettiin enintään 4,3 vuotta.
Potilaiden oli lopetettava nykyinen ACEI- tai ARB-hoito ja siirryttävä peräkkäiseen, yksisokkoiseen sisäänajojaksoon. Käyttöönottojakson aikana he saivat hoitoa enalapriililla 10 mg kahdesti vuorokaudessa, minkä jälkeen he saivat yksisokkohoitoa sakubitriilillä/valsartaanilla 100 mg kahdesti vuorokaudessa, joka nostettiin 200 mg:aan kahdesti vuorokaudessa. Tämän jälkeen heidät satunnaistettiin tutkimuksen kaksoissokkojaksoon. Tänä aikana he saivat joko sacubitriilia/valsartaania 200 mg tai enalapriilia 10 mg kahdesti päivässä. Tutkitun väestön keski-ikä oli 64 vuotta, ja 19 % oli 75-vuotiaita tai vanhempia. Satunnaistettaessa 70 % potilaista kuului NYHA-luokkaan II, 24 % luokkaan III ja 0,7 % luokkaan IV. Keskimääräinen LVEF oli 29 %, ja 963 (11,4 %) potilaalla oli lähtötilanteessa LVEF > 35 % ja ≤ 40 %. Tutkimus lopetettiin ennenaikaisesti, koska kardiovaskulaarisista syistä johtuva kuolema ja yhdistetyn ensisijaisen päätetapahtuman (kardiovaskulaarinen kuolema tai sydämen vajaatoiminnan aiheuttama sairaalahoito) vähenivät ylivoimaisesti. PARADIGM-HF-tutkimuksesta käytetään myös nimitystä 20 %:n tutkimus, koska kaikkien tutkittujen päätetapahtumien, mukaan lukien yhdistetty ensisijainen päätetapahtuma eli sydän- ja verisuonitautikuolema, äkillinen sydänkuolema ja sairaalahoitoon joutuminen sydämen vajaatoiminnan vuoksi (taulukko 1), suhteellinen vähenemä oli homogeeninen ∼20 % (taulukko 1).
PARADIGM-HF- tutkimus: Treatment Effects on the Primary Composite Endpoint, Its Components, and All-cause Mortality, Over a Median Follow-up of 27 Months
| Endpoints | Hazard ratio (95%CI) | Relative risk reduction | P |
|---|---|---|---|
| Ensisijainen yhdistetty päätetapahtuma CV-kuolema ja sydämen vajaatoiminnasta johtuvat sairaalahoitojaksot | 0.80 (0.73-0.87) | 20 % | .0000002 |
| Primäärisen yhdistetyn päätetapahtumakohdan yksittäiset osatekijät | |||
| CV-kuolema | 0.80 (0.71-0.89) | 20 % | .00004 |
| Ensimmäinen sydämen vajaatoiminnan sairaalahoito | 0.79 (0.71-0.89) | 21 % | .00004 |
| Toinen päätetapahtuma | |||
| Yleiskuolleisuus | 0.84 (0.76-0.93) | 16% | .0005 |
95%CI, 95 %:n luottamusväli; CV, sydän- ja verisuonisairauksiin liittyvä.
Vaikka sakubitriili/valsartaani on osoittanut olevansa valtavan lupaava, on olemassa haasteita ja käsittelemättömiä seikkoja, jotka ansaitsevat lisätutkimuksia ja tarkempaa selvittelyä (taulukko 2). Jotkin näistä kysymyksistä otettiin esille ja niitä käsiteltiin Euroopan lääkeviraston Entrestoa koskevassa arviointikertomuksessa.7
Yhteenveto Sacubitril/Valsartaanin turvallisuuteen liittyvistä huolenaiheista
| Tärkeät tunnistetut riskit | Hypotensio Munuaisten vajaatoiminta Hyperkalemia Angioedeema |
| Tärkeitä mahdollisia riskejä | Hepatotoksisuus Kognitiivinen heikentyminen Statiinilääkkeisiin-lääkkeiden yhteisvaikutukset Trombosytopenia Neutropenia |
| Puuttuvat tiedot | Pediatriset potilaat, joilla on HF Potilaat, joilla on vaikea munuaisten vajaatoiminta Pitkä-pitkäaikaistiedot sakubitriilin/valsartaanin käytöstä HF:n hoidossa Vaikutukset ACEI/ARB-naivilla HF-potilailla |
ACEI, angiotensiinikonvertaasientsyymin estäjä; ARB, angiotensiini II -reseptorin salpaaja; HF, sydämen vajaatoiminta.
Muokattu Euroopan lääkeviraston arviointikertomuksesta.7
Ensinnäkin, kun potilailla ilmenee siedettävyysongelmia (esim. systolinen verenpaine ≤ 95 mmHg, oireinen hypotensio, hyperkalemia, munuaisten toimintahäiriö), nykyiset suositukset ovat samanaikaisten lääkkeiden mukauttaminen ja/tai sakubitriilin/valsartaanin vähentäminen alaspäin tai tilapäinen lopettaminen. Itse asiassa Euroopan lääkevirasto suosittelee, että hoitoa ei pidä aloittaa potilailla, joiden seerumin kaliumpitoisuus on > 5,4 mmol/l tai joiden systolinen verenpaine on
mmHg.
Toiseksi, tiedot ovat rajalliset niiden potilaiden osalta, jotka käyttävät tällä hetkellä pieniä annoksia ACEI:tä tai ARB:tä tai eivät käytä niitä lainkaan. Siksi nykyiset suositukset näille potilaille ovat, että aloitetaan annoksella 50 mg kahdesti vuorokaudessa ja titrataan annosta hitaasti (kaksinkertaistamalla annos 3-4 viikon välein).
Kolmanneksi, sakubitriilia/valsartaania ei saa antaa samanaikaisesti ACEI:n tai ARB:n kanssa. Käytettäessä samanaikaisesti ACEI:n kanssa on suuri mahdollinen angioedeeman riski. Tämän vuoksi sacubitriilia/valsartaania ei saa aloittaa vähintään 36 tuntiin sen jälkeen, kun ACEI-hoito on lopetettu.
Neljänneksi, annoksen mukauttamista ei tarvita potilailla, joilla on lievä munuaisten vajaatoiminta (arvioitu glomerulusten suodatusnopeus 60-90 ml/min/1,73 m2). Potilailla, joilla on keskivaikea munuaisten vajaatoiminta (arvioitu glomerulussuodatusnopeus 30-60 ml/min/1,73 m2), on kuitenkin harkittava 50 mg:n aloitusannosta kahdesti vuorokaudessa. Tietoja potilaista, joilla on loppuvaiheen munuaistauti, ei ole, mutta sacubitriilin/valsartaanin käyttöä ei suositella näille potilaille.
Viidenneksi, sacubitriilin/valsartaanin aloittamisessa potilaille, joilla on NYHA-toimintoluokitus IV, on noudatettava varovaisuutta, koska kliinistä kokemusta tästä väestöstä on vähän.
Kuudenneksi, BNP ei ole sopiva sydämen vajaatoiminnan biomarkkeri sacubitriilillä/valsartaanilla hoidetuilla potilailla, koska se on neprilysiinisubstraatti. Siirtymistä NT-proBNP:hen natriureettisen peptidin biomarkkerina suositellaan.
Seitsemänneksi, neprilysiinin estoon liittyvä teoreettinen riski liittyy neprilysiinisubstraatin, amyloidi-β:n, kertymiseen aivoihin.8 Kognitioon tai dementiaan liittyvien haittatapahtumien lisääntynyttä esiintyvyyttä ei raportoitu PARADIGM-HF-tutkimuksessa. Näitä vaikutuksia ei kuitenkaan välttämättä ole havaittu tähän mennessä, koska dementian kehittyminen voi kestää kauemmin kuin tutkimukseen osallistuneiden nykyinen seuranta-aika. Myöskään lievää dementiaa sairastavien henkilöiden ei odotettu osallistuvan tutkimukseen. Käynnissä olevassa vaiheen III PARAGON-HF-tutkimuksessa on kuitenkin otettu käyttöön kognitiivisten toimintojen arviointi.
Kahdeksanneksi, sakubitriilin/valsartaanin ja atorvastatiinin samanaikainen käyttö lisäsi atorvastatiinin ja sen metaboliittien Cmax-arvoa jopa 2-kertaiseksi. Mahdolliset statiiniin liittyvät haittavaikutukset eivät lisääntyneet merkittävästi potilailla, jotka saivat sekä sacubitriilia/valsartaania että statiinia PARADIGM-HF-tutkimuksessa. Lisäanalyysit ovat kuitenkin osoittaneet, että suurempiin statiiniannoksiin liittyi enemmän haittatapahtumia, kun ne yhdistettiin joko sacubitriilin/valsartaanin tai enalapriilin kanssa. Kuvio oli kuitenkin erilainen riippuen annetusta statiinista. Lisätutkimusten tuloksia odotettaessa on suositeltu varovaisuutta tämän lääkeyhdistelmän suhteen.7
PARADIGM-HF-tutkimuksessa keskitytään krooniseen sydämen vajaatoimintaan, jossa LVEF on rajallinen. Näin ollen herää kysymys: Entä muut 50 % potilaista, joilla on sydämen vajaatoiminta, mutta joiden ejektiofraktio on säilynyt, eli niin sanotut HFpEF-potilaat? Tällä hetkellä HFpEF-potilaita koskevia kliinisiä tutkimuksia, joissa olisi osoitettu terapeuttisia hyötyjä aineilla, joita käytetään yleisesti potilailla, joiden ejektiofraktio on pienentynyt, ei ole. Tämän vuoksi HFpEF:n hoidot on suunnattu oireiden hallintaan ja sydän- ja verisuonitautien riskitekijöihin. HFpEF-potilaiden keskuudessa sacubitril/valsartaani osoitti kuitenkin lupaavia turvallisuus- ja tehotuloksia vaiheen 2 tutkimuksessa. PARAMOUNT-tutkimus oli satunnaistettu, kaksoissokkoutettu, rinnakkaisryhmiin perustuva aktiivinen kontrolloitu tutkimus, jossa verrattiin sacubitriilia/valsartaania pelkkään valsartaaniin.9 Ensisijainen päätetapahtuma oli NT-proBNP:n muutos lähtötilanteesta 12 viikon kuluttua. Ryhmillä oli samanlaiset lähtötason ominaisuudet. Suurin osa potilaista oli iäkkäitä, naisia, ylipainoisia ja luokiteltu NYHA-luokkaan II. Sakubitriili/valsartaaniryhmässä havaittiin suurempi NT-proBNP:n väheneminen viikolla 4 verrattuna valsartaaniryhmään, mutta se ei saavuttanut merkitsevyyttä (P = 0,063). 12 viikon kohdalla NT-proBNP väheni merkitsevästi sakubitriili/valsartaaniryhmässä verrattuna valsartaaniryhmään (P = 0,005). PARAMOUNT-tutkimuksen tulokset viittasivat siihen, että sacubitriililla/valsartaanilla saattaa olla suotuisia vaikutuksia HFpEF-potilailla. HFpEF-populaatiota tutkitaan edelleen PARAGON-tutkimuksessa, joka on monikeskuksinen, satunnaistettu, kaksoissokkoutettu, rinnakkaisryhmiin perustuva aktiivinen kontrolloitu tutkimus. Kyseisessä tutkimuksessa pyritään arvioimaan sakubitriilin/valsartaanin tehoa ja turvallisuutta valsartaaniin verrattuna sairastuvuuteen ja kuolleisuuteen sydämen vajaatoimintapotilailla, joilla on sydämen vajaatoiminta (NYHA-luokka II-IV) ja joiden ejektiofraktio on säilynyt.
Viimeisimpänä, mutta ei vähäisimpänä, aivan hiljattain verenkierrossa kiertävää liukenevaa neprilysiiniä (sNEP) ehdotettiin potentiaaliseksi biomarkkeriksi.2 Tällä hetkellä sNEP:stä saadut tiedot viittaavat siihen, että sillä voi olla ennusteellinen merkitys sekä kroonisessa10 että akuutisti dekompensoituneessa sydämen vajaatoiminnassa,11 mutta HFpEF:ssä tulokset ovat kiistanalaisia.12 Mielenkiintoista on, että verenkierrossa olevan sNEP:n on osoitettu olevan katalyyttisesti aktiivinen.13 Lisäksi hiljattain julkaistussa raportissa osoitettiin, että sNEP saattaa olla jopa NT-proBNP:tä parempi sydämen vajaatoiminnan neurohormonaalisen akselin ennusteellisena korvikkeellisena biomarkkerina.14 sNEP:n määritystekniikoiden hienosäätöä on pakko parantaa entisestään, ennen kuin sNEP:n voi ottaa käyttöön kliinisessä käytännössä. Tähän mennessä raportoidut tiedot viittaavat kuitenkin siihen, että siitä voi tulla arvokas väline potilaiden ennusteiden laatimisessa ja lopulta hoidon ohjauksessa.
Epilogina todettakoon, että tämän uuden aineen hoitokustannukset ovat todennäköisesti esteenä sen käytölle jokapäiväisessä todellisessa kliinisessä käytännössä, sillä tehokkaiden lääkkeiden, kuten ACEI-enaalipriilin, kustannukset ovat hyvin alhaiset (verrattavissa purukumin hintaan monissa maissa). Voidaan ajatella, että voitaisiin ehdottaa biomarkkeripohjaisen strategian toteuttamista, jotta ACEI-hoidosta siirrytään Entresto-hoitoon ensisijaisesti kaikkein sairaimmilla potilailla. On huomionarvoista, että natriureettisten peptidien käyttö oli yksi PARADIGM-HF-tutkimuksen sisäänottokriteereistä. Sacubitriilin/valsartaanin kustannusvaikuttavuus ja kustannukset saavutettua laatukorjattua elinvuotta kohti suhteessa enalapriiliin HFrEF:n hoidossa ansaitsevat intensiivistä tutkimusta reaalimaailman skenaarioissa, jotka on mukautettu maittain ja terveydenhuoltojärjestelmittäin.15
CONFLICTS OF INTEREST
A. Bayes-Genis ja J. Lupón ovat hakeneet patenttia sNEP:lle prognostisena biomarkkerina, joka odottaa hyväksyntää. A. Bayes-Genis on luennoinut ja osallistunut Novartisin neuvoa-antaviin toimikuntiin.