La química nos ayuda a entender las propiedades y la composición del mundo que nos rodea. Aquí aprenderás sobre los estados de la materia, así como muchas cosas sobre un estado en particular (tres adivinanzas: no es sólido ni líquido…).
Los estados de la materia
En función de la temperatura, la presión y las propiedades de una sustancia, ésta puede adoptar diferentes formas físicas. A estas formas físicas las llamamos Estados de la Materia. Hay tres estados de la materia muy conocidos: Los sólidos, los líquidos y los gases. También existen otros estados de la materia. Entre ellos se encuentran el plasma (un estado de la materia similar a un gas, pero que contiene electrones e iones que se mueven libremente, es decir, átomos que han perdido electrones) y los condensados de Bose-Einstein (BEC) (ondas de materia que pueden producirse con algunos tipos de átomos a temperaturas superfrías).
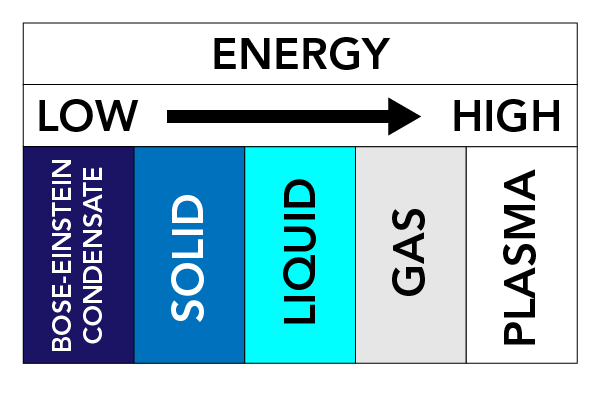
Las fuerzas entre las partículas y la presión sobre las partículas mantienen las partículas juntas. Si calentamos la materia (añadimos energía), las partículas empiezan a moverse más rápido y tienden a separarse. Este movimiento de las partículas tiene un gran efecto en el estado de una sustancia.
Sólidos
En los sólidos, las fuerzas que mantienen unidas las partículas son relativamente fuertes, y las partículas permanecen muy cerca unas de otras. Las partículas pueden vibrar pero no se mueven mucho. Por eso los sólidos son duros y rígidos. Si se dejan solos, los sólidos mantienen su forma.
Líquidos
En los líquidos, las fuerzas entre las partículas son más débiles que en los sólidos. Las partículas siguen estando bastante juntas, pero pueden moverse libremente. Los líquidos pueden fluir dentro de un recipiente y no tienen ninguna forma fija en particular.
Gases
Los gases son difíciles de relacionar porque a menudo son invisibles, pero se encuentran por todas partes. Puedes sentirlos cuando, por ejemplo, sopla el viento. A veces puedes olerlos cuando, por ejemplo, hueles el olor de la comida que se está cocinando, o cuando una mofeta se ha molestado. Algunos gases son importantes para nuestra salud (por ejemplo, el oxígeno) mientras que otros pueden ser mortales (por ejemplo, el sulfuro de hidrógeno y el cloro). Antes de una intervención quirúrgica, puede recibir un gas anestésico, que contiene sustancias químicas, para aliviar el dolor y dejarle inconsciente durante el procedimiento. Los gases también son responsables de la fuerza de las explosiones. Veamos con más detalle los gases.
Tipos de gases
Hay gases elementales (formados por un solo elemento) y gases que son compuestos (formados por más de un elemento). Los símbolos de los gases elementales se pueden encontrar en cualquier Tabla Periódica de los Elementos. Se resumen en el siguiente cuadro.
Gas diatómico |
Fórmula química |
Gas monatómico Gas |
Fórmula química |
|
Hidrógeno |
H2 |
Helio |
He |
|
Oxígeno |
O2 |
Neón |
Ne |
|
Nitrógeno |
N2 |
Argón |
Ar |
|
Fluorina |
F2 |
Criptón |
Kr |
|
Cloro |
Cl2 |
Xenón |
Xe |
Un gas diatómico es aquel en el que la unidad básica es una molécula formada por dos átomos unidos. Un gas monatómico es aquel en el que la unidad básica es un solo átomo. La mayoría de los gases, sin embargo, son compuestos con dos o más elementos diferentes unidos químicamente. El más común es el vapor de agua, H2O. Estos son los nombres, fórmulas y usos de algunos gases compuestos:
Nombre común |
Fórmula química |
Donde se normalmente lo encuentras |
|
Dióxido de carbono |
CO2 |
Atmósfera, los gases de escape de los coches, el pop, nuestros pulmones |
|
Propano |
C3H8 |
Asadores, estufas de campamento, combustible para algunos vehículos |
|
Metano |
CH4 |
Componente del gas de efecto invernadero y del gas natural |
|
Amoníaco |
NH3 |
Utilizado para fabricar fertilizantes, productos de limpieza |