Elementos moleculares
Hay muchas sustancias que existen como dos o más átomos conectados entre sí con tanta fuerza que se comportan como una sola partícula. Estas combinaciones multiatómicas se denominan moléculas. Una molécula es la parte más pequeña de una sustancia que tiene las propiedades físicas y químicas de esa sustancia. En algunos aspectos, una molécula es similar a un átomo. Una molécula, sin embargo, está compuesta por más de un átomo.
| Hidrógeno, H | Oxígeno | Nitrógeno | Fluoro | Cloro | Bromo | Yodo |
Algunos elementos existen naturalmente como moléculas. Por ejemplo, el hidrógeno y el oxígeno existen como moléculas de dos átomos. Otros elementos también existen naturalmente como moléculas diatómicas – una molécula con sólo dos átomos (Tabla \(\PageIndex{1}\)). Como cualquier molécula, estos elementos se etiquetan con una fórmula molecular, un listado formal de qué y cuántos átomos hay en una molécula. (A veces sólo se utiliza la palabra fórmula, y su significado se deduce del contexto). Por ejemplo, la fórmula molecular del hidrógeno elemental es H2, siendo H el símbolo del hidrógeno y el subíndice 2 implica que hay dos átomos de este elemento en la molécula. Otros elementos diatómicos tienen fórmulas similares: O2, N2, etc. Otros elementos existen como moléculas; por ejemplo, el azufre existe normalmente como una molécula de ocho átomos, S8, mientras que el fósforo existe como una molécula de cuatro átomos, P4 (Figura \(\PageIndex{1})).
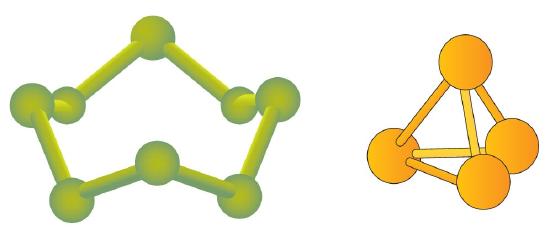
La figura \N(\PageIndex{1}) muestra dos ejemplos de cómo se representarán las moléculas en este texto. Un átomo se representa con una pequeña bola o esfera, que generalmente indica dónde está el núcleo en la molécula. Una línea cilíndrica que conecta las bolas representa la conexión entre los átomos que hacen de este conjunto de átomos una molécula. Esta conexión se llama enlace químico.