Nachrichtenmeldung
Montag, 28. Dezember 2020
NIH- und BARDA-finanzierte Studie wird bis zu 30.000 Freiwillige aufnehmen.
Personen ab 18 Jahren, die an einer Teilnahme an dieser Studie interessiert sind, können sich unter coronaviruspreventionnetwork.org, ClinicalTrials.gov und der Suchnummer NCT04611802 oder Novavax.com/PREVENT-19 informieren. Bitte wenden Sie sich nicht an die Medien-Telefonnummer oder E-Mail des NIAID, um sich für diese Studie anzumelden.
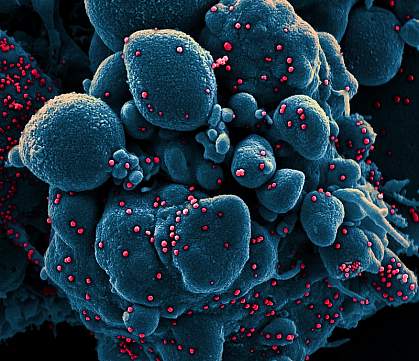 Farbige Rasterelektronenmikroskopische Aufnahme einer apoptotischen Zelle (blau), die mit SARS-COV-2-Viruspartikeln (rot) infiziert ist, isoliert aus einer Patientenprobe.NIAID
Farbige Rasterelektronenmikroskopische Aufnahme einer apoptotischen Zelle (blau), die mit SARS-COV-2-Viruspartikeln (rot) infiziert ist, isoliert aus einer Patientenprobe.NIAID Die Phase-3-Studie eines weiteren Impfstoffs gegen Coronaviren 2019 (COVID-19) hat mit der Rekrutierung erwachsener Freiwilliger begonnen. An der randomisierten, placebokontrollierten Studie werden etwa 30.000 Personen an rund 115 Standorten in den Vereinigten Staaten und Mexiko teilnehmen. Untersucht werden die Sicherheit und Wirksamkeit von NVX-CoV2373, einem von Novavax, Inc. in Gaithersburg, Maryland, entwickelten Impfstoffkandidaten. Novavax leitet die Studie als behördlicher Sponsor. Das National Institute of Allergy and Infectious Diseases (NIAID), Teil der National Institutes of Health, und die Biomedical Advanced Research and Development Authority (BARDA), Teil des U.S. Department of Health and Human Services Office of the Assistant Secretary for Preparedness and Response, finanzieren die Studie.
„Die Bewältigung der beispiellosen Gesundheitskrise von COVID-19 hat außergewöhnliche Anstrengungen seitens der Regierung, der Wissenschaft, der Industrie und der Gemeinschaft erfordert“, sagte NIAID-Direktor Anthony S. Fauci, M.D. „Der Start dieser Studie – der fünfte COVID-19-Impfstoffkandidat, der in einer Phase-3-Studie in den Vereinigten Staaten getestet wird – zeigt unsere Entschlossenheit, die Pandemie durch die Entwicklung mehrerer sicherer und wirksamer Impfstoffe zu beenden.“
Die Studie wird in Zusammenarbeit mit der Operation Warp Speed (OWS) durchgeführt, einer behördenübergreifenden Zusammenarbeit unter der Leitung des HHS und des Verteidigungsministeriums, die darauf abzielt, die Entwicklung, Herstellung und Verteilung medizinischer Gegenmaßnahmen für COVID-19 zu beschleunigen. Einige der teilnehmenden US-Studienzentren sind Teil des vom NIAID unterstützten COVID-19-Präventionsnetzwerks (CoVPN). Das CoVPN umfasst bestehende, vom NIAID unterstützte Netzwerke für klinische Forschung mit Fachwissen über Infektionskrankheiten und wurde für eine schnelle und gründliche Bewertung von Impfstoffkandidaten und monoklonalen Antikörpern zur Vorbeugung von COVID-19 konzipiert.
Die Freiwilligen werden vor ihrer Teilnahme an der Studie um eine informierte Zustimmung gebeten. Sie werden in zwei Gruppen eingeteilt: Personen im Alter von 18 bis 64 Jahren und Personen im Alter von 65 Jahren und älter, wobei angestrebt wird, mindestens 25 % aller Freiwilligen, die 65 Jahre oder älter sind, in die Studie aufzunehmen. Die Organisatoren der Studie legen auch großen Wert auf die Rekrutierung von Personen, die ein höheres Risiko für eine schwere COVID-19-Erkrankung haben, darunter Schwarze (einschließlich Afroamerikaner), amerikanische Ureinwohner, Menschen lateinamerikanischer oder hispanischer Abstammung und Menschen mit Grunderkrankungen wie Fettleibigkeit, chronischen Nierenerkrankungen oder Diabetes.
„Wir sind so schnell so weit gekommen, aber wir müssen die Ziellinie erreichen“, sagte NIH-Direktor Francis S. Collins, M.D., Dr. Francis S. Collins, Direktor des NIH: „Dazu sind mehrere Impfstoffe mit unterschiedlichen Ansätzen erforderlich, um sicherzustellen, dass alle Menschen sicher und wirksam vor dieser tödlichen Krankheit geschützt sind.“
Nach der Abgabe einer Nasopharyngeal- und Blutprobe werden die Teilnehmer nach dem Zufallsprinzip einer intramuskulären Injektion entweder des Prüfimpfstoffs oder eines Kochsalz-Placebos zugewiesen. Die Zuteilung erfolgt im Verhältnis 2:1, d. h. zwei Probanden erhalten den Prüfimpfstoff für jeden Probanden, der das Placebo erhält. Da die Studie verblindet ist, wissen weder die Prüfer noch die Teilnehmer, wer den Impfstoffkandidaten erhält. Eine zweite Injektion wird 21 Tage nach der ersten verabreicht.
Die Teilnehmer werden engmaschig auf mögliche Nebenwirkungen des Impfstoffs überwacht und werden gebeten, zu bestimmten Zeitpunkten nach jeder Injektion und während der folgenden zwei Jahre Blutproben abzugeben. Die Wissenschaftler werden die Blutproben analysieren, um Immunreaktionen auf SARS-CoV-2, das Virus, das COVID-19 verursacht, zu erkennen und zu quantifizieren. Dabei werden spezielle Tests verwendet, um zwischen der Immunität infolge einer natürlichen Infektion und der durch den Impfstoff ausgelösten Immunität zu unterscheiden. Der primäre Endpunkt der Studie ist die Feststellung, ob NVX-CoV2373 im Vergleich zu Placebo sieben oder mehr Tage nach der zweiten Injektion eine symptomatische COVID-19-Erkrankung verhindern kann.
Novavax‘ Prüfimpfstoff NVX-CoV2373 wird aus einer stabilisierten Form des Coronavirus-Spike-Proteins unter Verwendung der rekombinanten Protein-Nanopartikeltechnologie des Unternehmens hergestellt. Die gereinigten Protein-Antigene im Impfstoff können sich nicht replizieren und können kein COVID-19 verursachen. Der Impfstoff enthält außerdem ein proprietäres Adjuvans, MatrixM™. Adjuvantien sind Zusatzstoffe, die die gewünschte Reaktion des Immunsystems auf den Impfstoff verstärken. NVX-CoV2373 wird in flüssiger Form verabreicht und kann bei Temperaturen über dem Gefrierpunkt (35° bis 46°F) gelagert, gehandhabt und verteilt werden. Eine einzelne Impfstoffdosis enthält 5 Mikrogramm (mcg) Protein und 50 mcg Adjuvans.
In Tierversuchen führte die Impfung mit NVX-CoV2373 zur Bildung von Antikörpern, die das Spike-Protein des Coronavirus daran hinderten, sich an die Zelloberflächenrezeptoren zu binden, auf die das Virus abzielt, und so eine virale Infektion verhinderten. Die Ergebnisse einer klinischen Phase-1-Studie, die im New England Journal of Medicine veröffentlicht wurden, zeigen, dass NVX-CoV2373 im Allgemeinen gut vertragen wurde und höhere Antikörperspiegel hervorrief als in Blutproben von Personen, die sich von einer klinisch signifikanten COVID-19-Infektion erholt hatten. NVX-CoV2373 wird auch in einer Phase-2b-Studie in Südafrika untersucht, in die inzwischen 4.422 Freiwillige aufgenommen wurden. Daten aus einer Phase-1/2-Fortsetzungsstudie in den Vereinigten Staaten und Australien werden bereits im ersten Quartal 2021 erwartet. Novavax hat außerdem vor kurzem die Rekrutierung von mehr als 15.000 Freiwilligen für eine Phase-3-Studie mit dem Impfstoffkandidaten in Großbritannien abgeschlossen, in der ebenfalls zwei Injektionen von 5 mcg Protein und 50 mcg Matrix-M-Adjuvans im Abstand von 21 Tagen getestet werden.
Ein unabhängiges Data and Safety Monitoring Board (DSMB) wird die sichere und ethische Durchführung der Studie überwachen. Alle klinischen Phase-3-Studien mit Impfstoffkandidaten, die von OWS unterstützt werden, werden von einem gemeinsamen DSMB überwacht, das in Absprache mit der NIH-Initiative Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV) entwickelt wurde.
Erwachsene, die an einer Teilnahme an dieser Studie interessiert sind, können Coronaviruspreventionnetwork.org, Novavax.com/PREVENT-19 oder ClinicalTrials.gov besuchen und den Identifikator NCT04611802 suchen.
Über das COVID-19-Präventionsnetzwerk: Das COVID-19-Präventionsnetzwerk (CoVPN) wurde vom National Institute of Allergy and Infectious Diseases (NIAID) an den U.S. National Institutes of Health gegründet, um auf die globale Pandemie zu reagieren. Durch das CoVPN nutzt das NIAID die Expertise seiner bestehenden Forschungsnetzwerke und globalen Partner im Bereich Infektionskrankheiten, um den dringenden Bedarf an Impfstoffen und Antikörpern gegen SARS-CoV-2 zu decken. Das CoVPN wird an der Entwicklung und Durchführung von Studien arbeiten, um eine schnelle und gründliche Bewertung von Impfstoffen und Antikörpern zur Prävention von COVID-19 zu gewährleisten. Das CoVPN hat seinen Sitz im Fred Hutchinson Cancer Research Center. Weitere Informationen über das CoVPN finden Sie unter: coronaviruspreventionnetwork.org.
Über das HHS, ASPR und BARDA: Das HHS arbeitet daran, die Gesundheit und das Wohlergehen aller Amerikaner zu verbessern und zu schützen, indem es effektive Gesundheits- und Humandienste bereitstellt und Fortschritte in der Medizin, im öffentlichen Gesundheitswesen und in den sozialen Diensten fördert. Die Aufgabe der ASPR ist es, Leben zu retten und die Amerikaner vor den Gesundheitsbedrohungen des 21. Jahrhunderts zu schützen. Innerhalb des ASPR investiert die BARDA in Innovation, fortschrittliche Forschung und Entwicklung, Beschaffung und Herstellung medizinischer Gegenmaßnahmen – Impfstoffe, Medikamente, Therapeutika, Diagnoseinstrumente und nicht-pharmazeutische Produkte, die zur Bekämpfung von Gesundheitsbedrohungen benötigt werden. Bis heute haben BARDA-geförderte Produkte 55 FDA-Zulassungen, Lizenzen oder Freigaben erhalten. Weitere Informationen über die Unterstützung des Bundes für die landesweite COVID-19-Reaktion finden Sie unter www.coronavirus.gov.
Über die Operation Warp Speed: OWS ist eine Partnerschaft zwischen Komponenten des Gesundheitsministeriums und des Verteidigungsministeriums, die mit privaten Firmen und anderen Bundesbehörden zusammenarbeitet und die bestehenden HHS-weiten Bemühungen koordiniert, um die Entwicklung, Herstellung und Verteilung von COVID-19-Impfstoffen, -Therapeutika und -Diagnostika zu beschleunigen.
Über das National Institute of Allergy and Infectious Diseases: Das NIAID betreibt und unterstützt Forschung – an den NIH, in den Vereinigten Staaten und weltweit – zur Erforschung der Ursachen von Infektions- und immunvermittelten Krankheiten und zur Entwicklung besserer Mittel zur Prävention, Diagnose und Behandlung dieser Krankheiten. Pressemitteilungen, Informationsblätter und andere NIAID-bezogene Materialien sind auf der NIAID-Website zu finden.
Über die National Institutes of Health (NIH):Die NIH, die nationale Behörde für medizinische Forschung, umfasst 27 Institute und Zentren und ist Teil des US-Gesundheitsministeriums (U.S. Department of Health and Human Services). Die NIH sind die wichtigste Bundesbehörde, die medizinische Grundlagen-, klinische und translationale Forschung durchführt und unterstützt. Sie erforschen die Ursachen, Behandlungen und Heilmittel für häufige und seltene Krankheiten. Weitere Informationen über die NIH und ihre Programme finden Sie unter www.nih.gov.
NIH…Turning Discovery Into Health®
###