US Pharm. 2017;42(4):HS16-HS20.
ABSTRACT: Nekrotisierende Weichteilinfektionen (NSTI) sind eine Art von schweren bakteriellen Infektionen, die eine schnelle Erkennung und Intervention durch Ärzte und Chirurgen in Kombination mit einer rechtzeitigen antibiotischen Behandlung erfordern. Diese Infektionen können eine polymikrobielle Ursache haben, aber in den meisten Fällen ist Methicillin-resistenter Staphylococcus aureus beteiligt. Bei der Behandlung von NSTI ist Zeit das A und O, um Komplikationen wie Amputationen zu vermeiden, und vor kurzem wurden neue Medikamente in die Liste der Behandlungsmöglichkeiten aufgenommen. Zu diesen neuen Antibiotika gehören Tedizolid (Sivextro), Oritavancin (Orbactiv) und Dalbavancin (Dalvance). Vor allem die lange Halbwertszeit von Dalbavancin und Oritavancin ermöglicht entweder eine einmalige oder eine wöchentliche Verabreichung.
Nekrotisierende Weichteilinfektion (NSTI) ist ein weiter gefasster Begriff als nekrotisierende Fasziitis, da die Infektion bei NSTI über die Faszie hinausgehen kann. Umgangssprachliche Bezeichnungen sind „fleischfressende Bakterien“ und „fleischfressende Infektion“. Diese Art der Infektion wurde erstmals im 5. Jahrhundert v. Chr. von Hippokrates erwähnt, der sie wie folgt beschrieb: „Viele wurden vom Erysipel am ganzen Körper befallen, wenn die erregende Ursache ein banaler Unfall war … Fleisch, Sehnen und Knochen fielen in großen Mengen ab … es gab viele Todesfälle.“1 Seitdem wurden andere beschreibende Begriffe verwendet, um die NSTI zu charakterisieren, wie „phagedämisches Geschwür, phagedämische Gangrän, gangränöses Geschwür, bösartiges Geschwür, fauliges Geschwür oder Krankenhausgangrän“.2 Der Begriff Gangrän wird immer noch verwendet, wie bei der Fournier-Gangrän, die eine Nekrose des Dammes und des Skrotums ist.3
Epidemiologie
Das Risiko einer NSTI ist mit etwa 1.000 Fällen pro Jahr in den Vereinigten Staaten insgesamt gering. Diese Zahl könnte jedoch ansteigen, vielleicht aufgrund eines größeren Bewusstseins und der Anerkennung des Krankheitszustands, zunehmender Antibiotikaresistenz oder erhöhter bakterieller Virulenzfähigkeit.4
Etiologie
NSTI werden nach anatomischer Lage klassifiziert (z. B. Fournier-Gangrän), treten jedoch am häufigsten an den Extremitäten, dem Damm und den Genitalien auf. Zu den häufigen bakteriellen Erregern gehören Methicillin-resistenter Staphylococcus aureus (MRSA), gramnegative Organismen und Anaerobier sowie Streptokokken der Gruppe A (GAS).4
Klinische Präsentation und Diagnose
Die anfängliche Präsentation von Patienten mit NSTI kann die Symptome einer Zellulitis nachahmen, einschließlich Erythem, Schwellung, Fieber, Verhärtung und Ödem außerhalb des Bereichs der Hautveränderungen.4 Die Patienten können Schmerzen beschreiben, die denen einer Muskelzerrung ähneln.5 Zu den Symptomen, die den Verdacht auf eine NSTI verstärken sollten, gehören Schmerzen, die in keinem Verhältnis zum Untersuchungsbefund stehen (zu Beginn des Krankheitsverlaufs), das Vorhandensein von Blasen, Hautekchymosen, die einer Hautnekrose vorausgehen, Gase im Gewebe und eine kutane Anästhesie. Darüber hinaus deutet die Chronologie der Infektion bei Patienten mit NSTI im Vergleich zu Patienten mit einer Cellulitisdiagnose auf einen viel schnelleren Krankheitsverlauf hin.4 Daher sollte bei Patienten mit Verdacht auf Cellulitis die Diagnose einer nekrotisierenden Fasziitis ausgeschlossen werden.6 Damit eine Infektion auftreten kann, müssen die Bakterien in den Blutkreislauf gelangen, und zwar in der Regel durch eine auslösende Wunde (eine Verletzung der Epithel- oder Schleimhautoberfläche), wie z. B. eine kleine Schnitt- oder Kratzwunde, einen Insektenstich, ein Hautgeschwür oder eine postoperative Wunde; gelegentlich lassen sich solche Verletzungen jedoch nicht identifizieren. Zu den Risikofaktoren für eine NSTI gehören ein geschwächtes Immunsystem (AIDS, Steroidtherapie), Übergewicht, Alkoholmissbrauch, Krebs, Diabetes mellitus, periphere Gefäßerkrankungen, Nierenerkrankungen, Unterernährung und andere chronische Erkrankungen. Aktiver parenteraler Drogenkonsum (intravenöse oder subkutane Injektion illegaler Substanzen) wurde ebenfalls als Risikofaktor identifiziert, insbesondere im städtischen Umfeld.7
Review der Leitlinien
Die Praxisleitlinien 2014 der Infectious Diseases Society of America (IDSA) für die Diagnose und Behandlung von Haut- und Weichteilinfektionen enthalten Informationen zum Umgang mit allen Arten von Haut- und Weichteilinfektionen, von der einfachen Zellulitis bis zum kutanen Milzbrand bei gesunden Menschen und geschwächten Patienten. Da diese Infektionen in allen Altersgruppen auftreten, enthalten die Leitlinien Empfehlungen sowohl für pädiatrische als auch für erwachsene Patienten. Ein Unterabschnitt der Leitlinien enthält Informationen zu NSTI. Spezifische Behandlungsempfehlungen werden auf der Grundlage einer Bewertung gegeben, die die Stärke der Evidenz für die Empfehlung gemäß dem IDSA/U.S. Public Health Service Grading System für die Bewertung von Empfehlungen in klinischen Leitlinien angibt.6 Die Leitlinie gibt Antworten auf 24 klinische Fragen, einschließlich zweier Fragen, die sich auf NSTI beziehen.
Die erste Frage, die sich auf NSTI bezieht, wird in den Leitlinien behandelt: Was ist die bevorzugte Bewertung und Behandlung von nekrotisierender Fasziitis, einschließlich Fournier-Gangrän? Die erste Empfehlung lautet, bei Patienten mit aggressiven Infektionen mit Anzeichen systemischer Toxizität oder bei Verdacht auf nekrotisierende Fasziitis oder Gasgangrän umgehend einen Chirurgen aufzusuchen.6 Darauf folgen zwei Empfehlungen zur Antibiotikatherapie. Die anfängliche antimikrobielle Therapie sollte breit gefächert sein, um sowohl Infektionen durch einen einzelnen Organismus als auch durch mehrere Organismen abzudecken. Darüber hinaus wird Penicillin in Kombination mit Clindamycin bei nachgewiesener nekrotisierender GAS-Fasziitis empfohlen. Alle drei Empfehlungen werden als stark eingestuft, wobei die Qualität der Belege gering ist, was bedeutet, dass die erwünschten Wirkungen eindeutig die unerwünschten Wirkungen überwiegen. Nach den Empfehlungen folgt ein Überblick über die Evidenz, gefolgt von einem Überblick über die häufigsten klinischen Merkmale, die mikrobiologischen Ursachen (monomikrobiell versus polymikrobiell), die Diagnose und die Behandlung.
Ein separater Abschnitt der Leitlinien befasst sich mit dem Management der clostridialen NSTI gemäß der folgenden Frage: Welches ist der geeignete Ansatz für die Bewertung und Behandlung von clostridialer Gasgangrän oder Myonekrose? Zunächst sollte eine dringende chirurgische Exploration der vermuteten Gasgangränstelle und ein Débridement des betroffenen Gewebes durchgeführt werden. Sofern keine eindeutige mikrobiologische Ursache vorliegt, wird eine Breitspektrum-Antibiotikatherapie empfohlen. Im Falle einer Clostridien-Myonekrose wird Penicillin in Kombination mit Clindamycin empfohlen. Schließlich wird eine hyperbare Sauerstofftherapie nicht empfohlen. Für alle diese Empfehlungen gibt es eine starke Empfehlung, und bis auf die chirurgische Empfehlung haben alle eine geringe Qualität der Evidenz (die chirurgische Empfehlung hat eine mäßige Qualität der Evidenz). Der Abschnitt über NSTI schließt mit einem Überblick über die Evidenz zu diesen Empfehlungen.6
NSTI unterscheiden sich von weniger schweren Hautinfektionen nicht nur durch ihr klinisches Erscheinungsbild und andere systemische Manifestationen, sondern erfordern auch einen anderen Behandlungsansatz. Es gibt viele Arten von NSTI, aber die antibiotische Behandlung und der chirurgische Ansatz sind bei allen Arten ähnlich, und ein chirurgischer Eingriff ist der primäre Ansatz, wenn eine NSTI zu erwarten ist. Bei den meisten Patienten sind mehrere Besuche im Operationssaal (OP) erforderlich, bis kein Débridement mehr notwendig ist.6
Medikamentöse Behandlung
Die anfängliche Auswahl der Antibiotika sollte Wirkstoffe umfassen, die gegen ein breites Spektrum von Organismen wirksam sind, darunter Aerobier, MRSA und Anaerobier (TABELLE 1).6 Bei der Auswahl der Antibiotika sollten patientenspezifische Faktoren wie frühere Antibiotikaexposition, begleitende Erkrankungen, Organstörungen und Allergien berücksichtigt werden. Wie bei der Behandlung der meisten Infektionen gehört zu einem guten antimikrobiellen Stewardship auch die Optimierung der Antibiotikatherapie auf das engste Spektrum, sobald eine mikrobiologische Ursache identifiziert wurde.
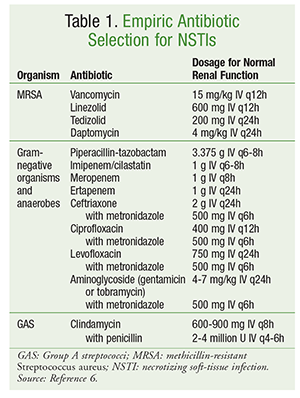
Die definitive Behandlung von NSTI umfasst eine Vielzahl von Antibiotika. Bei polymikrobiellen Infektionen wird häufig eine Breitspektrum-Antibiotikatherapie durchgeführt. Bei durch GAS verursachten Infektionen sollten sowohl Clindamycin als auch Penicillin eingesetzt werden. Der Zusatz von Clindamycin unterdrückt die Toxin- und Zytokinproduktion, und die Verwendung von Penicillin bietet eine Absicherung für den Fall einer Clindamycin-Resistenz bei GAS. Bei Infektionen, die durch Methicillin-empfängliche S. aureus verursacht werden, ist die Verwendung von Nafcillin, Oxacillin oder Cefazolin vorzuziehen. Clostridien-Infektionen sollten mit Clindamycin in Kombination mit Penicillin behandelt werden. Die Antibiotikatherapie wird in der Regel so lange fortgesetzt, bis kein weiteres Débridement mehr erforderlich ist, der Patient eine klinische Besserung zeigt und seit 48 bis 72 Stunden kein Fieber mehr auftritt.6
Seit der Veröffentlichung der IDSA-Leitlinien 2014 wurden mehrere neue Antibiotika für die Behandlung komplizierter Haut- und Weichteilinfektionen zugelassen. Diese Wirkstoffe sind Tedizolid (Sivextro), Oritavancin (Orbactiv) und Dalbavancin (Dalvance).
Tedizolid ist ein Oxazolidinon-Antibiotikum, das Linezolid ähnelt. Es hat eine zuverlässige Aktivität gegen MRSA und andere multiresistente grampositive Organismen. Im Gegensatz zu Linezolid, das zweimal täglich verabreicht wird, wird Tedizolid in einer einzigen Tagesdosis oral oder intravenös verabreicht. Tedizolid kann im Vergleich zu Linezolid ein günstigeres Nebenwirkungs- und Wechselwirkungsprofil aufweisen.8 Obwohl Tedizolid bei der Behandlung akuter bakterieller Haut- und Hautstrukturinfektionen untersucht wurde, ist es bei NSTI nicht untersucht worden.
Dalbavancin und Oritavancin sind Lipoglykopeptide, die für die Behandlung akuter bakterieller Haut- und Hautstrukturinfektionen zugelassen sind. Diese Wirkstoffe zeichnen sich durch eine lange Halbwertszeit aus, die eine einmalige oder wöchentliche Gabe ermöglicht. Die Dosierung von Dalbavancin muss bei Patienten mit einer Kreatinin-Clearance <30 ml/Minute reduziert werden. Oritavancin erfordert keine Dosisanpassungen im Zusammenhang mit Organfunktionsstörungen, sollte aber nicht bei Patienten angewendet werden, die Heparin erhalten, da es die Gerinnungstests künstlich verlängert. Oritavancin kann auch die Wirkung von Vitamin-K-Antagonisten wie Warfarin verstärken.9 Beide Wirkstoffe haben sich bei der Behandlung von Haut- und Hautstrukturinfektionen bewährt, wurden jedoch nicht für den Einsatz bei nekrotisierenden Infektionen untersucht.
Zu den ergänzenden Therapien für NSTI gehören IV-Immunglobulin (IVIG) und hyperbare Sauerstofftherapie. Es wird angenommen, dass IVIG aufgrund einer möglichen Neutralisierung der bei Streptokokkeninfektionen gebildeten Toxine von Vorteil ist. Die Reduzierung dieser Toxine könnte möglicherweise einen Teil des Organversagens, des Schocks und der Gewebezerstörung verringern, die bei NSTI häufig auftreten.6 Zum Zeitpunkt der Veröffentlichung der IDSA-Leitlinien (April 2014) berichteten eine Beobachtungsstudie und eine Studie aus Europa über einige Erfolge bei der Verwendung von IVIG bei Streptokokkeninfektionen.6 Da es jedoch keine Belege für die Wirksamkeit gibt, wird der Einsatz von IVIG derzeit nicht empfohlen.
In einer neueren Studie wurde die Wirksamkeit von Clindamycin und IVIG bei invasiven GAS-Infektionen beschrieben.10 Vierundachtzig Patienten erfüllten die Kriterien für eine invasive GAS-Erkrankung, und IVIG wurde bei 14 Patienten eingesetzt, darunter acht mit nekrotisierender Fasziitis. Die Sterblichkeit war bei Patienten, die mit Clindamycin und IVIG behandelt wurden, niedriger, aber dieser Unterschied war nicht signifikant. Obwohl es keinen statistischen Unterschied in der Sterblichkeitsrate gab, wenn IVIG zusätzlich zu Clindamycin verabreicht wurde, schlugen die Autoren vor, dass es bei Erwachsenen mit einer schwereren Erkrankung einen möglichen Nutzen geben könnte.10
Die hyperbare Sauerstofftherapie (HBOT) wurde für die Behandlung von Gasgangrän befürwortet, aber ihre Rolle ist umstritten.6 Laborstudien haben gezeigt, dass sauerstoffreiche Gewebezustände dazu beitragen, das Wachstum von Clostridium perfringens zu unterdrücken und die Abwehrkräfte des Wirts gegen fremde Zellen zu stärken, aber es fehlen Kriterien, um Patienten zu identifizieren, die davon profitieren könnten, und um den geeigneten Zeitpunkt für den Beginn der Therapie zu bestimmen.6,11 Nichts sollte ein sofortiges chirurgisches Débridement und die Verabreichung von Antibiotika verzögern, da beides wichtig ist, um das Überleben zu sichern.6
Da die meisten veröffentlichten Studien klein und wenig aussagekräftig waren, wurde eine Studie durchgeführt, um Daten über den Einsatz der HBOT von mehreren Zentren mit HBOT-Einrichtungen auszuwerten.11 Über einen Zeitraum von drei Jahren wurden in 14 HBOT-Einrichtungen 1.583 Fälle von NSTI behandelt und in 117 Fällen eine adjuvante HBOT durchgeführt. Die HBOT-Gruppe hatte höhere Kosten und eine längere Verweildauer im Krankenhaus als die Kontrollgruppe, wies jedoch eine deutlich niedrigere Krankenhaussterblichkeit auf (5 % gegenüber 12 %; P <.05). Bei Berücksichtigung des Schweregrads der Erkrankung wiesen die am schwersten erkrankten HBOT-Patienten signifikant niedrigere Sterblichkeits- und Komplikationsraten auf, aber es gab keine Unterschiede bei der Aufenthaltsdauer oder den Kosten. Eine multivariate Analyse zeigte, dass Patienten, die keine HBOT erhielten, ein höheres Risiko hatten, während des Krankenhausaufenthalts zu sterben (Odds Ratio, 10,6; 95% CI 5,2-25,1). Mit jeder Zunahme des Schweregrads der Erkrankung erhöhte sich das Sterberisiko.
Diese Studie mit 14 HBOT-Einrichtungen scheint bessere Ergebnisse zu zeigen, insbesondere für die kränksten Patienten, die direkt in ein Zentrum eingewiesen werden, das diese Behandlung anbieten kann.11 Dies mildert jedoch nicht die Kontroverse um den Einsatz der HBOT, da diese Untersuchung mehrere Einschränkungen aufweist. Die Studie wurde retrospektiv anhand einer Verwaltungsdatenbank an akademischen medizinischen Zentren durchgeführt. Außerdem kann es sein, dass in einigen Zentren ein Dritter Eigentümer der HBOT-Einrichtung ist, so dass die Ergebnisse weniger auf die Patienten in diesen Einrichtungen übertragbar sind. Eine randomisierte, kontrollierte Studie wäre hilfreich, um den letztendlichen Nutzen dieser Therapie zu ermitteln.
Komplikationen
Die Sterblichkeitsrate im Zusammenhang mit NSTI liegt bei 30 bis 70 % bei Patienten mit nekrotisierender Fasziitis des GAS in Verbindung mit Hypotonie und Organversagen.6 Da die Behandlung mehrere Besuche im OP erfordert, werden routinemäßig große Wunden und mögliche Amputationen gemeldet. Andere Komplikationen wie rekonstruktive Chirurgie, Sepsis, nosokomiale Infektionen und verlängerte Intensivpflegezeiten aufgrund der Entwicklung eines Multisystem-Organversagens sind häufige Komplikationen der NSTI.12
Informationen über die langfristigen Auswirkungen der NSTI wurden in ausführlichen Interviews mit 18 Überlebenden gesammelt.12,13 Die Forscher fanden heraus, dass die Lebensqualität durch die körperliche Funktion und die anhaltenden Schmerzen erheblich beeinträchtigt wurde. Auch die Auswirkungen der Erfahrung auf familiäre und andere Beziehungen wurden als erheblich eingestuft. Mehrere Überlebende beschrieben die langfristigen psychologischen Folgen der Krankheit, einschließlich Depressionen und posttraumatischem Stress.
Schlussfolgerung
Krankenhausapotheker sind sehr gut geeignet, um die Versorgung von Patienten mit NSTI zu unterstützen, einschließlich der Rationalisierung der Versorgung, der Förderung von antimikrobiellem Stewardship und der Verbesserung der klinischen Ergebnisse, der Kostensenkung, der Minimierung von Komplikationen und der Rückübernahme. Zu den weiteren Aufgaben des Apothekers gehört es, die idealen Patienten für die neuen, aber teureren Therapeutika (z. B. Oritavancin) zu identifizieren und Wechselwirkungen (z. B. mit Antikoagulantien) mit diesen Antibiotikaklassen zu erkennen.
1. Descamps V, Aitken J, Lee MG. Hippocrates on necrotising fasciitis. Lancet. 1994;344:556.
2. Loudon I. Necrotising fasciitis, hospital gangrene, and phagedena. Lancet. 1994;344:1416-1419.
3. Sarani B, Strong M, Pascual J, Schwab CW. Nekrotisierende Fasziitis: aktuelle Konzepte und Überblick über die Literatur. J Am Coll Surg. 2009;208:279-288.
4. Hakkarainen TW, Kopari NM, Pham TN, Evans HL. Nekrotisierende Weichteilinfektionen: Übersicht und aktuelle Konzepte für Behandlung, Versorgungssysteme und Ergebnisse. Curr Probl Surg. 2014;51:344-362.
5. CDC. Nekrotisierende Fasziitis: eine seltene Krankheit, besonders für Gesunde. www.cdc.gov/features/necrotizingfasciitis/. Accessed November 29, 2016.
6. Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the Infectious Diseases Society of America. Clin Infect Dis. 2014;59:147-159.
7. Bosshardt TL, Henderson VJ, Organ CH Jr. Necrotizing soft-tissue infections. Arch Surg. 1996;131:846-852.
8. Kisgen JJ, Mansour H, Unger NR, Childs LM. Tedizolid: ein neues antimikrobielles Oxazolidinon. Am J Health Syst Pharm. 2014;71:621-633.
9. Roberts KD, Sulaiman RM, Rybak MJ. Dalbavancin und Oritavancin: ein innovativer Ansatz für die Behandlung von grampositiven Infektionen. Pharmacotherapy. 2015;35:935-948.
10. Carapetis JR, Jacoby P, Carville K, et al. Wirksamkeit von Clindamycin und intravenösem Immunglobulin und Krankheitsrisiko bei Kontaktpersonen bei invasiven Streptokokken-Infektionen der Gruppe A. Clin Infect Dis. 2014;59:358-365.
11. Shaw JJ, Psoinos C, Ernhoff TA, et al. Not just full of hot air: hyperbaric oxygen therapy increases survival in cases of necrotizing soft tissue infections. Surg Infect (Larchmt). 2014;15:328-335.
12. Hakkarainen TW, Burkette Ikebata N, Bulger E, Evans HL. Moving beyond survival as a measure of success: understanding the patient experience of necrotizing soft-tissue infections. J Surg Res. 2014;192:143-149.
13. Miller LG, Perdreau-Remington F, Rieg G, et al. Nekrotisierende Fasziitis verursacht durch gemeindeassoziierten Methicillin-resistenten Staphylococcus aureus in Los Angeles. New Engl J Med. 2005;352:1445-1453.