Flaviviradae er en stor familie af virale patogener, der er ansvarlige for at forårsage alvorlig sygdom og dødelighed hos mennesker og dyr. Familien består af tre slægter: Flavivirus, Pestivirus og Hepacivirus. Flavivirus-slægten, som er den største af de tre, indeholder mere end 70 vira, herunder Denguevirus (DV), japansk encephalitisvirus (JEV), West Nile-virus (WNV), gul febervirus (YFV) og zikavirus (ZIKV). Flavivirusser udviser morfologisk ensartethed med et icosaedrisk kapsid og en tætsiddende, spidsformet hyldest. Kapsidets størrelse er ca. 30 nm, og hele virionen måler 45 nm. Flavivirusenes genom er et enkeltstrenget sense-RNA med en størrelse på ca. 10 kb. Det koder for 3 strukturelle proteiner: capsid (C-protein), membran (M, der udtrykkes som prM, forløberen for M, og hjulekuvert (E-protein) samt 7 ikke-strukturelle proteiner: NS1, NS2A, NS2B, NS3, NS4A, NS4B og NS5 (figur 1 a.b).
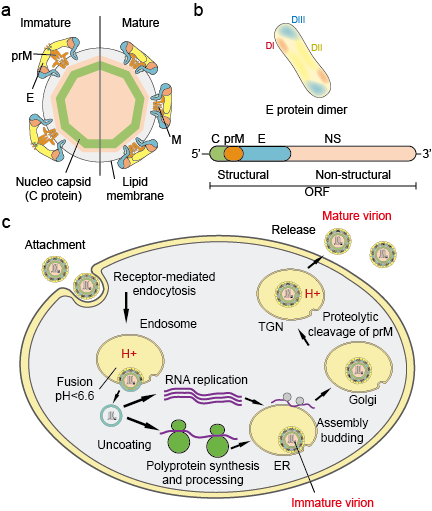
Figur 1. Flaviviruspartikler (a), proteiner (b) og livscyklus (c).
Browse All Flavivirus Related Products
Flavivirus livscyklus:
Virioner sætter sig fast på overfladen af en værtscelle og kommer efterfølgende ind i cellen ved receptormedieret endocytose (Figur 1c). Der er blevet identificeret adskillige primære receptorer og co-receptorer med lav affinitet for flavivirus. Forsuring af den endosomale vesikel udløser konformationsændringer i virionen, fusion af viral- og cellemembranen og adskillelse af partiklerne. Når genomet er frigivet i cytoplasmaet, oversættes det positivt-sense RNA til et enkelt polyprotein, der behandles co- og posttranslationelt af virale proteaser og værtsproteaser. Replikation af genomet sker på intracellulære membraner. Virus samling sker på overfladen af det endoplasmatiske reticulum (ER), når de strukturelle proteiner og det nysyntetiserede RNA knopper ind i lumenet af ER’et. De resulterende ikke-infektiøse, umodne virale og subvirale partikler transporteres gennem det trans-Golgi-netværk (TGN). De umodne virionpartikler spaltes af værtsproteasen furin, hvorved der dannes modne, infektiøse partikler. Subvirale partikler spaltes også af furin. Modne virioner og subvirale partikler frigives efterfølgende ved eksocytose.
Flavivirus-epidemiologi:
Flavivirus, der overføres af myg i naturen i en eller flere forskellige eller overlappende cyklusser, der omfatter en myggevektor, generelt Aedes-myg for YFV og DENV og Culex-myg for JEV og WNV, og en pattedyr- eller fuglevært. Overførsel mellem myg og hvirveldyrværter betegnes som horisontal overførsel og forårsager sygdom hos hvirveldyr. I modsætning til horisontal transmission kan myggebårne flavivirusser opretholdes i miljøet gennem vertikal, dvs. transgenerationel, transmission, som gør det muligt at sprede flavivirusser udelukkende i myg. Det mest direkte bevis for vertikal overførsel af myggebårne flavivirusser stammer fra isolering af virus fra inficerede larver, formentlig ved transovariel overførsel. Denne observation er i overensstemmelse med påvisningen af virale antigener i ovarievæv fra inficerede myg. (Figur 2)
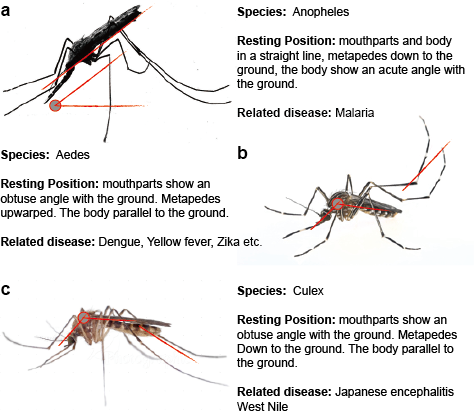
Figur 2. Tre typiske myg, der overfører sygdomme.
Flavivirusser har en global udbredelse, og nogle medlemmer af slægten udgør et stort folkesundhedsproblem (f.eks. gul febervirus , denguevirus , West Nile-virus og japansk encephalitisvirus ) med høj morbiditet og/eller mortalitet. I det sidste årti har flavivirusser udvist en øget prævalens og udgør en risiko for mere end 3 mia. mennesker på verdensplan, hvilket gør dem til et paradigme for nye sygdomme.
I de sidste 50 år har mange flavivirusser, såsom dengue-, West Nile- og gul febervirus, udvist en dramatisk stigning i incidens, sygdomsgrad og/eller geografisk udbredelse. Miljøafledte virale patogener udviser relativt ensartede epidemiologiske karakteristika. Myg, flåter og bidende fluer fungerer som vektorer for de fleste virussygdomme hos mennesker. Sygdomme hos mennesker opstår, når vektorerne er aktive, typisk om foråret, sommeren og efteråret i tempererede klimaer, og de udviser ofte forskellige epidemiologiske karakteristika, der svarer til vektorens levested (figur 3).
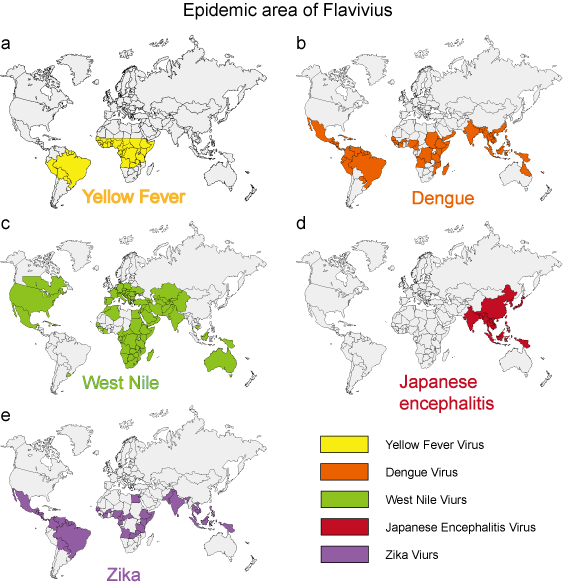
Figur 3. Det epidemiske område for 5 typiske flavivirus.
Manifestationer:
Flavivirus varierer meget med hensyn til deres patogene potentiale og mekanismer til at frembringe sygdom hos mennesker (tabel 1). Infektion af mennesker med både myggebårne og flåtbårne flavivirusser indledes ved afgivelse af virus gennem huden via spyt fra en inficeret leddyrs spyt. Viruset replikerer lokalt og i regionale lymfeknuder og resulterer i viremi. Blandt de vigtigste syndromer og eksempler på flavivirusser, der forårsager sygdommen, kan nævnes: encephalitis (japansk encephalitis), febril sygdom med udslæt (denguevirus), hæmoragisk feber (Kyasanur Forest disease-virus og undertiden denguevirus) og hæmoragisk feber med hepatitis (gul febervirus).
Tabel 1 Oversigt over de vigtigste flavivirusser
| Virusarter | Overførende vektor | Geografisk spredning | Syndrom |
|---|---|---|---|
| Gul feber | Myg (Aedes) | Se figur 3a | Hæmorrhagisk feber |
| Denguefeber | Myg (Aedes, Stegomyia) |
Se figur 3b | Dengue syndrom, DHF, DSS |
| West Nile feber | Myg (Culex), flåter (Argasidae) |
Se figur 3c | Denguesyndrom, encephalitis |
| Japansk encephalitis | Myg (Culex) | Se figur 3d | Encephalitis |
| Zika | Mosquito (Aedes) | Se figur 3e | Mikrocefali |
Diagnostik:
Den kliniske diagnose af de forskellige flavivirusser er ikke pålidelig på grund af de uspecifikke symptomer, og laboratoriediagnostik er obligatorisk for at bekræfte sygdommens ætiologi. Ved flavivirusinfektioner kan viruset findes i serum eller plasma, som regel 2-7 dage efter sygdomsudbruddet, og varigheden af denne viremiske fase og den påviste virale belastning varierer afhængigt af det inficerende virus (tabel 2). Almindeligvis opstår der efter 5-7 dage efter infektionens indtræden et immunrespons mod infektionen, med IgM-antistoffer, der topper efter 15 dage. Disse IgM-antistoffer kan vare fra måneder (som i tilfælde af DENV) til år (som i tilfælde af WNV-infektioner). IgG-antistoffer fremkommer efter 8-10 dage fra infektionens begyndelse og kan påvises hele livet igennem. De enkelte flavivirus’ særlige kendetegn har en markant indflydelse på de diagnostiske algoritmer, der skal anvendes til identifikation af flavivirale infektioner. Generelt har mange laboratorier valgt serologiske test til diagnosticering af infektioner forårsaget af flavivirus på grund af deres nøjagtighed og tilgængeligheden af kommercielle test baseret på høje kvalitetsstandarder. Forekomsten af serologiske krydsreaktioner mellem de forskellige vira og den tid, der er nødvendig for at påvise antistoffer i forbindelse med visse infektioner, hæmmer imidlertid serologiens anvendelighed som diagnostisk værktøj for akutte flavivirusinfektioner. Viral isolering udgør “guldstandarden” for at opnå en bekræftet flavivirusdiagnose.
Browse All Flavivirus ELSIA Kit and Flavivirus RDT Products
Tabel 2. Flavivirus-diagnosealgoritmer.
| Akut fase | Konvalescent fase | Foretrukken prøve† | Forventet viral belastning | ||
|---|---|---|---|---|---|
| YFV | RT-PCR, RT-qPCR, IgM, virusisolering | IgM, IgG | Serum, plasma og væv | Høj | |
| DENV | RT-PCR, RT-qPCR, NS1 Ag, IgM, virusisolering | IgM, IgG | IgM, IgG | Serum, plasma, CSF og PBMC’er | Op til 106 virioner/ml |
| WNV | RT-PCR, IgM, IgG | IgM, IgG | CSF og serum | Low | |
| JEV | RT-PCR, IgM, IgG | IgG | IgM, IgG | CSF, serum, blod og PBMC’er | Low |
| ZIKV | RT-PCR, IgM, IgG | IgM, IgG | CSF og serum | Low |
| Gould E A, Solomon T. Patogene flavivirusser . The Lancet, 2008, 371(9611): 500-509. | |
| Gaunt M W, Sall A A A, de Lamballerie X, et al. Fylogenetiske relationer mellem flavivirusser korrelerer med deres epidemiologi, sygdomsforbindelse og biogeografi . Journal of General Virology, 2001, 82(8): 1867-1876. | |
| Kuno G, Chang G J J J, Tsuchiya K R, et al. Phylogeny of the genus Flavivirus . Journal of virology, 1998, 72(1): 73-83. | |
| Mukhopadhyay S, Kuhn R J, Rossmann M G. A structural perspective of the flavivirus life cycle . Nature Reviews Microbiology, 2005, 3(1): 13-22. | |
| Huang Y J S, Higgs S, Horne K M E, et al. Flavivirus-mosquito interaktioner. Viruses, 2014, 6(11): 4703-4730. |