Molekylære grundstoffer
Der findes mange stoffer, der eksisterer som to eller flere atomer, der er forbundet så stærkt med hinanden, at de opfører sig som en enkelt partikel. Disse kombinationer af flere atomer kaldes molekyler. Et molekyle er den mindste del af et stof, som har stoffets fysiske og kemiske egenskaber. I nogle henseender svarer et molekyle til et atom. Et molekyle er imidlertid sammensat af mere end ét atom.
| Hydrogen, H | Syre | Sitrogen | Fluor | Chlor | Brom | Iod |
Nogle grundstoffer eksisterer naturligt som molekyler. For eksempel findes hydrogen og oxygen som molekyler med to atomer. Andre grundstoffer findes også naturligt som diatomare molekyler – et molekyle med kun to atomer (Tabel \(\PageIndex{1}\)). Som alle andre molekyler er disse grundstoffer mærket med en molekylformel, en formel liste over, hvilke og hvor mange atomer der er i et molekyle, og hvor mange. (Nogle gange bruges kun ordet formel, og dets betydning kan udledes af sammenhængen). F.eks. er molekylformlen for elementært brint H2, hvor H er symbolet for brint, og hvor subscript 2 antyder, at der er to atomer af dette grundstof i molekylet. Andre toatomige grundstoffer har lignende formler: O2, N2 og så videre. Andre grundstoffer findes som molekyler – f.eks. findes svovl normalt som et molekyle med otte atomer, S8, mens fosfor findes som et molekyle med fire atomer, P4 (figur \(\PageIndex{1}\)).
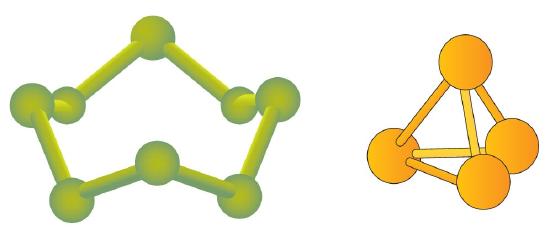
Figur \(\PageIndex{1}\) viser to eksempler på, hvordan molekyler vil blive repræsenteret i denne tekst. Et atom er repræsenteret ved en lille kugle eller kugle, som generelt angiver, hvor kernen befinder sig i molekylet. En cylinderformet linje, der forbinder kuglerne, repræsenterer forbindelsen mellem de atomer, der gør denne samling af atomer til et molekyle. Denne forbindelse kaldes en kemisk binding.