US Pharm. 2017;42(4):HS16-HS20.
ABSTRAKT: Nekrotiserande mjukdelsinfektioner (NSTI) är en typ av allvarlig bakteriell infektion som kräver snabb upptäckt och ingripande av läkare och kirurger i kombination med snabb antibiotikabehandling. Dessa infektioner kan ha en polymikrobiell orsak, men meticillinresistent Staphylococcus aureus är inblandad i de flesta fall. Vid behandling av NSTI är tiden viktig för att undvika komplikationer som t.ex. amputation, och nya läkemedel har nyligen lagts till listan över behandlingsalternativ. Dessa nya antibiotika omfattar tedizolid (Sivextro), oritavancin (Orbactiv) och dalbavancin (Dalvance). Den långa halveringstiden för både dalbavancin och oritavancin gör det möjligt att använda antingen en engångsdosregim eller dosering en gång i veckan.
Nekrotiserande mjukdelsinfektion (NSTI) är en bredare term än nekrotiserande fasciit, eftersom infektionen vid NSTI kan sträcka sig bortom fascian. I vardagliga termer ingår ”köttätande bakterier” och ”köttätande infektion”. Denna typ av infektion noterades för första gången på 500-talet f.Kr. av Hippokrates, som beskrev den på följande sätt: ”Många angreps av erysipelas över hela kroppen när den spännande orsaken var en trivial olycka … kött, senor och ben föll bort i stora mängder … det var många dödsfall.”1 Sedan dess har andra beskrivande termer använts för att karaktärisera NSTI, till exempel ”phagedaenic ulcer, phagedena gangrenous, gangrenous ulcer, maligna ulcer, putrid ulcer eller hospital gangrene. ”2 Termen gangrene används fortfarande, som i Fournier gangrene, som är nekros av perineum och scrotum.3
Epidemiologi
Risken för NSTI förblir överlag låg, med cirka 1 000 fall per år i USA. Detta antal kan dock öka, kanske på grund av större medvetenhet och erkännande av sjukdomstillståndet, ökad antibiotikaresistens eller ökad bakteriell virulensförmåga.4
Etiologi
NSTI klassificeras efter anatomisk plats (t.ex. Fourniergangrän), men de förekommer oftast i extremiteterna, perineum och genitalierna. Vanliga bakteriella orsaksorganismer är meticillinresistenta Staphylococcus aureus (MRSA), gramnegativa organismer och anaerobier samt streptokocker av grupp A (GAS).4
Klinisk presentation och diagnos
Den initiala presentationen av patienter med NSTI kan efterlikna symtom som är förknippade med cellulit, inklusive erytem, svullnad, feber, induration och ödem utanför det område där hudförändringar förekommer.4 Patienterna kan beskriva ömhet eller smärta som liknar den som uppstår vid en muskelbristning.5 Symtom som bör öka klinikerns misstanke om NSTI är bland annat smärta som är oproportionerlig i förhållande till undersökningsfynden (tidigt i sjukdomsförloppet), förekomst av bullae, hudekchymos som föregår hudnekros, gas i vävnaderna och kutana anestesier. Jämfört med patienter med en cellulitdiagnos pekar infektionsförloppet hos patienter med NSTI dessutom på ett mycket snabbare sjukdomsförlopp.4 Därför bör patienter som misstänks ha cellulit få diagnosen nekrotiserande fasciit utesluten.6 För att en infektion ska inträffa måste bakterierna komma in i blodomloppet, vanligen genom ett initierande sår (en brytning av epitel- eller slemhinneytan), t.ex. ett mindre skärsår eller skrapmärke, ett insektsbett, ett hudsår eller ett postoperativt sår; ibland kan dock sådana skador inte identifieras. Riskfaktorer för NSTI är bland annat nedsatt immunförsvar (aids, steroidbehandling), fetma, alkoholmissbruk, cancer, diabetes mellitus, perifer kärlsjukdom, njursjukdom, undernäring och andra kroniska tillstånd. Aktiv parenteral läkemedelsanvändning (intravenös eller subkutan injektion av illegala substanser) har också identifierats som en riskfaktor, särskilt i stadsmiljö.7
Guidelines Review
Infektionssällskapet IDSA (Infectious Diseases Society of America) 2014 års riktlinjer för diagnos och behandling av hud- och mjukdelsinfektioner innehåller information om hur man hanterar alla typer av hud- och mjukdelsinfektioner, från enkel cellulit till kutan mjältbrand hos friska individer och komprometterade patienter. Eftersom dessa infektioner förekommer i alla åldersgrupper innehåller riktlinjerna rekommendationer för både barn- och vuxenpatienter. En del av riktlinjerna innehåller information om NSTI. Specifika behandlingsrekommendationer ges baserat på ett betyg som anger styrkan i bevisningen för rekommendationen enligt IDSA/U.S. Public Health Service graderingssystem för betygsättning av rekommendationer i kliniska riktlinjer.6 Riktlinjerna ger svar på 24 kliniska frågor, inklusive två frågor som är relaterade till NSTI.
Den första NSTI-relaterade frågan som tas upp i riktlinjerna är: Vilken är den föredragna utvärderingen och behandlingen av nekrotiserande fasciit, inklusive Fournier-gangrän? Den första rekommendationen gäller snabb kirurgisk konsultation hos patienter med aggressiva infektioner med tecken på systemisk toxicitet eller om det finns oro för nekrotiserande fasciit eller gasgangrän.6 Detta följs av två rekommendationer som rör antibiotikabehandling. Den initiala antimikrobiella behandlingen bör vara bred så att den täcker både infektioner med en och flera organismer. Dessutom rekommenderas penicillin i kombination med klindamycin vid dokumenterad nekrotiserande fasciit orsakad av GAS. Alla tre rekommendationerna har bedömts som starka med bevis av låg kvalitet, vilket tyder på att de önskvärda effekterna klart överväger eventuella oönskade effekter. Efter rekommendationerna ges en evidensgenomgång, följt av en genomgång av de vanligaste kliniska dragen, mikrobiologiska orsakerna (monomikrobiella kontra polymikrobiella), diagnos och behandling.
Ett separat avsnitt i riktlinjerna fokuserar på hanteringen av clostridial NSTI enligt följande fråga: Vad är det lämpliga tillvägagångssättet för utvärdering och behandling av clostridiell gasgangrän eller myonekros? För det första bör man göra en brådskande kirurgisk undersökning av det misstänkta gasgangränområdet och avlägsna den inblandade vävnaden. Antibiotikabehandling med ett brett spektrum föreslås om det inte finns en definitiv mikrobiologisk orsak. Vid myonekros orsakad av clostridier föreslås penicillin i kombination med klindamycin. Slutligen rekommenderas inte hyperbar syrebehandling. Alla dessa förslag har en stark rekommendation och alla utom den kirurgiska rekommendationen har låg beviskvalitet (den kirurgiska rekommendationen har måttlig beviskvalitet). En genomgång av bevisen kring dessa rekommendationer avslutar avsnittet om NSTI.6
Förutom att NSTI skiljer sig från mindre allvarliga hudinfektioner genom den kliniska presentationen och andra systemiska manifestationer, kräver NSTI en annan strategi för behandling. Det finns många olika typer av NSTI, men antibiotikabehandlingen och det kirurgiska tillvägagångssättet är likartat för alla typer, och kirurgiskt ingrepp är det primära tillvägagångssättet när man förväntar sig en NSTI. De flesta patienter kommer att behöva flera besök på operationssalen (OR) tills debridering inte längre behövs.6
Läkemedelsbehandling
Det initiala antibiotikavalet bör omfatta agens med aktivitet mot ett brett spektrum av organismer, inklusive aerobier, MRSA och anaerobier (TABELL 1).6 Patientspecifika faktorer som tidigare antibiotikaexponering, samtidiga sjukdomstillstånd, organdysfunktion och allergier bör beaktas vid val av antibiotika. Liksom vid hantering av de flesta infektioner innefattar god antimikrobiell stewardship att optimera antibiotikabehandlingen till det smalaste spektrumet när en mikrobiologisk orsak har identifierats.
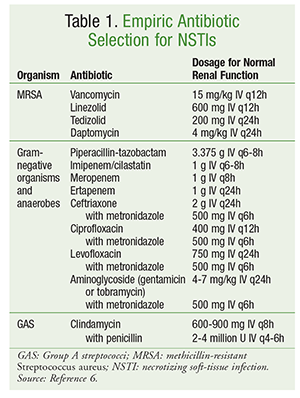
Den definitiva hanteringen av NSTI inbegriper en mängd olika antibiotiska medel. Vid polymikrobiella infektioner fortsätter ofta bredspektrumantibiotikabehandling. Vid infektioner orsakade av GAS bör både klindamycin och penicillin användas. Tillägget av klindamycin dämpar toxin- och cytokinproduktionen, och användningen av penicillin ger täckning i händelse av klindamycinresistens hos GAS. För infektioner orsakade av meticillinkänslig S aureus är användningen av nafcillin, oxacillin eller cefazolin att föredra. Clostridieinfektioner bör behandlas med klindamycin i kombination med penicillin. Antibiotikabehandlingen fortsätter vanligtvis tills ingen ytterligare debridering är nödvändig, patienten har visat klinisk förbättring och febern har varit frånvarande i 48 till 72 timmar.6
Sedan publiceringen av IDSA:s riktlinjer från 2014 har flera nya antibiotika godkänts för användning vid behandling av komplicerade infektioner i hud och mjuka vävnader. Dessa medel är tedizolid (Sivextro), oritavancin (Orbactiv) och dalbavancin (Dalvance).
Tedizolid är ett oxazolidinonantibiotikum som liknar linezolid. Det har tillförlitlig aktivitet mot MRSA och andra multiresistenta grampositiva organismer. Till skillnad från den två gånger dagliga doseringen av linezolid ges tedizolid i en enda daglig dos, antingen oralt eller intravenöst. Tedizolid kan ha gynnsammare biverknings- och läkemedelsinteraktionsprofiler jämfört med linezolid.8 Även om tedizolid har studerats vid behandling av akuta bakteriella hud- och hudstrukturinfektioner har det inte studerats vid NSTI.
Dalbavancin och oritavancin är lipoglykopeptider som är godkända för behandling av akuta bakteriella hud- och hudstrukturinfektioner. Dessa medel är unika genom att de har en lång halveringstid, vilket gör det möjligt att använda antingen en engångsdosregim eller en regim en gång i veckan. Dosen av dalbavancin måste minskas hos patienter med ett kreatininclearance <30 ml/minut. Oritavancin kräver inga dosjusteringar relaterade till organdysfunktion, men det ska inte användas till patienter som får heparin eftersom det förlänger koagulationstesterna på konstgjord väg. Oritavancin kan också öka effekterna av vitamin K-antagonister som warfarin.9 Båda medlen har bevisad effekt vid behandling av hud- och hudstrukturinfektioner, men de har inte utvärderats för användning vid nekrotiserande infektioner.
Adjunktiva terapier för NSTI inkluderar IV immunoglobulin (IVIG) och hyperbar syrebehandling. IVIG anses vara fördelaktigt på grund av möjlig neutralisering av de toxiner som produceras vid streptokockinfektioner. En minskning av dessa toxiner skulle potentiellt kunna minska en del av organsvikt, chock och vävnadsdestruktion som ofta ses vid NSTI.6 När IDSA:s riktlinjer publicerades (april 2014) rapporterade en observationsstudie och en prövning från Europa om vissa framgångar med användningen av IVIG vid streptokockinfektioner.6 Baserat på bristen på evidens som stödjer effekten rekommenderas dock inte användningen av IVIG för närvarande.
En nyare studie beskrev effektiviteten av klindamycin och IVIG mot invasiva GAS-infektioner.10 Åttiofyra patienter uppfyllde kriterierna för invasiv GAS-sjukdom, och IVIG användes hos 14 patienter, inklusive åtta med nekrotiserande fasciit. Mortaliteten var lägre hos patienter som behandlades med klindamycin och IVIG, men denna skillnad var inte signifikant. Även om det inte fanns någon statistisk skillnad i mortalitet när IVIG lades till klindamycin, föreslog författarna att det kan finnas en möjlig fördel hos vuxna med svårare sjukdom.10
Hyperbar syrebehandling (HBOT) har förespråkats för behandling av gasgangrän, men dess roll är kontroversiell.6 Laboratoriestudier har visat att syrerika vävnadstillstånd bidrar till att undertrycka tillväxten av Clostridium perfringens och öka värdets försvar mot främmande celler, men det saknas kriterier för att identifiera vilka patienter som kan gynnas och vilken tidpunkt som är lämplig för att påbörja behandlingen.6,11 Ingenting bör fördröja akut kirurgisk debridering och antibiotikaadministrering, eftersom båda är viktiga för att säkerställa överlevnad.6
Eftersom majoriteten av de publicerade studierna var små och underbemannade genomfördes en studie för att utvärdera data om användningen av HBOT från flera centra med HBOT-anläggningar.11 Under en treårsperiod såg 14 HBOT-anläggningar 1 583 fall av NSTI och tillhandahöll adjuvant HBOT i 117 fall. HBOT-gruppen hade ökade kostnader och en längre sjukhusvistelse än kontrollgruppen, men hade en betydligt lägre sjukhusdödlighet (5 % respektive 12 %; P <.05). När sjukdomens svårighetsgrad beaktades hade de svårast sjuka HBOT-patienterna signifikant lägre dödlighet och komplikationer, men det fanns inga skillnader i vistelsetid eller kostnader. En multivariat analys visade att patienter som inte fick HBOT hade större sannolikhet att dö under sjukhusvistelsen (oddskvot, 10,6; 95 % KI 5,2-25,1). Varje ökning av sjukdomens svårighetsgrad medförde en ökad risk för dödsfall.
Denna studie av 14 HBOT-anläggningar tycks visa på förbättrade resultat, särskilt för de sjukaste patienterna som läggs in direkt på ett center som har möjlighet att erbjuda denna behandling.11 Detta minskar dock inte kontroverserna kring användningen av HBOT, eftersom denna undersökning hade flera begränsningar. Studien genomfördes retrospektivt med hjälp av en administrativ databas vid akademiska medicinska centra. Dessutom kan vissa centra ha en tredje part som äger HBOT-anläggningen, vilket gör att resultaten är mindre generaliserbara för patienter vid dessa institutioner. En randomiserad, kontrollerad studie skulle vara till hjälp för att fastställa den slutliga nyttan av denna behandling.
Komplikationer
Den dödlighet som är förknippad med NSTI är så hög som 30 till 70 % hos patienter med GAS nekrotiserande fasciit i kombination med hypotoni och organsvikt.6 Eftersom behandlingen innebär flera besök på operationssalen rapporteras rutinmässigt stora sår och eventuella amputationer. Andra komplikationer, såsom rekonstruktiv kirurgi, sepsis, nosokomiala infektioner och förlängd intensivvårdstid på grund av utveckling av organsvikt i flera system, är frekventa komplikationer till NSTI.12
Information om långtidseffekter av NSTI samlades in genom djupintervjuer med 18 överlevande.12,13 Utredarna konstaterade att den rapporterade livskvaliteten påverkades avsevärt av den fysiska funktionen och fortsatt smärta. Man upptäckte också att effekten av upplevelsen på familje- och andra relationer var betydande. Flera överlevare beskrev långsiktiga psykologiska konsekvenser av sjukdomen, inklusive depression och posttraumatisk stress.
Slutsats
Sjukhusfarmaceuter är mycket väl lämpade för att hjälpa till med vården av patienter med NSTI, inklusive effektivisering av vården, främjande av antimikrobiell stewardship och förbättringar av de kliniska resultaten, kostnadsreducering, komplikationsminimering och återinskrivningar. Andra roller för farmaceuten är att identifiera idealiska patienter för de nya men dyrare terapeutiska medlen (t.ex. oritavancin) och att känna igen läkemedelsinteraktioner (t.ex. antikoagulantia) med dessa antibiotikaklasser.
1. Descamps V, Aitken J, Lee MG. Hippokrates om nekrotiserande fasciit. Lancet. 1994;344:556.
2. Loudon I. Necrotising fasciitis, hospital gangrene, and phagedena. Lancet. 1994;344:1416-1419.
3. Sarani B, Strong M, Pascual J, Schwab CW. Nekrotiserande fasciit: aktuella begrepp och litteraturgenomgång. J Am Coll Surg. 2009;208:279-288.
4. Hakkarainen TW, Kopari NM, Pham TN, Evans HL. Nekrotiserande mjukdelsinfektioner: genomgång och aktuella begrepp inom behandling, vårdsystem och resultat. Curr Probl Surg. 2014;51:344-362.
5. CDC. Nekrotiserande fasciit: en sällsynt sjukdom, särskilt för friska. www.cdc.gov/features/necrotizingfasciitis/. Accessed November 29, 2016.
6. Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the Infectious Diseases Society of America. Clin Infect Dis. 2014;59:147-159.
7. Bosshardt TL, Henderson VJ, Organ CH Jr. Necrotizing soft-tissue infections. Arch Surg. 1996;131:846-852.
8. Kisgen JJ, Mansour H, Unger NR, Childs LM. Tedizolid: ett nytt antimikrobiellt oxazolidinon. Am J Health Syst Pharm. 2014;71:621-633.
9. Roberts KD, Sulaiman RM, Rybak MJ. Dalbavancin och oritavancin: en innovativ strategi för behandling av grampositiva infektioner. Farmakoterapi. 2015;35:935-948.
10. Carapetis JR, Jacoby P, Carville K, et al. Effektivitet av klindamycin och intravenöst immunglobulin, och risk för sjukdom hos kontakter, vid invasiva streptokockinfektioner av grupp A. Clin Infect Dis. 2014;59:358-365.
11. Shaw JJ, Psoinos C, Ernhoff TA, et al. Not just full of hot air: Hyperbaric oxygen therapy increases survival in cases of necrotizing soft tissue infections. Surg Infect (Larchmt). 2014;15:328-335.
12. Hakkarainen TW, Burkette Ikebata N, Bulger E, Evans HL. Moving beyond survival as a measure of success: understanding the patient experience of necrotizing soft-tissue infections. J Surg Res. 2014;192:143-149.
13. Miller LG, Perdreau-Remington F, Rieg G, et al. Nekrotiserande fasciit orsakad av samhällsassocierad meticillinresistent Staphylococcus aureus i Los Angeles. New Engl J Med. 2005;352:1445-1453.