Nyhetsmeddelande
Måndag den 28 december 2020
Den av NIH och BARDA finansierade studien kommer att omfatta upp till 30 000 frivilliga.
Personer som är 18 år och äldre och som är intresserade av att delta i denna studie kan besöka coronaviruspreventionnetwork.org, ClinicalTrials.gov och söka identifieringskoden NCT04611802, eller Novavax.com/PREVENT-19 för mer information. Kontakta inte NIAID:s medietelefonnummer eller e-post för att anmäla dig till den här studien.
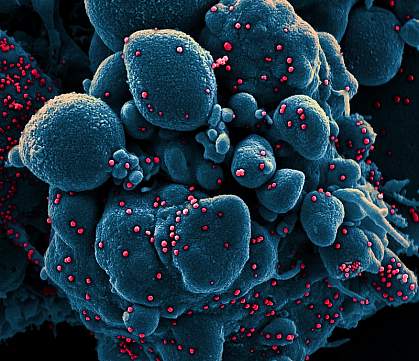 Kolorerad skanningselektronmikroskopisk bild av en apoptotisk cell (blå) som är infekterad med viruspartiklar av SARS-COV-2 (röd), isolerad från ett patientprov.NIAID
Kolorerad skanningselektronmikroskopisk bild av en apoptotisk cell (blå) som är infekterad med viruspartiklar av SARS-COV-2 (röd), isolerad från ett patientprov.NIAID Fas 3-studien av ett annat undersökande vaccin mot coronavirus sjukdom 2019 (COVID-19) har börjat rekrytera vuxna frivilliga. Den randomiserade, placebokontrollerade studien kommer att rekrytera cirka 30 000 personer på cirka 115 platser i USA och Mexiko. Den kommer att utvärdera säkerheten och effekten av NVX-CoV2373, en vaccinkandidat som utvecklats av Novavax, Inc. i Gaithersburg, Maryland. Novavax leder studien i egenskap av regulatorisk sponsor. National Institute of Allergy and Infectious Diseases (NIAID), en del av National Institutes of Health, och Biomedical Advanced Research and Development Authority (BARDA), en del av U.S. Department of Health and Human Services Office of the Assistant Secretary for Preparedness and Response, finansierar försöket.
”Det har krävts extraordinära insatser från regeringens, den akademiska världens, näringslivets och samhällets sida för att ta itu med den aldrig tidigare skådade hälsokrisen COVID-19”, säger NIAID-chefen Anthony S. Fauci, M.D. ”Lanseringen av denna studie – den femte undersökande COVID-19-vaccinkandidaten som testas i en fas 3-studie i USA – visar vår beslutsamhet att få slut på pandemin genom att utveckla flera säkra och effektiva vacciner.”
Studien genomförs i samarbete med Operation Warp Speed (OWS), ett samarbete mellan flera myndigheter som övervakas av HHS och försvarsdepartementet och som syftar till att påskynda utvecklingen, tillverkningen och distributionen av medicinska motåtgärder för COVID-19. Några av de amerikanska försöksplatser som deltar ingår i det NIAID-stödda COVID-19 Prevention Network (CoVPN). CoVPN omfattar befintliga NIAID-stödda kliniska forskningsnätverk med expertis inom infektionssjukdomar och har utformats för snabb och grundlig utvärdering av vaccinkandidater och monoklonala antikroppar för att förebygga COVID-19.
Frivilliga kommer att ombes ge ett informerat samtycke innan de deltar i studien. De kommer att grupperas i två kohorter: individer mellan 18 och 64 år och de som är 65 år och äldre, med målet att rekrytera minst 25 % av alla frivilliga som är 65 år eller äldre. Försöksorganisatörerna betonar också rekrytering av personer som löper större risk att drabbas av allvarlig COVID-19-sjukdom, bland annat personer som är svarta (inklusive afroamerikaner), infödda amerikaner, latinamerikaner eller latinamerikaner och personer som har underliggande hälsoproblem som fetma, kronisk njursjukdom eller diabetes.
”Vi har kommit så här långt, så här snabbt, men vi måste ta oss till mållinjen”, sade NIH:s direktör Francis S. Collins, M.D., Det kommer att kräva flera vacciner med olika tillvägagångssätt för att se till att alla skyddas säkert och effektivt mot denna dödliga sjukdom.”
Efter att ha lämnat ett baslinjeprov från nasofarynx och ett blodprov kommer deltagarna att slumpmässigt tilldelas en intramuskulär injektion av antingen det undersökta vaccinet eller ett placebo med saltlösning. Randomiseringen kommer att ske i ett 2:1-förhållande med två frivilliga som får det undersökande vaccinet för var och en som får placebo. Eftersom studien är blindad kommer varken utredare eller deltagare att veta vem som får kandidatvaccinet. En andra injektion kommer att ges 21 dagar efter den första.
Deltagarna kommer att följas noga för att upptäcka eventuella biverkningar av vaccinet och kommer att uppmanas att lämna blodprover vid bestämda tidpunkter efter varje injektion och under de följande två åren. Forskarna kommer att analysera blodproverna för att upptäcka och kvantifiera immunsvar mot SARS-CoV-2, det virus som orsakar COVID-19. Speciella tester kommer att användas för att skilja mellan immunitet till följd av naturlig infektion och vaccininducerad immunitet. Prövningens primära endpoint är att fastställa om NVX-CoV2373 kan förhindra symtomatisk COVID-19-sjukdom sju eller fler dagar efter den andra injektionen i förhållande till placebo.
Novavax undersökningsvaccin, NVX-CoV2373, tillverkas av en stabiliserad form av coronavirusets spikprotein med hjälp av företagets teknik för rekombinanta proteinnanopartiklar. De renade proteinantigenerna i vaccinet kan inte replikera och kan inte orsaka COVID-19. Vaccinet innehåller också en egenutvecklad adjuvant, MatrixM™. Adjuvans är tillsatser som förstärker önskade immunsystemresponser på vaccinet. NVX-CoV2373 administreras i flytande form och kan lagras, hanteras och distribueras vid temperaturer över fryspunkten (35° till 46°F). En enda vaccindos innehåller 5 mikrogram (mcg) protein och 50 mcg adjuvans.
I djurförsök producerade NVX-CoV2373-vaccinering antikroppar som blockerade coronavirusets spikprotein från att binda sig till de receptorer på cellytan som viruset riktar in sig på, vilket förhindrade virusinfektion. I resultaten av en klinisk fas 1-studie som publicerades i New England Journal of Medicine tolererades NVX-CoV2373 i allmänhet väl och framkallade högre nivåer av antikroppar än de som sågs i blodprover från personer som hade återhämtat sig från kliniskt signifikant COVID-19. NVX-CoV2373 utvärderas också i en fas 2b-studie i Sydafrika, som nu är fulltecknad med 4 422 frivilliga, och data från en fortsatt fas 1/2-studie i USA och Australien väntas så tidigt som första kvartalet 2021. Novavax avslutade också nyligen rekryteringen av mer än 15 000 frivilliga i en fas 3-studie av kandidatvaccinet i Storbritannien, där man också testar två injektioner av 5 mcg protein och 50 mcg Matrix-M adjuvans som administreras med 21 dagars mellanrum.
En oberoende data- och säkerhetsövervakningsnämnd (Data and Safety Monitoring Board, DSMB) kommer att utöva tillsyn för att garantera ett säkert och etiskt genomförande av studien. Alla kliniska fas 3-studier av kandidatvaccin som stöds genom OWS övervakas av en gemensam DSMB som utvecklats i samråd med initiativet NIH Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV).
Vuxna som är intresserade av att delta i den här studien kan gå in på Coronaviruspreventionnetwork.org, Novavax.com/PREVENT-19 eller ClinicalTrials.gov och söka identifieraren NCT04611802.
Om COVID-19 Prevention Network: COVID-19 Prevention Network (CoVPN) bildades av National Institute of Allergy and Infectious Diseases (NIAID) vid U.S. National Institutes of Health för att reagera på den globala pandemin. Genom CoVPN utnyttjar NIAID expertisen om infektionssjukdomar i sina befintliga forskningsnätverk och globala partner för att tillgodose det akuta behovet av vacciner och antikroppar mot SARS-CoV-2. CoVPN kommer att arbeta för att utveckla och genomföra studier för att säkerställa en snabb och grundlig utvärdering av vacciner och antikroppar för att förebygga COVID-19. CoVPN har sitt huvudkontor vid Fred Hutchinson Cancer Research Center. Mer information om CoVPN finns på coronaviruspreventionnetwork.org.
Om HHS, ASPR och BARDA: HHS arbetar för att förbättra och skydda alla amerikaners hälsa och välbefinnande genom att tillhandahålla effektiva hälso- och sjukvårdstjänster och främja framsteg inom medicin, folkhälsa och sociala tjänster. ASPR:s uppdrag är att rädda liv och skydda amerikanerna från 2000-talets hot mot hälsosäkerheten. Inom ASPR investerar BARDA i innovation, avancerad forskning och utveckling, förvärv och tillverkning av medicinska motåtgärder – vacciner, läkemedel, terapier, diagnostiska verktyg och icke-farmaceutiska produkter som behövs för att bekämpa hot mot hälsosäkerheten. Hittills har produkter som fått stöd från BARDA fått 55 FDA-godkännanden, licenser eller godkännanden. Om du vill veta mer om det federala stödet till den landsomfattande COVID-19-insatsen kan du besöka www.coronavirus.gov.
Om Operation Warp Speed: OWS är ett partnerskap mellan delar av hälso- och sjukvårdsdepartementet och försvarsdepartementet, som engagerar sig i privata företag och andra federala organ och samordnar befintliga HHS-omfattande insatser för att påskynda utvecklingen, tillverkningen och distributionen av COVID-19-vacciner, terapier och diagnostik.
Om National Institute of Allergy and Infectious Diseases: OWS är ett partnerskap mellan olika delar av hälso- och sjukvårdsdepartementet och försvarsdepartementet: NIAID bedriver och stöder forskning – vid NIH, i hela USA och över hela världen – för att studera orsakerna till smittsamma och immunmedierade sjukdomar och för att utveckla bättre metoder för att förebygga, diagnostisera och behandla dessa sjukdomar. Nyhetsmeddelanden, faktablad och annat NIAID-relaterat material finns på NIAID:s webbplats.
Om National Institutes of Health (NIH):NIH, landets organ för medicinsk forskning, omfattar 27 institut och centra och är en del av USA:s Department of Health and Human Services. NIH är det främsta federala organet som bedriver och stöder grundläggande, klinisk och translationell medicinsk forskning och undersöker orsaker, behandlingar och botemedel för både vanliga och sällsynta sjukdomar. Mer information om NIH och dess program finns på www.nih.gov.
NIH…Turning Discovery Into Health®
####