Comunicat de presă
Luni, 28 decembrie 2020
Studiul finanțat de NIH și BARDA va înrola până la 30.000 de voluntari.
Persoanele cu vârsta de 18 ani și peste care sunt interesate să participe la acest studiu pot vizita coronaviruspreventionnetwork.org, ClinicalTrials.gov și căutați identificatorul NCT04611802, sau Novavax.com/PREVENT-19 pentru detalii. Vă rugăm să nu contactați numărul de telefon media al NIAID sau e-mailul pentru a vă înscrie în acest studiu.
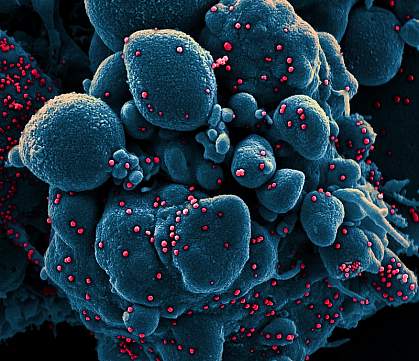 Micrografie electronică de scanare colorată a unei celule apoptotice (albastru) infectate cu particule de virus SARS-COV-2 (roșu), izolate dintr-o probă de pacient.NIAID
Micrografie electronică de scanare colorată a unei celule apoptotice (albastru) infectate cu particule de virus SARS-COV-2 (roșu), izolate dintr-o probă de pacient.NIAID Studiul de fază 3 al unui alt vaccin experimental împotriva bolii coronavirus 2019 (COVID-19) a început să înroleze voluntari adulți. Studiul randomizat, controlat cu placebo, va înrola aproximativ 30.000 de persoane în aproximativ 115 locații din Statele Unite și Mexic. Acesta va evalua siguranța și eficacitatea NVX-CoV2373, un vaccin candidat dezvoltat de Novavax, Inc. din Gaithersburg, Maryland. Novavax conduce studiul în calitate de sponsor de reglementare. Institutul Național de Alergii și Boli Infecțioase (National Institute of Allergy and Infectious Diseases – NIAID), care face parte din Institutele Naționale de Sănătate, și Autoritatea pentru Cercetare și Dezvoltare Biomedicală Avansată (Biomedical Advanced Research and Development Authority – BARDA), care face parte din Departamentul de Sănătate și Servicii U.S. Office of the Assistant Secretary for Preparedness and Response, finanțează studiul.
„Abordarea crizei de sănătate fără precedent a COVID-19 a necesitat eforturi extraordinare din partea guvernului, a mediului academic, a industriei și a comunității”, a declarat directorul NIAID, Anthony S. Fauci, M.D. „Lansarea acestui studiu – al cincilea vaccin experimental candidat pentru COVID-19 care va fi testat în cadrul unui studiu de fază 3 în Statele Unite – demonstrează hotărârea noastră de a pune capăt pandemiei prin dezvoltarea mai multor vaccinuri sigure și eficiente.”
Studiul se desfășoară în colaborare cu Operation Warp Speed (OWS), o colaborare între mai multe agenții, supervizată de HHS și de Departamentul Apărării, care are ca scop accelerarea dezvoltării, fabricării și distribuirii de contramăsuri medicale pentru COVID-19. Unele dintre centrele de testare din SUA care participă fac parte din Rețeaua de prevenire a COVID-19 (CoVPN), sprijinită de NIAID. CoVPN include rețelele existente de cercetare clinică susținute de NIAID cu expertiză în domeniul bolilor infecțioase și a fost concepută pentru evaluarea rapidă și amănunțită a vaccinurilor candidate și a anticorpilor monoclonali pentru prevenirea COVID-19.
Voluntarii vor trebui să își dea consimțământul în cunoștință de cauză înainte de participarea la studiu. Aceștia vor fi grupați în două cohorte: persoanele cu vârste cuprinse între 18 și 64 de ani și cele cu vârste de 65 de ani și peste, cu scopul de a înrola cel puțin 25% din toți voluntarii care au 65 de ani sau mai mult. De asemenea, organizatorii trialului pun accentul pe recrutarea persoanelor care prezintă un risc mai mare de îmbolnăvire severă cu COVID-19, inclusiv a celor de culoare (inclusiv afro-americani), nativi americani sau de etnie latină sau hispanică, precum și a persoanelor care au condiții de sănătate subiacente, cum ar fi obezitatea, boala cronică de rinichi sau diabetul.
„Am ajuns atât de departe, atât de repede, dar trebuie să ajungem la linia de sosire”, a declarat directorul NIH, Francis S. Collins, M.D., Ph.D. „Acest lucru va necesita mai multe vaccinuri care folosesc abordări diferite pentru a ne asigura că toată lumea este protejată în siguranță și în mod eficient de această boală mortală.”
După ce vor furniza o probă nazofaringiană și de sânge de referință, participanții vor fi repartizați aleatoriu pentru a primi o injecție intramusculară fie a vaccinului experimental, fie a unui placebo salin. Randomizarea se va face într-un raport 2:1, cu doi voluntari care primesc vaccinul experimental pentru fiecare voluntar care primește placebo. Deoarece studiul este orbit, nici investigatorii, nici participanții nu vor ști cine primește vaccinul candidat. O a doua injecție va fi administrată la 21 de zile după prima.
Participanții vor fi urmăriți îndeaproape pentru potențiale efecte secundare ale vaccinului și li se va cere să furnizeze probe de sânge la anumite intervale de timp după fiecare injecție și pe parcursul următorilor doi ani. Oamenii de știință vor analiza probele de sânge pentru a detecta și cuantifica răspunsurile imune la SARS-CoV-2, virusul care provoacă COVID-19. De menționat că se vor folosi teste specializate pentru a face distincția între imunitatea ca rezultat al infecției naturale și imunitatea indusă de vaccin. Obiectivul principal al studiului este de a determina dacă NVX-CoV2373 poate preveni boala COVID-19 simptomatică la șapte sau mai multe zile după a doua injecție în raport cu placebo.
Vaccinul experimental al Novavax, NVX-CoV2373, este realizat dintr-o formă stabilizată a proteinei spike a coronavirusului, folosind tehnologia nanoparticulelor de proteine recombinate a companiei. Antigenele proteice purificate din vaccin nu se pot replica și nu pot provoca COVID-19. Vaccinul conține, de asemenea, un adjuvant brevetat, MatrixM™. Adjuvanții sunt aditivi care sporesc răspunsurile dorite ale sistemului imunitar la vaccin. NVX-CoV2373 se administrează sub formă lichidă și poate fi depozitat, manipulat și distribuit la temperaturi peste zero grade Celsius (35° – 46° F). O singură doză de vaccin conține 5 micrograme (mcg) de proteină și 50 mcg de adjuvant.
În testele pe animale, vaccinarea cu NVX-CoV2373 a produs anticorpi care au blocat legarea proteinei spike a coronavirusului de receptorii de la suprafața celulară vizați de virus, împiedicând infecția virală. În rezultatele unui studiu clinic de fază 1 publicat în New England Journal of Medicine, NVX-CoV2373 a fost, în general, bine tolerat și a determinat niveluri mai ridicate de anticorpi decât cele observate în probele de sânge prelevate de la persoane care s-au vindecat de COVID-19 semnificative din punct de vedere clinic. NVX-CoV2373 este, de asemenea, în curs de evaluare într-un studiu de fază 2b în Africa de Sud, în prezent complet înscris cu 4.422 de voluntari, iar datele dintr-un studiu de continuare de fază 1/2 în Statele Unite și Australia sunt așteptate încă din primul trimestru al anului 2021. De asemenea, Novavax a finalizat recent înscrierea a peste 15.000 de voluntari într-un studiu de fază 3 al vaccinului candidat în Regatul Unit, care testează, de asemenea, două injecții de 5 mcg de proteină și 50 mcg de adjuvant Matrix-M administrate la 21 de zile distanță.
Un comitet independent de monitorizare a datelor și a siguranței (DSMB) va asigura supravegherea pentru a garanta desfășurarea sigură și etică a studiului. Toate studiile clinice de fază 3 ale vaccinurilor candidate susținute prin OWS sunt supravegheate de un DSMB comun dezvoltat în consultare cu inițiativa NIH Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV).
Adulții care sunt interesați să se alăture acestui studiu pot vizita Coronaviruspreventionnetwork.org, Novavax.com/PREVENT-19 sau ClinicalTrials.gov și să caute identificatorul NCT04611802.
Despre Rețeaua de prevenire COVID-19: Rețeaua de prevenire COVID-19 (CoVPN) a fost formată de către Institutul Național de Alergii și Boli Infecțioase (NIAID) din cadrul Institutelor Naționale de Sănătate din SUA pentru a răspunde pandemiei globale. Prin intermediul CoVPN, NIAID valorifică expertiza în domeniul bolilor infecțioase a rețelelor sale de cercetare existente și a partenerilor globali pentru a răspunde nevoii urgente de vaccinuri și anticorpi împotriva SARS-CoV-2. CoVPN va lucra la dezvoltarea și desfășurarea de studii pentru a asigura o evaluare rapidă și completă a vaccinurilor și anticorpilor pentru prevenirea COVID-19. CoVPN își are sediul la Fred Hutchinson Cancer Research Center. Pentru mai multe informații despre CoVPN, vizitați: coronaviruspreventionnetwork.org.
Despre HHS, ASPR și BARDA: HHS se străduiește să îmbunătățească și să protejeze sănătatea și bunăstarea tuturor americanilor, asigurând servicii de sănătate și servicii umane eficiente și promovând progresele în medicină, sănătate publică și servicii sociale. Misiunea ASPR este de a salva vieți și de a proteja americanii de amenințările la adresa securității sanitare din secolul XXI. În cadrul ASPR, BARDA investește în inovarea, cercetarea și dezvoltarea avansată, achiziția și fabricarea de contramăsuri medicale – vaccinuri, medicamente, produse terapeutice, instrumente de diagnosticare și produse non-farmaceutice necesare pentru a combate amenințările la adresa securității sanitare. Până în prezent, produsele sprijinite de BARDA au obținut 55 de aprobări, licențe sau autorizări din partea FDA. Pentru a afla mai multe despre sprijinul federal pentru răspunsul la nivel național la COVID-19, vizitați www.coronavirus.gov.
Despre Operațiunea Warp Speed: OWS este un parteneriat între componentele Departamentului Sănătății și Serviciilor Umane și ale Departamentului Apărării, care se angajează cu firme private și alte agenții federale și se coordonează între eforturile existente la nivelul HHS pentru a accelera dezvoltarea, fabricarea și distribuția de vaccinuri, produse terapeutice și diagnostice COVID-19.
Despre Institutul Național de Alergii și Boli Infecțioase: NIAID desfășoară și sprijină cercetarea – la NIH, în Statele Unite și în întreaga lume – pentru a studia cauzele bolilor infecțioase și imunomediate și pentru a dezvolta mijloace mai bune de prevenire, diagnosticare și tratare a acestor boli. Comunicate de presă, fișe informative și alte materiale legate de NIAID sunt disponibile pe site-ul web al NIAID.
Despre National Institutes of Health (NIH):NIH, agenția națională de cercetare medicală, include 27 de institute și centre și este o componentă a Departamentului de Sănătate și Servicii Umane al SUA. NIH este principala agenție federală care efectuează și sprijină cercetarea medicală fundamentală, clinică și translațională și investighează cauzele, tratamentele și leacurile atât pentru bolile comune, cât și pentru cele rare. Pentru mai multe informații despre NIH și programele sale, vizitați www.nih.gov.
NIH…Turning Discovery Into Health®
###