Neprilizina a devenit un punct de interes în cardiologie, datorită beneficiilor impresionante ale combinației dintre inhibarea neprilizinei și blocarea receptorilor de angiotensină demonstrate în recentul studiu PARADIGM-HF, care a testat LCZ696 (cunoscut în prezent sub denumirea de sacubitril/valsartan și comercializat de Novartis sub numele de Entresto) pentru tratarea insuficienței cardiace sistolice cu fracție de ejecție redusă (HFrEF).1 Cu toate acestea, neprilizina EC 3.4.24.11 (cunoscută, de asemenea, sub numele de endopeptidază neutră, endoprotează 24.11, NEP, antigenul comun al leucemiei acute limfoblastice, antigenul de diferențiere a grupării antigenelor neutrofile 10, metaloendopeptidaza membranară EC 3.4.24.11 și encefalinaza) este o enzimă foarte versatilă, care a revenit în centrul atenției, după o carieră plină de evenimente de > 40 de ani.2
În sistemul cardiovascular, neprilizina scindează numeroase peptide vasoactive. Unele dintre aceste peptide au efecte vasodilatatoare (inclusiv peptidele natriuretice, adrenomedullina și bradikinina), iar altele au efecte vasoconstrictoare (angiotensina I și II și endotelina-1, printre altele). Cu toate acestea, neprilizina prezintă afinități relative diferite între diferiți substraturi; afinitatea sa cea mai mare este pentru peptida natriuretică atrială, peptida natriuretică de tip C și angiotensinele I și II; afinitatea sa cea mai mică este pentru peptida natriuretică de tip B (BNP), endotelina-1 și bradikinina.3
De zeci de ani, neprilizina a fost o bioțintă importantă. Academia și industria și-au combinat eforturile active pentru a căuta inhibitori de neprilizină (NEPI) care ar putea fi utili în practica clinică. Inițial, la sfârșitul anilor 1980 și începutul anilor 1990, a fost testată monoterapia cu NEPI. Candoxatrilul a arătat efecte preliminare promițătoare asupra parametrilor hemodinamici. Cu toate acestea, un alt NEPI, ecadotrilul, a dus la o mortalitate mai mare, fără dovezi de eficacitate clinică în comparație cu placebo la pacienții cu insuficiență cardiacă.4,5 În consecință, dezvoltarea monoterapiei cu NEPI pentru insuficiența cardiacă a fost întreruptă. Ulterior, unele studii au arătat dovezi de activare concomitentă a sistemului renină-angiotensină-aldosteron, împreună cu creșterea bioactivității peptidei natriuretice. Aceste constatări au inspirat dezvoltarea și testarea agenților care au combinat NEPI și activitatea de inhibare a enzimei de conversie a angiotensinei (IECA), ceea ce a dus la medicamentele cunoscute sub numele de inhibitori de vasopeptidază. Au fost dezvoltați mai mulți inhibitori de vasopeptidază, inclusiv omapatrilat, fasidotril, sampatrilat și mixanpril. După numeroase studii, domeniul a fost extrem de dezamăgit să constate că omapatrilatul a provocat un număr tot mai mare de episoade de angioedem relevante din punct de vedere clinic.6 După mai mult de un deceniu de rătăcire în deșert, a fost dezvoltat un nou concept, combinația dintre NEPI și blocantele receptorilor de angiotensină II (BRA), care a dus la o nouă clasă de medicamente numite inhibitori de neprilizină ai receptorilor de angiotensină. Sacubitril/valsartan este un inhibitor de neprilizină al receptorilor de angiotensină din prima clasă, care a prezentat rezultate mai bune decât se aștepta în studiul PARADIGM-HF1 (figura).
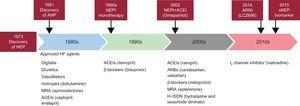
Schema de evidențiere istorică a neprilizinei. IECA, inhibitor al enzimei de conversie a angiotensinei; ANP, peptidă natriuretică atrială; ARB, blocant al receptorilor de angiotensină II; ARNI, inhibitor al neprilizinei receptorilor de angiotensină; IC, insuficiență cardiacă; ARM, antagonist al receptorilor mineralocorticoizi; NEP, neprilizină; NEPI, inhibitor de neprilizină; sNEP, neprilizină solubilă.
PARADIGM-HF a fost un studiu multinațional, randomizat, dublu-orb, cu 8442 pacienți. Scopul a fost de a compara sacubitril/valsartan cu enalaprilul la pacienții adulți cu insuficiență cardiacă cronică (New York Heart Association clasa II-IV) și fracție de ejecție ventriculară stângă redusă (FEVS ≤ 40%, modificată ulterior la ≤ 35%), în plus față de alte terapii pentru insuficiență cardiacă.1 Criteriul principal de evaluare a fost criteriul compozit de deces cardiovascular sau spitalizare pentru insuficiență cardiacă. Înainte de participarea la studiu, pacienții au fost tratați cu terapia standard de îngrijire, care a inclus ACEI/ARB (> 99%), beta-blocante (94%), antagoniști mineralocorticoizi (58%) și diuretice (82%). Durata mediană de urmărire a fost de 27 de luni, iar pacienții au fost tratați timp de până la 4,3 ani.
Pacienților li s-a cerut să întrerupă tratamentul ACEI sau ARB existent și să intre într-o perioadă secvențială, cu un singur orb, de rodaj. În timpul perioadei de rodaj, aceștia au primit tratament cu enalapril 10 mg de două ori pe zi, urmat de un tratament cu un singur orb cu sacubitril/valsartan 100 mg de două ori pe zi, care a fost crescut la 200 mg de două ori pe zi. Apoi au fost repartizați aleatoriu în perioada dublu-orb a studiului. În această perioadă, au primit fie sacubitril/valsartan 200mg, fie enalapril 10mg, de două ori pe zi. Vârsta medie a populației studiate a fost de 64 de ani, iar 19% aveau 75 de ani sau mai mult. La randomizare, 70% dintre pacienți erau de clasa II NYHA, 24% erau de clasa III și 0,7% erau de clasa IV. FEVS medie a fost de 29% și au existat 963 (11,4%) de pacienți cu o FEVS inițială > 35% și ≤ 40%. Studiul a fost încheiat prematur, din cauza reducerilor copleșitoare ale deceselor de cauză cardiovasculară și a reducerii punctului final primar compus (deces cardiovascular sau spitalizare secundară insuficienței cardiace). Studiul PARADIGM-HF este denumit, de asemenea, studiul 20%, datorită reducerilor relative omogene de ∼20% ale tuturor parametrilor finali studiați, inclusiv parametrul final primar compozit de deces cardiovascular, moarte cardiacă subită și spitalizare pentru insuficiență cardiacă (tabelul 1).
Studiul PARADIGM-HF: Efectele tratamentului asupra punctului final compozit primar, a componentelor sale și a mortalității de toate cauzele, Over a Median Follow-up of 27 Months
| Endpoints | Hazard ratio (95%CI) | Reducere relativă a riscului | P |
|---|---|---|---|
| Criteriul principal de evaluare compozit de deces CV și spitalizări din cauza insuficienței cardiace | 0.80 (0,73-0,87) | 20% | .0000002 |
| Componente individuale ale parametrului final compozit primar | |||
| Decesul CV | 0,80 (0,71-0.89) | 20% | .00004 |
| Prima spitalizare pentru insuficiență cardiacă | 0,79 (0,71-0,89) | 21% | .00004 |
| Secondary endpoint | |||
| Mortalitate de toate cauzele | 0,84 (0,76-0,93) | 16% | .0005 |
95%CI, interval de încredere de 95%; CV, legat de afecțiuni cardiovasculare.
Deși sacubitrilul/valsartan s-a dovedit a fi foarte promițător, există provocări și probleme nerezolvate care merită studii suplimentare și clarificări suplimentare (tabelul 2). Unele dintre aceste probleme au fost ridicate și discutate în raportul de evaluare al Agenției Europene pentru Medicamente privind Entresto.7
Rezumat al problemelor de siguranță pentru Sacubitril/Valsartan
| Riscuri importante identificate | Hipotensiune arterială Deteriorare renală Hiperkaliemie Angioedem |
| Riscuri potențiale importante | Hepatotoxicitate Deteriorare cognitivă Medicament cu statină .interacțiune medicamentoasă Trombocitopenie Neutropenie |
| Informații care lipsesc | Pacienți pediatrici cu IC Pacienți cu insuficiență renală severă Pacienți cu insuficiență renală severă Lung-date pe termen lung privind utilizarea sacubitrilului/valsartanului în IC Efecte la pacienții cu IC naivi la ACEI/ARB |
ACEI, inhibitor al enzimei de conversie a angiotensinei; ARB, blocant al receptorilor de angiotensină II; IC, insuficiență cardiacă.
Modificat din Raportul de evaluare al Agenției Europene pentru Medicamente.7
În primul rând, atunci când pacienții se confruntă cu probleme de tolerabilitate (de exemplu, tensiune arterială sistolică ≤ 95 mmHg, hipotensiune arterială simptomatică, hiperkaliemie, disfuncție renală), recomandările actuale sunt de a ajusta medicamentele concomitente și/sau de a micșora dozajul sau de a întrerupe temporar sacubitril/valsartan. De fapt, Agenția Europeană a Medicamentului recomandă ca tratamentul să nu fie inițiat la pacienții cu niveluri serice de potasiu > 5,4 mmol/L sau cu tensiune arterială sistolică
mmHg.
În al doilea rând, datele sunt limitate pentru pacienții care iau în prezent doze mici sau nu iau doze mici de IECA sau BRA. Prin urmare, recomandările actuale pentru acești pacienți sunt de a începe cu o doză de 50 mg de două ori pe zi și de a titra doza lent (dublarea la fiecare 3-4 săptămâni).
În al treilea rând, sacubitrilul/valsartanul nu trebuie să fie administrat în asociere cu un IECA sau un BRA. Atunci când este utilizat concomitent cu un IECA, există un risc potențial ridicat de angioedem. În consecință, sacubitril/valsartan nu trebuie inițiat timp de cel puțin 36 de ore după întreruperea tratamentului cu IECA.
În al patrulea rând, nu este necesară ajustarea dozei la pacienții cu insuficiență renală ușoară (rata de filtrare glomerulară estimată 60-90mL/min/1,73 m2). Cu toate acestea, o doză inițială de 50 mg de două ori pe zi trebuie luată în considerare la pacienții cu insuficiență renală moderată (rata estimată de filtrare glomerulară 30-60mL/min/1,73 m2). Nu există date privind pacienții cu insuficiență renală în stadiu terminal, dar utilizarea sacubitril/valsartan nu este recomandată pentru acești pacienți.
În al cincilea rând, trebuie manifestată prudență la inițierea sacubitril/valsartan la pacienții cu clasificare funcțională NYHA IV, din cauza experienței clinice limitate la această populație.
În al șaselea rând, BNP nu este un biomarker adecvat al insuficienței cardiace la pacienții tratați cu sacubitril/valsartan, deoarece este un substrat al neprilizinei. Se recomandă trecerea la NT-proBNP ca biomarker al peptidei natriuretice.
În al șaptelea rând, un risc teoretic asociat cu inhibarea neprilizinei este legat de acumularea substratului neprilizinei, amiloid-β, în creier.8 În studiul PARADIGM-HF nu a fost raportată o incidență crescută a evenimentelor adverse legate de cogniție sau demență. Cu toate acestea, este posibil ca aceste efecte să nu fi fost detectate până în prezent, deoarece este posibil ca dezvoltarea demenței să dureze mai mult timp decât perioada actuală de observare a participanților la studiu. De asemenea, nu era de așteptat ca subiecții cu demență ușoară să participe. Cu toate acestea, studiul PARAGON-HF de fază III în curs de desfășurare PARAGON-HF a implementat o evaluare a funcției cognitive.
În al optulea rând, coadministrarea de sacubitril/valsartan și atorvastatină a crescut Cmax a atorvastatinei și a metaboliților acesteia de până la 2 ori. Nu au existat creșteri semnificative ale evenimentelor adverse potențiale legate de statine la pacienții care au primit atât sacubitril/valsartan, cât și statine în studiul PARADIGM-HF. Cu toate acestea, analizele ulterioare au arătat că dozele mai mari de statine au fost asociate cu mai multe evenimente adverse, atunci când au fost combinate fie cu sacubitril/valsartan, fie cu enalapril. Cu toate acestea, modelele au fost diferite, în funcție de statina specifică administrată. În așteptarea rezultatelor unor studii suplimentare, s-a recomandat prudență pentru această combinație de medicamente.7
Ensamblul PARADIGM-HF se concentrează pe insuficiența cardiacă cronică cu FEVS limitată. Astfel, se pune întrebarea: Ce se întâmplă cu ceilalți 50% dintre pacienții cu insuficiență cardiacă, dar cu fracție de ejecție păstrată, cunoscuți și sub numele de pacienți cu HFpEF? În prezent, există o lipsă de studii clinice privind HFpEF care să demonstreze beneficii terapeutice cu agenți utilizați în mod obișnuit la pacienții cu fracție de ejecție redusă. În consecință, terapiile pentru HFpEF sunt direcționate către gestionarea simptomelor și a factorilor de risc cardiovascular. Cu toate acestea, în rândul pacienților cu HFpEF, sacubitril/valsartan a demonstrat rezultate promițătoare în ceea ce privește siguranța și eficacitatea într-un studiu de fază 2. Studiul PARAMOUNT a fost un studiu randomizat, dublu-orb, cu grupuri paralele, controlat activ, care a comparat sacubitril/valsartan cu valsartan singur.9 Criteriul principal de evaluare a fost o modificare față de valoarea inițială a NT-proBNP la 12 săptămâni. Grupurile au avut caracteristici inițiale similare. Majoritatea pacienților erau în vârstă, de sex feminin, supraponderali și clasificați în clasa II NYHA. O reducere mai mare a NT-proBNP a fost detectată la săptămâna 4 în grupul sacubitril/valsartan în comparație cu grupul valsartan, dar nu a atins semnificația (P = 0,063). La 12 săptămâni, NT-proBNP a fost redus semnificativ în grupul sacubitril/valsartan în comparație cu valsartan (P = 0,005). Constatările din PARAMOUNT au sugerat că sacubitril/valsartan ar putea avea efecte favorabile la pacienții cu HFpEF. Investigarea suplimentară a populației cu HFpEF este în curs de desfășurare în cadrul studiului PARAGON, un studiu multicentric, randomizat, dublu-orb, cu grupuri paralele, controlat activ. Acest studiu are ca scop evaluarea eficacității și siguranței sacubitrilului/valsartanului comparativ cu valsartanul asupra morbidității și mortalității la pacienții cu insuficiență cardiacă (clasa NYHA II-IV) și fracție de ejecție conservată.
În sfârșit, dar nu în ultimul rând, foarte recent, neprilizina solubilă circulantă (sNEP) a fost propusă ca biomarker putativ.2 În prezent, datele privind sNEP au sugerat că ar putea juca un rol prognostic atât în insuficiența cardiacă cronică10 , cât și în insuficiența cardiacă acută decompensată11 , dar în HFpEF rezultatele sunt controversate.12 Interesant este faptul că sNEP circulantă s-a dovedit a fi activă din punct de vedere catalitic.13 Mai mult, un raport recent a demonstrat că sNEP ar putea fi chiar superioară NT-proBNP ca biomarker prognostic surogat al axei neurohormonale în insuficiența cardiacă.14 Înainte de introducerea sa în practica clinică, sunt obligatorii perfecționări suplimentare ale testelor sNEP. Cu toate acestea, datele raportate până în prezent sugerează că ar putea deveni un instrument valoros pentru prognosticul pacienților și, în cele din urmă, pentru orientarea terapeutică.
Ca un epilog, costul tratamentului cu acest nou agent este posibil să reprezinte o barieră în calea utilizării sale în practica clinică de zi cu zi din viața reală, deoarece costul agenților eficienți, cum ar fi IECA enalapril, este foarte scăzut (comparabil cu costul gumei de mestecat în multe țări). În mod conceptibil, se poate propune punerea în aplicare a unei strategii bazate pe biomarker pentru a trece preferențial de la tratamentul cu IECA la Entresto la cei mai bolnavi pacienți. În acest sens, este demn de remarcat faptul că utilizarea peptidelor natriuretice s-a numărat printre criteriile de includere în studiul PARADIGM-HF. Raportul cost-eficacitate și costul pe an de viață câștigat, ajustat la calitatea vieții, al sacubitrilului/valsartanului în raport cu enalaprilul pentru tratamentul HFrEF merită o cercetare intensivă în scenarii din lumea reală, ajustate în funcție de țară și de sistemul de sănătate.15
CONFLICTE DE INTERESE
A. Bayes-Genis și J. Lupón au depus o cerere de brevet pentru sNEP ca biomarker prognostic, care este în curs de aprobare. A. Bayes-Genis a ținut prelegeri și a participat la comitete consultative din partea Novartis.
.