Neprylizyna stała się przedmiotem zainteresowania kardiologii ze względu na imponujące korzyści z połączenia inhibicji neprylizyny i blokady receptora angiotensyny wykazane w niedawnym badaniu PARADIGM-HF, w którym badano LCZ696 (obecnie znany jako sakubitril/walwalsartan i wprowadzany na rynek przez firmę Novartis pod nazwą Entresto) w leczeniu skurczowej niewydolności serca z obniżoną frakcją wyrzutową (HFrEF).1 Jednak neprylizyna EC 3.4.24.11 (znana również jako neutralna endopeptydaza, endoproteaza 24.11, NEP, wspólny antygen ostrej białaczki limfoblastycznej, antygen różnicowania gromady neutrofilów 10, błonowa metaloendopeptydaza EC 3.4.24.11 i enkefalinaza) jest wysoce wszechstronnym enzymem, który powrócił do światła reflektorów po burzliwej karierze trwającej > 40 lat.2
W układzie sercowo-naczyniowym, neprylizyna rozszczepia liczne wazoaktywne peptydy. Niektóre z tych peptydów mają działanie rozszerzające naczynia (w tym peptydy natriuretyczne, adrenomedullina i bradykinina), a inne mają działanie wazokonstrykcyjne (między innymi angiotensyna I i II oraz endotelina-1). Niemniej jednak, neprylizyna wykazuje różne względne powinowactwa do różnych substratów; najwyższe powinowactwo wykazuje do przedsionkowego peptydu natriuretycznego, peptydu natriuretycznego typu C oraz angiotensyn I i II; najniższe powinowactwo wykazuje do peptydu natriuretycznego typu B (BNP), endoteliny-1 i bradykininy.3
Od dziesięcioleci neprylizyna jest ważnym biotargetem. Środowisko akademickie i przemysł połączyły aktywne wysiłki w poszukiwaniu inhibitorów neprylizyny (NEPI), które mogłyby być użyteczne w praktyce klinicznej. Początkowo, w późnych latach 80. i wczesnych 90. ubiegłego wieku, testowano monoterapię NEPI. Candoxatril wykazał wstępnie obiecujący wpływ na parametry hemodynamiczne. Jednak inny NEPI, ekadotryl, prowadził do większej śmiertelności, bez dowodów na skuteczność kliniczną w porównaniu z placebo u pacjentów z niewydolnością serca.4,5 W związku z tym zaprzestano rozwijania monoterapii NEPI w niewydolności serca. Następnie w niektórych badaniach wykazano dowody na jednoczesną aktywację układu renina-angiotensyna-aldosteron, wraz ze zwiększeniem bioaktywności peptydów natriuretycznych. Wyniki te stały się inspiracją do opracowania i testowania leków łączących działanie NEPI i inhibitorów konwertazy angiotensyny (ACEI), co doprowadziło do powstania leków znanych jako inhibitory wazopeptydazy. Opracowano kilka inhibitorów wazopeptydazy, w tym omapatrilat, fasidotril, sampatrilat i mixanpril. Po przeprowadzeniu licznych badań okazało się, że omapatrilat wywołuje coraz większą liczbę istotnych klinicznie epizodów obrzęku naczynioruchowego.6 Po ponad dziesięciu latach błądzenia po pustyni opracowano nową koncepcję – połączenie NEPI i blokerów receptora angiotensyny II (ARBs), co doprowadziło do powstania nowej klasy leków zwanych inhibitorami neprylizyny receptora angiotensyny. Sacubitril/walwalsartan jest pierwszym w klasie inhibitorem neprylizyny receptora angiotensyny, który wykazał lepsze od oczekiwanych wyniki w badaniu PARADIGM-HF1 (rycina).
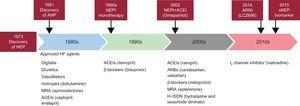
Schemat historycznych wyróżników neprylizyny. ACEI, inhibitor konwertazy angiotensyny; ANP, przedsionkowy peptyd natriuretyczny; ARB, bloker receptora angiotensyny II; ARNI, inhibitor neprylizyny receptora angiotensyny; HF, niewydolność serca; MRA, antagonista receptora mineralokortykoidowego; NEP, neprylizyna; NEPI, inhibitor neprylizyny; sNEP, rozpuszczalna neprylizyna.
PARADIGM-HF było wielonarodowym, randomizowanym, podwójnie zaślepionym badaniem obejmującym 8442 pacjentów. Celem było porównanie sakubitrilu/walwalsartanu z enalaprylem u dorosłych pacjentów z przewlekłą niewydolnością serca (klasa II-IV wg New York Heart Association) i zmniejszoną frakcją wyrzutową lewej komory (LVEF ≤ 40%, później zmieniono na ≤ 35%), w uzupełnieniu innej terapii niewydolności serca.1 Pierwszorzędowym punktem końcowym był złożony zgon z przyczyn sercowo-naczyniowych lub hospitalizacja z powodu niewydolności serca. Przed przystąpieniem do badania pacjenci byli leczeni standardowo, co obejmowało ACEI/ARB (> 99%), beta-blokery (94%), antagonistów mineralokortykoidów (58%) i diuretyki (82%). Mediana czasu obserwacji wynosiła 27 miesięcy, a pacjenci byli leczeni przez okres do 4,3 roku.
Pacjenci byli zobowiązani do przerwania dotychczasowej terapii ACEI lub ARB i przystąpienia do sekwencyjnego, pojedynczo ślepego, okresu wstępnego. Podczas okresu run-in otrzymywali leczenie enalaprylem w dawce 10 mg dwa razy na dobę, a następnie pojedynczo zaślepione leczenie sakubitrylem/walwalsartanem w dawce 100 mg dwa razy na dobę, która została zwiększona do 200 mg dwa razy na dobę. Następnie zostali oni randomizowani do okresu badania prowadzonego metodą podwójnie ślepej próby. W tym okresie otrzymywali albo sakubitril/walwalsartan 200mg albo enalapril 10mg, dwa razy dziennie. Średni wiek badanej populacji wynosił 64 lata, a 19% miało 75 lat lub więcej. W momencie randomizacji 70% pacjentów było w klasie II NYHA, 24% w klasie III, a 0,7% w klasie IV. Średnia LVEF wynosiła 29%, a 963 (11,4%) pacjentów miało wyjściową LVEF > 35% i ≤ 40%. Badanie zostało przedwcześnie zakończone z powodu zbyt dużej redukcji zgonów z przyczyn sercowo-naczyniowych oraz redukcji złożonego pierwszorzędowego punktu końcowego (zgon z przyczyn sercowo-naczyniowych lub hospitalizacja wtórna do niewydolności serca). Badanie PARADIGM-HF jest również określane jako badanie 20%, ze względu na jednorodne ∼20% względne zmniejszenie wszystkich badanych punktów końcowych, w tym złożonego pierwszorzędowego punktu końcowego, jakim był zgon z przyczyn sercowo-naczyniowych, nagły zgon sercowy i hospitalizacja z powodu niewydolności serca (Tabela 1).
PARADIGM-HF Trial: Treatment Effects on the Primary Composite Endpoint, Its Components, and All-cause Mortality, Over a Median Follow-up of 27 Months
| Punkty końcowe | Współczynnik ryzyka (95%CI) | Zmniejszenie ryzyka względnego | P |
|---|---|---|---|
| Pierwotny złożony punkt końcowy zgonu z powodu CV i hospitalizacji z powodu niewydolności serca | 0.80 (0,73-0,87) | 20% | .0000002 |
| Poszczególne składowe pierwszorzędowego złożonego punktu końcowego | |||
| Zgon z powodu CV | 0,80 (0,71-0.89) | 20% | .00004 |
| Pierwsza hospitalizacja z powodu niewydolności serca | 0,79 (0,71-0,89) | 21% | .00004 |
| Podstawowy punkt końcowy | |||
| Śmiertelność z wszystkich przyczyn | 0,84 (0,76-0,93) | 16% | .0005 |
95%CI, 95% przedział ufności; CV, cardiovascular-related.
Chociaż sakubitril/walwalsartan wykazał ogromną obietnicę, istnieją wyzwania i nierozwiązane kwestie, które zasługują na dodatkowe badania i dalsze wyjaśnienia (Tabela 2). Niektóre z tych kwestii zostały poruszone i omówione w sprawozdaniu oceniającym Europejskiej Agencji Leków dotyczącym produktu Entresto.7
Summary of Safety Concerns for Sacubitril/Valsartan
| Ważne zidentyfikowane zagrożenia | Nadciśnienie tętnicze Upośledzenie czynności nerek Hiperkaliemia Obrzęk naczynioruchowy |
| Ważne potencjalne zagrożenia | Hepatotoksyczność Upośledzenie funkcji poznawczych Interakcje lek-stalatynaInterakcje lekowe Trombocytopenia Neutropenia |
| Brak informacji | Pacjenci pediatryczni z HF Pacjenci z ciężkimi zaburzeniami czynności nerek Dane dotyczące długotrwałego stosowaniaDane długoterminowe dotyczące stosowania sakubitrylu/walwalsartanu w HF Efekty u pacjentów z HF niewrażliwych na ACEI/ARB |
ACEI, inhibitor enzymu konwertującego angiotensynę; ARB, bloker receptora angiotensyny II; HF, niewydolność serca.
Zmodyfikowano na podstawie raportu oceniającego Europejskiej Agencji Leków.7
Po pierwsze, gdy u pacjentów występują problemy z tolerancją (np. skurczowe ciśnienie tętnicze ≤ 95 mmHg, objawowe niedociśnienie tętnicze, hiperkaliemia, zaburzenia czynności nerek), obecne zalecenia przewidują dostosowanie jednocześnie stosowanych leków i (lub) czasowe zmniejszenie dawki lub odstawienie sakubitrylu/walwalsartanu. W rzeczywistości Europejska Agencja Leków zaleca, aby nie rozpoczynać leczenia u pacjentów ze stężeniem potasu w surowicy > 5,4 mmol/l lub ze skurczowym ciśnieniem krwi
mmHg.
Po drugie, dane dotyczące pacjentów, którzy obecnie przyjmują małe dawki ACEI lub ARB lub nie przyjmują ich wcale, są ograniczone. Dlatego aktualne zalecenia dla tych pacjentów to rozpoczęcie leczenia od dawki 50 mg dwa razy na dobę i powolne miareczkowanie dawki (podwajanie co 3-4 tygodnie).
Po trzecie, sakubitrylu/walwalsartanu nie należy podawać jednocześnie z ACEI lub ARB. Podczas jednoczesnego stosowania z ACEI istnieje duże potencjalne ryzyko wystąpienia obrzęku naczynioruchowego. W związku z tym nie wolno rozpoczynać stosowania sakubitrylu/walsartanu przez co najmniej 36 godzin po przerwaniu leczenia ACEI.
Po czwarte, nie jest wymagane dostosowanie dawki u pacjentów z łagodnymi zaburzeniami czynności nerek (szacowany wskaźnik filtracji kłębuszkowej 60-90 ml/min/1,73 m2). Jednak u pacjentów z umiarkowanymi zaburzeniami czynności nerek (szacowany współczynnik przesączania kłębuszkowego 30-60 ml/min/1,73 m2) należy rozważyć zastosowanie dawki początkowej 50 mg dwa razy na dobę. Nie ma danych dotyczących pacjentów ze schyłkową niewydolnością nerek, ale nie zaleca się stosowania sakubitrylu/walsartanu u tych pacjentów.
Po piąte, należy zachować ostrożność podczas rozpoczynania stosowania sakubitrylu/walsartanu u pacjentów z IV klasyfikacją czynnościową według NYHA, ze względu na ograniczone doświadczenie kliniczne w tej populacji.
Po szóste, BNP nie jest odpowiednim biomarkerem niewydolności serca u pacjentów leczonych sakubitrylem/walwalsartanem, ponieważ jest substratem neprylizyny. Zalecane jest przejście na NT-proBNP jako biomarker peptydów natriuretycznych.
Po siódme, teoretyczne ryzyko związane z hamowaniem neprylizyny jest związane z gromadzeniem się substratu neprylizyny, amyloidu-β, w mózgu.8 W badaniu PARADIGM-HF nie odnotowano zwiększonej częstości występowania zdarzeń niepożądanych związanych z poznaniem lub demencją. Jednak efekty te mogły nie zostać wykryte do tej pory, ponieważ rozwój demencji może trwać dłużej niż obecny okres obserwacji uczestników badania. Ponadto nie spodziewano się udziału w badaniu osób z łagodną demencją. Jednak w trwającym badaniu III fazy PARAGON-HF wprowadzono ocenę funkcji poznawczych.
Po ósme, jednoczesne stosowanie sakubitrylu/walwalsartanu i atorwastatyny zwiększało Cmax atorwastatyny i jej metabolitów nawet 2-krotnie. U pacjentów, którzy otrzymywali jednocześnie sakubitryl/walwalsartan i statynę w badaniu PARADIGM-HF, nie obserwowano istotnego zwiększenia liczby potencjalnych zdarzeń niepożądanych związanych ze statyną. Niemniej jednak, dalsze analizy wykazały, że większe dawki statyn wiązały się z większą liczbą zdarzeń niepożądanych w połączeniu z sakubitrylem/walwalsartanem lub enalaprylem. Jednak prawidłowości te były różne, w zależności od rodzaju podawanej statyny. W oczekiwaniu na wyniki dalszych badań zalecono ostrożność w stosowaniu tego połączenia leków.7
Badanie PARADIGM-HF koncentruje się na przewlekłej niewydolności serca z ograniczoną LVEF. Pojawia się zatem pytanie: Co z pozostałymi 50% pacjentów z niewydolnością serca, ale z zachowaną frakcją wyrzutową, zwanych również pacjentami z HFpEF? Obecnie brak jest badań klinicznych dotyczących HFpEF, w których wykazano by korzyści terapeutyczne z zastosowaniem leków powszechnie stosowanych u chorych z obniżoną frakcją wyrzutową. W związku z tym terapia HFpEF jest ukierunkowana na zwalczanie objawów i czynników ryzyka sercowo-naczyniowego. Jednak wśród pacjentów z HFpEF sakubitril/walwalsartan w badaniu 2. fazy wykazał obiecujące wyniki w zakresie bezpieczeństwa i skuteczności. Badanie PARAMOUNT było randomizowanym, podwójnie zaślepionym, prowadzonym w grupach równoległych, aktywnie kontrolowanym badaniem, w którym porównywano sakubitril/walsartan z samym walsartanem.9 Pierwszorzędowym punktem końcowym była zmiana stężenia NT-proBNP w ciągu 12 tygodni w stosunku do wartości wyjściowych. Grupy miały podobną charakterystykę wyjściową. Większość pacjentów była w podeszłym wieku, płci żeńskiej, z nadwagą i zakwalifikowana do II klasy NYHA. Większe zmniejszenie NT-proBNP stwierdzono w 4. tygodniu w grupie sakubitrilu/walsartanu w porównaniu z grupą walsartanu, ale nie osiągnęło ono istotności (P = .063). W 12 tygodniu NT-proBNP było znacząco zmniejszone w grupie sakubitrilu/walsartanu w porównaniu z walsartanem (P = .005). Wyniki badania PARAMOUNT sugerują, że sakubitril/walwalsartan może mieć korzystne działanie u pacjentów z HFpEF. Dalsze badania w populacji pacjentów z HFpEF są prowadzone w ramach badania PARAGON, wieloośrodkowego, randomizowanego, prowadzonego metodą podwójnie ślepej próby, z grupą równoległą, aktywnie kontrolowanego badania. Celem tego badania jest ocena skuteczności i bezpieczeństwa stosowania sakubitrilu/walsartanu w porównaniu z walsartanem w odniesieniu do zachorowalności i śmiertelności u pacjentów z niewydolnością serca (klasa II-IV wg NYHA) i zachowaną frakcją wyrzutową.
Wreszcie, co nie mniej ważne, bardzo niedawno jako przypuszczalny biomarker zaproponowano krążącą rozpuszczalną neprylizynę (sNEP).2 Obecnie dane dotyczące sNEP sugerują, że może ona odgrywać rolę prognostyczną zarówno w przewlekłej10 , jak i ostrej zdekompensowanej niewydolności serca,11 ale w HFpEF wyniki są kontrowersyjne.12 Co ciekawe, wykazano, że krążąca sNEP jest aktywna katalitycznie.13 Co więcej, w ostatnim doniesieniu wykazano, że sNEP może nawet przewyższać NT-proBNP jako zastępczy biomarker prognostyczny osi neurohormonalnej w niewydolności serca.14 Przed wprowadzeniem sNEP do praktyki klinicznej konieczne jest dalsze udoskonalenie testów do oznaczania sNEP. Dotychczasowe dane sugerują jednak, że może on stać się cennym narzędziem prognozowania stanu pacjenta, a ostatecznie także wskazówek dotyczących terapii.
Jako epilog, koszt leczenia tym nowym środkiem prawdopodobnie będzie stanowił barierę dla jego stosowania w codziennej rzeczywistej praktyce klinicznej, ponieważ koszt skutecznych środków, takich jak enalapril ACEI, jest bardzo niski (porównywalny z kosztem gumy do żucia w wielu krajach). Można zaproponować wdrożenie strategii opartej na biomarkerach w celu preferencyjnego przejścia z leczenia ACEI na Entresto u najbardziej chorych pacjentów. W związku z tym warto zauważyć, że stosowanie peptydów natriuretycznych było jednym z kryteriów włączenia do badania PARADIGM-HF. Efektywność kosztowa i koszt na zyskany rok życia skorygowany o jakość sakubitrilu/walwalsartanu w porównaniu z enalaprylem w leczeniu HFrEF zasługują na intensywne badania w rzeczywistych scenariuszach dostosowanych do kraju i systemu opieki zdrowotnej.15
KONFLIKT INTERESÓW
A. Bayes-Genis i J. Lupón złożyli wniosek o patent na sNEP jako biomarker prognostyczny, który oczekuje na zatwierdzenie. A. Bayes-Genis prowadziła wykłady i uczestniczyła w radach doradczych firmy Novartis.
.