US Pharm. 2017;42(4):HS16-HS20.
ABSTRACT: Martwicze zakażenia tkanek miękkich (Necrotizing soft-tissue infections, NSTIs) są rodzajem poważnego zakażenia bakteryjnego, które wymaga szybkiego rozpoznania i interwencji lekarzy i chirurgów w połączeniu z terminowym leczeniem antybiotykami. Infekcje te mogą mieć podłoże wielobakteryjne, ale w większości przypadków w grę wchodzi metycylinooporny Staphylococcus aureus. W leczeniu NSTI najważniejszy jest czas, aby uniknąć powikłań, takich jak amputacja, a nowe leki zostały ostatnio dodane do listy opcji terapeutycznych. Te nowe antybiotyki obejmują tedizolid (Sivextro), ortawancynę (Orbactiv) i dalbawancynę (Dalvance). Zwłaszcza długi okres półtrwania zarówno dalbawancyny, jak i oritawancyny pozwala na podawanie w schemacie jednodawkowym lub raz w tygodniu.
Nekrotyzujące zakażenie tkanek miękkich (NSTI) jest terminem szerszym niż martwicze zapalenie powięzi, ponieważ w NSTI zakażenie może wykraczać poza powięź. Potoczne określenia obejmują „bakterie zjadające ciało” i „zakażenie zjadające ciało”. Ten rodzaj infekcji został po raz pierwszy zauważony w V wieku p.n.e. przez Hipokratesa, który opisał go w następujący sposób: „Wielu zostało zaatakowanych przez erysipelas na całym ciele, gdy ekscytującą przyczyną był błahy wypadek… miąższ, ścięgna i kości odpadły w dużych ilościach… było wiele zgonów.”1 Od tego czasu, inne terminy opisowe były używane do scharakteryzowania NSTI, takie jak „wrzód fagedaeniczny, fagedena zgorzelinowa, wrzód zgorzelinowy, wrzód złośliwy, wrzód gnilny lub zgorzel szpitalna. „2 Termin zgorzel jest nadal używany, jak w zgorzeli Fourniera, która jest martwicą krocza i moszny.3
Epidemiologia
Ryzyko wystąpienia NSTI pozostaje ogólnie niskie, z około 1000 przypadków rocznie występujących w Stanach Zjednoczonych. Liczba ta może jednak rosnąć, być może z powodu większej świadomości i rozpoznawania stanu chorobowego, rosnącej oporności na antybiotyki lub zwiększonej zjadliwości bakterii.4
Etiologia
NSTI są klasyfikowane według lokalizacji anatomicznej (np. zgorzel Fourniera), ale najczęściej występują na kończynach, kroczu i narządach płciowych. Powszechne bakteryjne drobnoustroje sprawcze obejmują metycylinooporne gronkowce złociste (MRSA), gram-ujemne organizmy i beztlenowce oraz paciorkowce grupy A (GAS).4
Prezentacja kliniczna i diagnostyka
Wstępna prezentacja pacjentów z NSTI może naśladować objawy związane z zapaleniem tkanki łącznej, w tym rumień, obrzęk, gorączkę, stwardnienie i obrzęk poza obszarem zmian skórnych.4 Pacjenci mogą opisywać bolesność lub ból podobny do tego po naciągnięciu mięśnia.5 Objawy, które powinny nasilić podejrzenie NSTI u klinicysty to ból nieproporcjonalny do wyników badania (we wczesnym okresie choroby), obecność pęcherzyków, wybroczyny skórne poprzedzające martwicę skóry, gaz w tkankach i znieczulenie skóry. Ponadto, w porównaniu z pacjentami z rozpoznaniem cellulitis, chronologia zakażenia u pacjentów z NSTI wskazuje na znacznie szybszą progresję choroby.4 Dlatego u pacjentów podejrzewanych o cellulitis należy wykluczyć rozpoznanie martwiczego zapalenia powięzi.6 Aby doszło do zakażenia, bakterie muszą dostać się do krwioobiegu, zwykle przez ranę wnikającą (przerwanie ciągłości nabłonka lub powierzchni błony śluzowej), taką jak drobne skaleczenie lub zadrapanie, ukąszenie owada, owrzodzenie skóry lub rana pooperacyjna; czasami jednak takich urazów nie można zidentyfikować. Czynniki ryzyka NSTI obejmują stan obniżonej odporności (AIDS, steroidoterapia), otyłość, nadużywanie alkoholu, nowotwory, cukrzycę, choroby naczyń obwodowych, choroby nerek, niedożywienie i inne przewlekłe schorzenia. Czynne pozajelitowe stosowanie narkotyków (dożylne lub podskórne wstrzykiwanie nielegalnych substancji) również uznano za czynnik ryzyka, szczególnie w środowisku miejskim.7
Przegląd wytycznych
Wytyczne 2014 Infectious Diseases Society of America (IDSA) Practice Guidelines for the Diagnosis and Management of Skin and Soft Tissue Infections zawierają informacje dotyczące postępowania we wszystkich rodzajach zakażeń skóry i tkanek miękkich, począwszy od prostego zapalenia tkanki łącznej do wąglika skórnego u osób zdrowych i pacjentów w stanie ciężkim. Ponieważ zakażenia te występują we wszystkich grupach wiekowych, w wytycznych przedstawiono zalecenia zarówno dla pacjentów pediatrycznych, jak i dorosłych. W jednym z podrozdziałów wytycznych podano informacje dotyczące NSTI. Szczegółowe zalecenia dotyczące leczenia przedstawiono na podstawie oceny wskazującej na siłę dowodów potwierdzających dane zalecenie, zgodnie z systemem oceny zaleceń w wytycznych klinicznych IDSA/U.S. Public Health Service.6 Wytyczne zawierają odpowiedzi na 24 pytania kliniczne, w tym dwa dotyczące NSTI.
Pierwszym pytaniem związanym z NSTI poruszonym w wytycznych jest: Jaka jest preferowana ocena i leczenie martwiczego zapalenia powięzi, w tym zgorzeli Fourniera? Pierwsze zalecenie dotyczy szybkiej konsultacji chirurgicznej u pacjentów z agresywnymi zakażeniami z objawami toksyczności ogólnoustrojowej lub jeśli istnieje obawa wystąpienia martwiczego zapalenia powięzi lub zgorzeli gazowej.6 Po tym zaleceniu następują dwa zalecenia dotyczące antybiotykoterapii. Wstępna terapia przeciwdrobnoustrojowa powinna być szeroka, aby zapewnić pokrycie zarówno zakażeń jedno-, jak i wieloorganizmowych. Dodatkowo penicylina w połączeniu z klindamycyną jest zalecana w przypadku udokumentowanego martwiczego zapalenia powięzi wywołanego przez GAS. Wszystkie trzy zalecenia zostały ocenione jako silne przy niskiej jakości dowodów, co wskazuje, że działania pożądane wyraźnie przeważają nad działaniami niepożądanymi. Po zaleceniach zamieszczono przegląd dowodów, a następnie omówiono najczęstsze cechy kliniczne, przyczyny mikrobiologiczne (monomikrobowe versus polimikrobowe), diagnostykę i leczenie.
Odrębna część wytycznych skupia się na postępowaniu w klostridialnych NSTI zgodnie z następującym pytaniem: Jakie jest właściwe podejście do oceny i leczenia klostridialnej zgorzeli gazowej lub martwicy mięśnia sercowego? Po pierwsze, należy w trybie pilnym przeprowadzić chirurgiczną eksplorację miejsca podejrzanego o zgorzel gazową i usunięcie tkanek objętych procesem chorobowym. Zalecana jest antybiotykoterapia o szerokim spektrum działania, o ile nie ma jednoznacznej przyczyny mikrobiologicznej. W przypadku mionekrozy klostridialnej sugeruje się stosowanie penicyliny w połączeniu z klindamycyną. Wreszcie, nie zaleca się stosowania tlenoterapii hiperbarycznej. Wszystkie te sugestie mają silne zalecenia i wszystkie, z wyjątkiem zalecenia chirurgicznego, mają niską jakość dowodów (zalecenie chirurgiczne ma umiarkowaną jakość dowodów). Przegląd dowodów dotyczących tych zaleceń kończy część poświęconą NSTI.6
Poza tym, że NSTI różnią się od mniej poważnych zakażeń skóry obrazem klinicznym i innymi objawami ogólnoustrojowymi, wymagają innego podejścia do leczenia. Istnieje wiele odmian NSTI, ale leczenie antybiotykami i podejście chirurgiczne są podobne dla wszystkich typów, a interwencja chirurgiczna jest podstawowym postępowaniem w przypadku spodziewanego NSTI. Większość pacjentów będzie wymagała wielokrotnych wizyt na sali operacyjnej (OR), aż do momentu, gdy usuwanie zmian chorobowych nie będzie już konieczne.6
Leczenie
Wstępny wybór antybiotyków powinien obejmować środki o aktywności wobec szerokiego zakresu drobnoustrojów, w tym aerobów, MRSA i anaerobów (TABELA 1).6 Przy wyborze antybiotyków należy brać pod uwagę czynniki specyficzne dla pacjenta, takie jak wcześniejsza ekspozycja na antybiotyki, współistniejące stany chorobowe, zaburzenia czynności narządów i alergie. Podobnie jak w przypadku leczenia większości zakażeń, właściwe postępowanie przeciwdrobnoustrojowe obejmuje optymalizację antybiotykoterapii do najwęższego spektrum po zidentyfikowaniu przyczyny mikrobiologicznej.
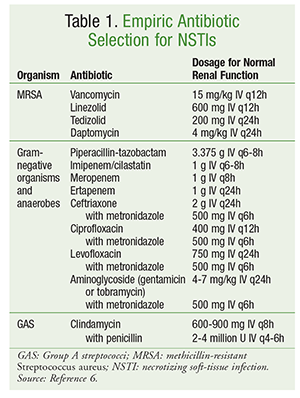
Szczegółowe postępowanie w NSTI obejmuje stosowanie różnych antybiotyków. W przypadku zakażeń wielobakteryjnych często kontynuuje się antybiotykoterapię o szerokim spektrum działania. W przypadku zakażeń wywołanych przez GAS należy stosować zarówno klindamycynę, jak i penicylinę. Dodanie klindamycyny hamuje produkcję toksyn i cytokin, a zastosowanie penicyliny zapewnia ochronę w przypadku oporności GAS na klindamycynę. W przypadku zakażeń wywołanych przez S. aureus wrażliwe na metycylinę, preferowane jest stosowanie nafcyliny, oksacyliny lub cefazoliny. W zakażeniach wywołanych przez bakterie Clostridial należy stosować klindamycynę w połączeniu z penicyliną. Antybiotykoterapia jest zazwyczaj kontynuowana do momentu, gdy nie jest konieczne dalsze usuwanie zmian chorobowych, pacjent wykazuje poprawę kliniczną, a gorączka nie występuje przez 48 do 72 godzin.6
Od czasu opublikowania wytycznych IDSA z 2014 roku kilka nowych antybiotyków zostało zatwierdzonych do stosowania w leczeniu powikłanych zakażeń skóry i tkanek miękkich. Te środki to tedizolid (Sivextro), oritawancyna (Orbactiv) i dalbawancyna (Dalvance).
Tedizolid jest antybiotykiem oksazolidynonowym podobnym do linezolidu. Wykazuje niezawodną aktywność wobec MRSA i innych wielolekoopornych organizmów Gram-dodatnich. W przeciwieństwie do dawkowania linezolidu dwa razy dziennie, tedizolid jest podawany w pojedynczej dawce dobowej, doustnie lub dożylnie. Tedizolid może mieć korzystniejsze profile działań niepożądanych i interakcji lekowych w porównaniu z linezolidem.8 Chociaż tedizolid był badany w leczeniu ostrych bakteryjnych zakażeń skóry i struktur skórnych, nie był badany w NSTI.
Dalbavancin i oritavancin są lipoglikopeptydami zatwierdzonymi do leczenia ostrych bakteryjnych zakażeń skóry i struktur skórnych. Środki te są wyjątkowe pod tym względem, że mają długi okres półtrwania, co umożliwia stosowanie schematu jednodawkowego lub raz w tygodniu. Dawkę dalbawancyny należy zmniejszyć u pacjentów z klirensem kreatyniny <30 mL/minutę. Oritawankina nie wymaga dostosowania dawki związanego z zaburzeniami czynności narządów, ale nie powinna być stosowana u pacjentów otrzymujących heparynę, ponieważ sztucznie wydłuża czas trwania testów krzepnięcia. Oritawankina może również nasilać działanie antagonistów witaminy K, takich jak warfaryna.9 Oba leki mają udowodnioną skuteczność w leczeniu zakażeń skóry i zakażeń struktur skórnych, ale nie zostały ocenione pod kątem stosowania w zakażeniach martwiczych.
Terapie wspomagające w leczeniu NSTI obejmują dożylne podawanie immunoglobuliny (IVIG) i tlenoterapię hiperbaryczną. Uważa się, że IVIG jest korzystna ze względu na możliwą neutralizację toksyn produkowanych w infekcjach paciorkowcowych. Zmniejszenie ilości tych toksyn mogłoby potencjalnie zmniejszyć niektóre z objawów niewydolności narządów, wstrząsu i zniszczenia tkanek często obserwowanych w NSTI.6 W czasie, gdy opublikowano wytyczne IDSA (kwiecień 2014 r.), badanie obserwacyjne i próba z Europy donosiły o pewnych sukcesach stosowania IVIG w zakażeniach paciorkowcowych.6 Jednak w oparciu o brak dowodów potwierdzających skuteczność, stosowanie IVIG nie jest obecnie zalecane.
W nowszym badaniu opisano skuteczność klindamycyny i IVIG w zwalczaniu inwazyjnych zakażeń GAS.10 Osiemdziesięciu czterech pacjentów spełniało kryteria inwazyjnej choroby GAS, a IVIG zastosowano u 14 pacjentów, w tym u ośmiu z martwiczym zapaleniem powięzi. Śmiertelność była mniejsza u pacjentów leczonych klindamycyną i IVIG, ale różnica ta nie była istotna. Chociaż nie stwierdzono statystycznej różnicy w śmiertelności po dodaniu IVIG do klindamycyny, autorzy zasugerowali, że może to przynieść korzyści u dorosłych z cięższą postacią choroby.10
Tlenoterapia hiperbaryczna (HBOT) jest zalecana w leczeniu zgorzeli gazowej, ale jej rola jest kontrowersyjna.6 Badania laboratoryjne wykazały, że bogate w tlen stany tkankowe pomagają hamować wzrost Clostridium perfringens i zwiększają obronę gospodarza przed obcymi komórkami, ale brakuje kryteriów pozwalających zidentyfikować pacjentów, którzy mogą odnieść korzyści i określić właściwy czas rozpoczęcia terapii.6,11 Nic nie powinno opóźniać nagłego chirurgicznego oczyszczenia i podania antybiotyków, ponieważ oba te elementy są ważne dla zapewnienia przeżycia.6
Ponieważ większość opublikowanych badań była mała i nie posiadała wystarczającej siły przebicia, przeprowadzono badanie w celu oceny danych dotyczących stosowania HBOT z kilku ośrodków posiadających ośrodki HBOT.11 W ciągu 3 lat, 14 ośrodków HBOT widziało 1 583 przypadki NSTI i zapewniło adjuwantowy HBOT w 117 przypadkach. Grupa HBOT miała wyższe koszty i dłuższy czas pobytu w szpitalu niż grupa kontrolna, ale miała znacząco niższą śmiertelność szpitalną (odpowiednio 5% vs. 12%; P <.05). Po uwzględnieniu ciężkości choroby, najciężej chorzy pacjenci poddani HBOT mieli istotnie niższe wskaźniki śmiertelności i powikłań, ale nie było różnic w długości pobytu i kosztach. Analiza wieloczynnikowa wykazała, że pacjenci, którzy nie otrzymywali HBOT, byli bardziej narażeni na zgon podczas hospitalizacji (iloraz szans, 10,6; 95% CI 5,2-25,1). Każdy wzrost ciężkości choroby wiązał się ze zwiększonym ryzykiem zgonu.
To badanie 14 ośrodków HBOT wydaje się wskazywać na poprawę wyników, szczególnie w przypadku najbardziej chorych pacjentów przyjmowanych bezpośrednio do ośrodka mającego możliwość prowadzenia takiej terapii.11 Nie rozwiewa to jednak kontrowersji wokół stosowania HBOT, ponieważ badanie to miało kilka ograniczeń. Badanie przeprowadzono retrospektywnie z wykorzystaniem administracyjnej bazy danych w akademickich ośrodkach medycznych. Ponadto, w niektórych ośrodkach właścicielem ośrodka HBOT może być osoba trzecia, co sprawia, że wyniki badania są mniej uogólnione na pacjentów w tych instytucjach. Randomizowane, kontrolowane badanie byłoby pomocne w określeniu ostatecznej korzyści z tej terapii.
Powikłania
Śmiertelność związana z NSTI wynosi od 30% do 70% u pacjentów z martwiczym zapaleniem powięzi wywołanym przez GAS w połączeniu z hipotensją i niewydolnością narządów.6 Ponieważ leczenie obejmuje wiele wizyt na sali operacyjnej, rutynowo zgłaszane są duże rany i możliwe amputacje. Inne powikłania, takie jak operacje rekonstrukcyjne, sepsa, zakażenia szpitalne i przedłużony czas opieki krytycznej z powodu rozwoju niewydolności wielonarządowej, są częstymi powikłaniami NSTI.12
Informacje na temat długoterminowych skutków NSTI zebrano na podstawie wywiadów pogłębionych z 18 osobami, które przeżyły.12,13 Badacze stwierdzili, że na zgłaszaną jakość życia istotny wpływ miało funkcjonowanie fizyczne i utrzymujący się ból. Stwierdzono, że wpływ doświadczenia na relacje rodzinne i inne był również znaczący. Kilka osób, które przeżyły, opisało długoterminowe psychologiczne konsekwencje choroby, w tym depresję i stres pourazowy.
Wnioski
Farmaceuci szpitalni są bardzo dobrze przystosowani do pomocy w opiece nad pacjentami z NSTI, w tym do usprawnienia opieki, promowania zarządzania antybiotykami oraz poprawy wyników klinicznych, redukcji kosztów, minimalizacji powikłań i ponownych przyjęć. Inne role farmaceuty obejmują identyfikację idealnych pacjentów dla nowych, ale droższych środków terapeutycznych (np. oritawancyna) i rozpoznawanie interakcji lekowych (tj. antykoagulantów) z tymi klasami antybiotyków.
1. Descamps V, Aitken J, Lee MG. Hippocrates on necrotising fasciitis. Lancet. 1994;344:556.
2. Loudon I. Necrotising fasciitis, hospital gangrene, and phagedena. Lancet. 1994;344:1416-1419.
3. Sarani B, Strong M, Pascual J, Schwab CW. Necrotizing fasciitis: current concepts and review of the literature. J Am Coll Surg. 2009;208:279-288.
4. Hakkarainen TW, Kopari NM, Pham TN, Evans HL. Necrotizing soft tissue infections: review and current concepts in treatment, systems of care, and outcomes. Curr Probl Surg. 2014;51:344-362.
5. CDC. Martwicze zapalenie powięzi: rzadka choroba, szczególnie dla osób zdrowych. www.cdc.gov/features/necrotizingfasciitis/. Dostęp 29 listopada 2016 r.
6. Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the Infectious Diseases Society of America. Clin Infect Dis. 2014;59:147-159.
7. Bosshardt TL, Henderson VJ, Organ CH Jr. Necrotizing soft-tissue infections. Arch Surg. 1996;131:846-852.
8. Kisgen JJ, Mansour H, Unger NR, Childs LM. Tedizolid: a new oxazolidinone antimicrobial. Am J Health Syst Pharm. 2014;71:621-633.
9. Roberts KD, Sulaiman RM, Rybak MJ. Dalbavancin i oritavancin: innowacyjne podejście do leczenia zakażeń wywołanych przez bakterie Gram-dodatnie. Pharmacotherapy. 2015;35:935-948.
10. Carapetis JR, Jacoby P, Carville K, et al. Effectiveness of clindamycin and intravenous immunoglobulin, and risk of disease in contacts, in invasive group A streptococcal infections. Clin Infect Dis. 2014;59:358-365.
11. Shaw JJ, Psoinos C, Ernhoff TA, et al. Not just full of hot air: hyperbaric oxygen therapy increases survival in cases of necrotizing soft tissue infections. Surg Infect (Larchmt). 2014;15:328-335.
12. Hakkarainen TW, Burkette Ikebata N, Bulger E, Evans HL. Moving beyond survival as a measure of success: understanding the patient experience of necrotizing soft-tissue infections. J Surg Res. 2014;192:143-149.
13. Miller LG, Perdreau-Remington F, Rieg G, et al. Necrotizing fasciitis caused by community-associated methicillin-resistant Staphylococcus aureus in Los Angeles. New Engl J Med. 2005;352:1445-1453.