Sulfonowanie metylobenzenu
Metylobenzen jest bardziej reaktywny niż benzen z powodu tendencji grupy metylowej do „push” elektronów w kierunku pierścienia.
Skutkiem tej większej reaktywności jest to, że metylobenzen będzie reagować z dymiącym kwasem siarkowym w temperaturze 0°C, a także ze stężonym kwasem siarkowym, jeśli są ogrzewane pod chłodnicą zwrotną przez około 5 minut.
As well as the effect on the rate of reaction, with methylbenzene you also have to think about where the sulfonic acid group ends up on the ring relative to the methyl group. Grupy metylowe mają tendencję do „kierowania” nowych grup do pozycji 2- i 4- na pierścieniu (zakładając, że grupa metylowa znajduje się w pozycji 1-). Mówi się, że grupy metylowe są 2,4-pośredniczące.
Więc otrzymujemy mieszaninę, która składa się głównie z dwóch izomerów. Tylko około 5 – 10% izomeru 3- jest utworzony. Główne reakcje to:
![]()
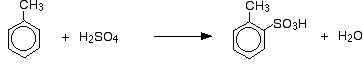
oraz:
![]()
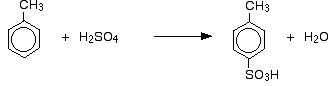
W przypadku sulfonowania, dokładna proporcja tworzących się izomerów zależy od temperatury reakcji. Wraz ze wzrostem temperatury uzyskuje się coraz większe proporcje izomeru 4-, a mniejsze izomeru 2-. Dzieje się tak, ponieważ sulfonowanie jest odwracalne. Grupa kwasu sulfonowego może ponownie odpaść od pierścienia i przyłączyć się w innym miejscu. Ma to tendencję do sprzyjania tworzeniu się najbardziej stabilnego termodynamicznie izomeru. Ta wymiana dzieje się bardziej w wyższych temperaturach.
4- izomer jest bardziej stabilny, ponieważ nie ma bałaganu w cząsteczce, jak byłoby, gdyby grupa metylowa i grupa kwasu sulfonowego były obok siebie.
.