Informacja prasowa
Poniedziałek, 28 grudnia 2020
Badanie finansowane przez NIH i BARDA obejmie do 30 000 ochotników.
Osoby w wieku 18 lat i starsze zainteresowane udziałem w tym badaniu mogą odwiedzić stronę coronaviruspreventionnetwork.org, ClinicalTrials.gov i wyszukać identyfikator NCT04611802 lub Novavax.com/PREVENT-19 w celu uzyskania szczegółowych informacji. Prosimy nie kontaktować się z medialnym numerem telefonu lub pocztą elektroniczną NIAID w celu zapisania się do tego badania.
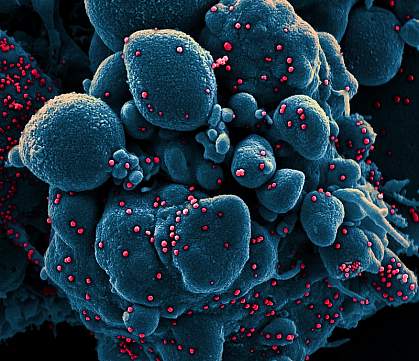 Kolorowy skaningowy mikrograf elektronowy komórki apoptotycznej (niebieski) zakażonej cząstkami wirusa SARS-COV-2 (czerwony), wyizolowanej z próbki pacjenta.NIAID
Kolorowy skaningowy mikrograf elektronowy komórki apoptotycznej (niebieski) zakażonej cząstkami wirusa SARS-COV-2 (czerwony), wyizolowanej z próbki pacjenta.NIAID Próba 3 fazy innej badanej szczepionki przeciwko koronawirusowi choroby 2019 (COVID-19) rozpoczęła rekrutację dorosłych ochotników. Randomizowane, kontrolowane placebo badanie obejmie około 30 000 osób w około 115 ośrodkach w Stanach Zjednoczonych i Meksyku. Oceni ono bezpieczeństwo i skuteczność NVX-CoV2373, kandydata na szczepionkę opracowanego przez firmę Novavax, Inc. z Gaithersburga w stanie Maryland. Novavax prowadzi to badanie jako sponsor regulacyjny. National Institute of Allergy and Infectious Diseases (NIAID), część National Institutes of Health, oraz Biomedical Advanced Research and Development Authority (BARDA), część U.S. Department of Health and Human Services Office of the Assistant Secretary for Preparedness and Response, finansują to badanie.
„Zajęcie się bezprecedensowym kryzysem zdrowotnym związanym z COVID-19 wymagało nadzwyczajnych wysiłków ze strony rządu, środowisk akademickich, przemysłu i społeczności”, powiedział dyrektor NIAID Anthony S. Fauci, M.D. „Rozpoczęcie tego badania – piątego badanego kandydata na szczepionkę przeciwko COVID-19, który będzie testowany w fazie 3 w Stanach Zjednoczonych – pokazuje naszą determinację, aby zakończyć pandemię poprzez rozwój wielu bezpiecznych i skutecznych szczepionek.”
Badanie jest prowadzone we współpracy z Operacją Warp Speed (OWS), współpracą wielu agencji nadzorowaną przez HHS i Departament Obrony, która ma na celu przyspieszenie rozwoju, produkcji i dystrybucji medycznych środków zaradczych dla COVID-19. Niektóre z uczestniczących amerykańskich ośrodków badawczych są częścią wspieranej przez NIAID sieci prewencyjnej COVID-19 (CoVPN). Sieć CoVPN obejmuje istniejące sieci badań klinicznych wspieranych przez NIAID z doświadczeniem w zakresie chorób zakaźnych i została zaprojektowana do szybkiej i dokładnej oceny kandydatów na szczepionki i przeciwciała monoklonalne w celu zapobiegania COVID-19.
Wolontariusze zostaną poproszeni o wyrażenie świadomej zgody przed ich udziałem w badaniu. Będą oni pogrupowani w dwie kohorty: osoby w wieku od 18 do 64 lat oraz osoby w wieku 65 lat i starsze, przy czym celem jest przyjęcie co najmniej 25% wszystkich ochotników, którzy mają 65 lat lub więcej. Organizatorzy badania kładą również nacisk na rekrutację osób, które są w grupie podwyższonego ryzyka ciężkiej choroby COVID-19, w tym osób czarnoskórych (w tym Afroamerykanów), rdzennych Amerykanów, osób pochodzenia latynoskiego lub hispanoamerykańskiego, a także osób, które cierpią na choroby podstawowe, takie jak otyłość, przewlekła choroba nerek lub cukrzyca.
„Doszliśmy tak daleko, tak szybko, ale musimy dotrzeć do mety”, powiedział dyrektor NIH Francis S. Collins, M.D., Ph.D. „Będzie to wymagało wielu szczepionek przy użyciu różnych podejść, aby zapewnić wszystkim bezpieczną i skuteczną ochronę przed tą śmiertelną chorobą.”
Po dostarczeniu podstawowej próbki nosogardła i krwi, uczestnicy zostaną przydzieleni losowo do otrzymania domięśniowego wstrzyknięcia badanej szczepionki lub placebo z soli fizjologicznej. Randomizacja odbędzie się w stosunku 2:1, przy czym dwóch ochotników otrzyma badaną szczepionkę na każdego ochotnika, który otrzyma placebo. Ponieważ badanie jest zaślepione, ani badacze, ani uczestnicy nie będą wiedzieli, kto otrzymuje szczepionkę. Drugi zastrzyk zostanie podany 21 dni po pierwszym.
Uczestnicy będą uważnie obserwowani pod kątem potencjalnych skutków ubocznych szczepionki i zostaną poproszeni o dostarczenie próbek krwi w określonych punktach czasowych po każdym zastrzyku i podczas kolejnych dwóch lat. Naukowcy będą analizować próbki krwi, aby wykryć i określić ilościowo reakcje immunologiczne na SARS-CoV-2, wirusa, który powoduje COVID-19. Co ważne, do rozróżnienia pomiędzy odpornością będącą wynikiem naturalnej infekcji a odpornością wywołaną przez szczepionkę zostaną użyte specjalistyczne testy. Pierwszorzędowym punktem końcowym badania jest określenie, czy szczepionka NVX-CoV2373 może zapobiec wystąpieniu objawowej choroby COVID-19 siedem lub więcej dni po drugim wstrzyknięciu w porównaniu z placebo.
Badana szczepionka firmy Novavax, NVX-CoV2373, jest wykonana ze stabilizowanej formy białka kolca koronawirusa przy użyciu opracowanej przez firmę technologii rekombinowanych nanocząstek białkowych. Oczyszczone antygeny białkowe zawarte w szczepionce nie mogą się replikować i nie mogą wywoływać COVID-19. Szczepionka zawiera również opatentowany adiuwant, MatrixM™. Adiuwanty są dodatkami, które wzmacniają pożądane reakcje układu odpornościowego na szczepionkę. NVX-CoV2373 jest podawana w postaci płynnej i może być przechowywana, przenoszona i dystrybuowana w temperaturze powyżej zera (35° do 46°F). Pojedyncza dawka szczepionki zawiera 5 mikrogramów (mcg) białka i 50 mcg adiuwantu.
W badaniach na zwierzętach szczepionka NVX-CoV2373 wytworzyła przeciwciała, które zablokowały białko kolca koronawirusa przed związaniem się z receptorami na powierzchni komórek, do których skierowany jest wirus, co zapobiegło zakażeniu wirusowemu. W wynikach badania klinicznego fazy 1, opublikowanych w New England Journal of Medicine, szczepionka NVX-CoV2373 była ogólnie dobrze tolerowana i wywoływała wyższe poziomy przeciwciał niż te obserwowane w próbkach krwi pobranych od osób, które wyzdrowiały po klinicznie istotnym zakażeniu wirusem COVID-19. NVX-CoV2373 jest również oceniany w badaniu fazy 2b w Republice Południowej Afryki, do którego obecnie zakwalifikowano 4 422 ochotników, a dane z kontynuacji badania fazy 1/2 w Stanach Zjednoczonych i Australii spodziewane są już w pierwszym kwartale 2021 roku. Novavax zakończył również niedawno rekrutację ponad 15 000 ochotników do badania fazy 3 szczepionki kandydującej w Wielkiej Brytanii, które również testuje dwie iniekcje 5 mcg białka i 50 mcg adiuwantu Matrix-M podawane w odstępie 21 dni.
Niezależna Rada Monitorowania Danych i Bezpieczeństwa (DSMB) zapewni nadzór w celu zapewnienia bezpiecznego i etycznego przebiegu badania. Wszystkie badania kliniczne fazy 3 dotyczące szczepionek kandydujących wspierane przez OWS są nadzorowane przez wspólną DSMB opracowaną w porozumieniu z inicjatywą NIH Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV).
Dorośli zainteresowani przyłączeniem się do tego badania mogą odwiedzić strony Coronaviruspreventionnetwork.org, Novavax.com/PREVENT-19 lub ClinicalTrials.gov i wyszukać identyfikator NCT04611802.
O sieci COVID-19 Prevention Network: COVID-19 Prevention Network (CoVPN) została utworzona przez National Institute of Allergy and Infectious Diseases (NIAID) w U.S. National Institutes of Health w odpowiedzi na globalną pandemię. Poprzez CoVPN, NIAID wykorzystuje wiedzę na temat chorób zakaźnych swoich istniejących sieci badawczych i partnerów globalnych w celu zaspokojenia pilnego zapotrzebowania na szczepionki i przeciwciała przeciwko SARS-CoV-2. CoVPN będzie pracować nad rozwojem i prowadzeniem badań w celu zapewnienia szybkiej i dokładnej oceny szczepionek i przeciwciał w celu zapobiegania COVID-19. Siedziba CoVPN znajduje się w Fred Hutchinson Cancer Research Center. Więcej informacji na temat CoVPN można znaleźć na stronie: coronaviruspreventionnetwork.org.
About HHS, ASPR, and BARDA: HHS działa na rzecz poprawy i ochrony zdrowia i dobrobytu wszystkich Amerykanów, zapewniając skuteczne usługi zdrowotne i ludzkie oraz wspierając postęp w medycynie, zdrowiu publicznym i usługach społecznych. Misją ASPR jest ratowanie życia i ochrona Amerykanów przed zagrożeniami bezpieczeństwa zdrowotnego XXI wieku. W ramach ASPR, BARDA inwestuje w innowacje, zaawansowane badania i rozwój, nabywanie i produkcję medycznych środków zaradczych – szczepionek, leków, terapii, narzędzi diagnostycznych i produktów niefarmaceutycznych potrzebnych do zwalczania zagrożeń dla bezpieczeństwa zdrowotnego. Do tej pory produkty wspierane przez BARDA uzyskały 55 zatwierdzeń, licencji lub dopuszczeń FDA. Aby dowiedzieć się więcej o federalnym wsparciu dla ogólnokrajowej reakcji na COVID-19, odwiedź stronę www.coronavirus.gov.
About Operation Warp Speed: OWS to partnerstwo pomiędzy komponentami Departamentu Zdrowia i Usług Społecznych oraz Departamentu Obrony, angażujące firmy prywatne i inne agencje federalne oraz koordynujące istniejące wysiłki całego HHS w celu przyspieszenia rozwoju, produkcji i dystrybucji szczepionek, terapii i diagnostyki COVID-19.
O Narodowym Instytucie Alergii i Chorób Zakaźnych: NIAID prowadzi i wspiera badania – w NIH, w całych Stanach Zjednoczonych i na całym świecie – w celu zbadania przyczyn chorób zakaźnych i chorób o podłożu immunologicznym oraz opracowania lepszych sposobów zapobiegania, diagnozowania i leczenia tych chorób. Komunikaty prasowe, arkusze informacyjne i inne materiały związane z NIAID są dostępne na stronie internetowej NIAID.
O Narodowych Instytutach Zdrowia (NIH):NIH, narodowa agencja badań medycznych, obejmuje 27 Instytutów i Centrów i jest częścią Departamentu Zdrowia i Usług Społecznych Stanów Zjednoczonych. NIH jest główną agencją federalną prowadzącą i wspierającą podstawowe, kliniczne i przekładające się na praktyczne zastosowania badania medyczne, a także bada przyczyny, metody leczenia i sposoby wyleczenia zarówno powszechnych, jak i rzadkich chorób. Więcej informacji o NIH i jego programach można znaleźć na stronie www.nih.gov.
NIH…Turning Discovery Into Health®
###