La neprilysina è diventata un centro di interesse in cardiologia, a causa degli impressionanti benefici della combinazione dell’inibizione della neprilysina e del blocco del recettore dell’angiotensina dimostrati nel recente trial PARADIGM-HF, che ha testato LCZ696 (ora noto come sacubitril/valsartan e commercializzato da Novartis con il nome di Entresto) per il trattamento dell’insufficienza cardiaca sistolica con frazione di eiezione ridotta (HFrEF).1 Tuttavia, la neprilisina EC 3.4.24.11 (nota anche come endopeptidasi neutra, endoproteasi 24.11, NEP, antigene comune della leucemia linfoblastica acuta, antigene di differenziazione cluster dei neutrofili 10, metalloendopeptidasi di membrana EC 3.4.24.11 ed enkefalinasi) è un enzima molto versatile, che è tornato sotto i riflettori, dopo una carriera movimentata di > 40 anni.2
Nel sistema cardiovascolare, la neprilisina scinde numerosi peptidi vasoattivi. Alcuni di questi peptidi hanno effetti vasodilatatori (compresi i peptidi natriuretici, l’adrenomedullina e la bradichinina), mentre altri hanno effetti vasocostrittori (angiotensina I e II ed endotelina-1, tra gli altri). Tuttavia, la neprilisina mostra varie affinità relative tra i diversi substrati; la sua maggiore affinità è per il peptide natriuretico atriale, il peptide natriuretico di tipo C e le angiotensine I e II; la sua minore affinità è per il peptide natriuretico di tipo B (BNP), l’endotelina-1 e la bradichinina.3
Per decenni, la neprilisina è stata un importante biotarget. Il mondo accademico e l’industria hanno unito gli sforzi attivi nella ricerca di inibitori della neprilisina (NEPI) che potrebbero essere utili nella pratica clinica. Inizialmente, alla fine degli anni ’80 e all’inizio degli anni ’90, è stata testata la monoterapia con NEPI. Candoxatril ha mostrato effetti preliminari promettenti sui parametri emodinamici. Tuttavia, un altro NEPI, l’ecadotril, ha portato a una maggiore mortalità, senza alcuna prova di efficacia clinica rispetto al placebo nei pazienti con insufficienza cardiaca.4,5 Di conseguenza, lo sviluppo della monoterapia con NEPI per l’insufficienza cardiaca è stato interrotto. Successivamente, alcuni studi hanno mostrato l’evidenza di una concomitante attivazione del sistema renina-angiotensina-aldosterone, insieme all’aumento della bioattività del peptide natriuretico. Questi risultati hanno ispirato lo sviluppo e la sperimentazione di agenti che combinano NEPI e attività di inibizione dell’enzima di conversione dell’angiotensina (ACEI), che ha portato ai farmaci noti come inibitori della vasopeptidasi. Sono stati sviluppati diversi inibitori della vasopeptidasi, tra cui omapatrilat, fasidotril, sampatrilat e mixanpril. Dopo numerosi studi, il campo è rimasto molto deluso nello scoprire che l’omapatrilat provocava un numero crescente di episodi clinicamente rilevanti di angioedema.6 Dopo oltre un decennio di peregrinazioni nel deserto, è stato sviluppato un nuovo concetto, la combinazione di NEPI e bloccanti del recettore dell’angiotensina II (ARB), che ha portato a una nuova classe di farmaci chiamati inibitori della neprilisina del recettore dell’angiotensina. Sacubitril/valsartan è un inibitore della neprilisina del recettore dell’angiotensina di prima classe, che ha mostrato risultati migliori del previsto nello studio PARADIGM-HF1 (Figura).
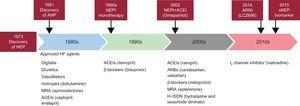
Schema dei punti salienti storici della neprilisina. ACEI, inibitore dell’enzima di conversione dell’angiotensina; ANP, peptide natriuretico atriale; ARB, bloccante del recettore dell’angiotensina II; ARNI, inibitore della neprilisina del recettore dell’angiotensina; HF, insufficienza cardiaca; MRA, antagonista del recettore dei mineralocorticoidi; NEP, neprilisina; NEPI, inibitore della neprilisina; sNEP, neprilisina solubile.
PARADIGM-HF era uno studio multinazionale, randomizzato, in doppio cieco su 8442 pazienti. L’obiettivo era quello di confrontare sacubitril/valsartan con enalapril in pazienti adulti con insufficienza cardiaca cronica (New York Heart Association classe II-IV) e ridotta frazione di eiezione ventricolare sinistra (LVEF ≤ 40%, successivamente modificata a ≤ 35%), in aggiunta ad altra terapia per l’insufficienza cardiaca.1 L’endpoint primario era il composito di morte cardiovascolare o ospedalizzazione per insufficienza cardiaca. Prima della partecipazione allo studio, i pazienti sono stati trattati con la terapia standard di cura, che comprendeva ACEI/ARBs (> 99%), beta-bloccanti (94%), antagonisti mineralocorticoidi (58%) e diuretici (82%). La durata mediana del follow-up è stata di 27 mesi, e i pazienti sono stati trattati fino a 4,3 anni.
I pazienti dovevano interrompere la loro terapia ACEI o ARB esistente ed entrare in un periodo di rodaggio sequenziale, in singolo cieco. Durante il periodo di rodaggio, hanno ricevuto un trattamento con enalapril 10 mg due volte al giorno, seguito da un trattamento in singolo cieco con sacubitril/valsartan 100 mg due volte al giorno, che è stato aumentato a 200 mg due volte al giorno. Sono stati poi randomizzati al periodo in doppio cieco dello studio. Durante questo periodo, hanno ricevuto o sacubitril/valsartan 200 mg o enalapril 10 mg, due volte al giorno. L’età media della popolazione studiata era di 64 anni, e il 19% aveva 75 anni o più. Al momento della randomizzazione, il 70% dei pazienti era in classe NYHA II, il 24% in classe III e lo 0,7% in classe IV. La LVEF media era del 29%, e c’erano 963 (11,4%) pazienti con una LVEF basale > 35% e ≤ 40%. Lo studio è stato terminato prematuramente, a causa delle riduzioni schiaccianti della morte per cause cardiovascolari e della riduzione dell’endpoint primario composito (morte cardiovascolare o ospedalizzazione secondaria a insufficienza cardiaca). Lo studio PARADIGM-HF viene anche chiamato lo studio del 20%, a causa delle riduzioni relative omogenee del ∼20% in tutti gli endpoint studiati, compreso l’endpoint primario composito di morte cardiovascolare, morte cardiaca improvvisa e ospedalizzazione per insufficienza cardiaca (Tabella 1).
SperimentazionePARADIGM-HF: Effetti del trattamento sull’endpoint primario composito, le sue componenti e la mortalità per tutte le cause, In un follow-up medianoup di 27 mesi
| Endpoints | Rapporto di rischio (95%CI) | Riduzione del rischio relativo | P |
|---|---|---|---|
| Endpoint composito primario di morte CV e ricoveri per insufficienza cardiaca | 0.80 (0,73-0,87) | 20% | .0000002 |
| Componenti individuali dell’endpoint primario composito | |||
| morte CV | 0,80 (0,71-0.89) | 20% | .00004 |
| Primo ricovero per insufficienza cardiaca | 0,79 (0,71-0,89) | 21% | .00004 |
| Esito secondario | |||
| Mortalità per tutte le cause | 0,84 (0,76-0,93) | 16% | .0005 |
95%CI, intervallo di confidenza al 95%; CV, cardiovascular-related.
Anche se sacubitril/valsartan ha mostrato un’enorme promessa, ci sono sfide e questioni non affrontate che meritano ulteriori studi e ulteriori chiarimenti (Tabella 2). Alcuni di questi problemi sono stati sollevati e discussi nel rapporto di valutazione dell’Agenzia Europea dei Medicinali su Entresto.7
Sommario dei problemi di sicurezza per Sacubitril/Valsartan
| Rischi importanti identificati | Ipotensione Compromissione renale Iperkalemia Angioedema |
| Rischi potenziali importanti | Epatotossicità Depressione cognitiva Interazione farmaco-statina Trombocitopenia Neutropenia |
| Informazioni mancanti | Pazienti pediatrici con HF Pazienti con grave insufficienza renale Dati a lungo terminedati a lungo termine sull’uso di sacubitril/valsartan nella HF Effetti in pazienti ACEI/ARB-naïve con HF |
ACEI, inibitore dell’enzima di conversione dell’angiotensina; ARB, bloccante del recettore dell’angiotensina II; HF, insufficienza cardiaca.
Modificato dal rapporto di valutazione dell’Agenzia Europea dei Medicinali.7
In primo luogo, quando i pazienti hanno problemi di tollerabilità (per esempio, pressione sanguigna sistolica ≤ 95mmHg, ipotensione sintomatica, iperkaliemia, disfunzione renale), le raccomandazioni attuali sono di adattare i farmaci concomitanti, e/o di ridurre il dosaggio o interrompere temporaneamente il sacubitril/valsartan. Infatti, l’Agenzia Europea dei Medicinali raccomanda che il trattamento non dovrebbe essere iniziato in pazienti con livelli sierici di potassio > 5,4 mmol/L o con pressione sanguigna sistolica
mmHg.
In secondo luogo, i dati sono limitati per i pazienti che attualmente stanno assumendo basse o nessuna dose di ACEI o ARB. Pertanto, le raccomandazioni attuali per questi pazienti sono di iniziare con una dose di 50 mg due volte al giorno e di titolare la dose lentamente (raddoppiando ogni 3-4 settimane).
In terzo luogo, sacubitril/valsartan non deve essere co-somministrato con un ACEI o un ARB. Quando si usa in concomitanza con un ACEI, c’è un alto rischio potenziale di angioedema. Di conseguenza, sacubitril/valsartan non deve essere iniziato per almeno 36 ore dopo l’interruzione della terapia con ACEI.
In quarto luogo, nessun aggiustamento della dose è richiesto nei pazienti con insufficienza renale lieve (tasso di filtrazione glomerulare stimato 60-90mL/min/1.73 m2). Tuttavia, una dose iniziale di 50mg due volte al giorno dovrebbe essere considerata nei pazienti con insufficienza renale moderata (tasso di filtrazione glomerulare stimato 30-60mL/min/1.73 m2). Non ci sono dati su pazienti con malattia renale allo stadio finale, ma l’uso di sacubitril/valsartan non è raccomandato per questi pazienti.
In quinto luogo, si deve esercitare cautela quando si inizia sacubitril/valsartan in pazienti con classificazione funzionale NYHA IV, a causa della limitata esperienza clinica in questa popolazione.
Sesto, BNP non è un biomarcatore adatto di insufficienza cardiaca in pazienti trattati con sacubril/valsartan, perché è un substrato della neprilisina. Si raccomanda il passaggio al NT-proBNP come biomarcatore del peptide natriuretico.
Settimo, un rischio teorico associato all’inibizione della neprilisina è legato all’accumulo del substrato della neprilisina, l’amiloide-β, nel cervello.8 Nello studio PARADIGM-HF non è stato riportato un aumento dell’incidenza di eventi avversi legati alla cognizione o alla demenza. Tuttavia, questi effetti potrebbero non essere stati rilevati fino ad oggi, perché la demenza potrebbe richiedere più tempo per svilupparsi rispetto all’attuale periodo di osservazione dei partecipanti allo studio. Inoltre, non era prevista la partecipazione di soggetti con demenza lieve. Tuttavia, lo studio di fase III PARAGON-HF in corso ha implementato una valutazione della funzione cognitiva.
In ottavo luogo, la co-somministrazione di sacubitril/valsartan e atorvastatina ha aumentato la Cmax di atorvastatina e dei suoi metaboliti fino a 2 volte. Non ci sono stati aumenti significativi dei potenziali eventi avversi legati alla statina nei pazienti che hanno ricevuto sia sacubitril/valsartan che la statina nello studio PARADIGM-HF. Tuttavia, ulteriori analisi hanno dimostrato che dosi più elevate di statine erano associate a un maggior numero di eventi avversi, quando combinate con sacubitril/valsartan o enalapril. Tuttavia, i modelli erano diversi, a seconda della statina specifica somministrata. In attesa dei risultati di ulteriori studi, è stata raccomandata cautela per questa combinazione di farmaci.7
Lo studio PARADIGM-HF è incentrato sull’insufficienza cardiaca cronica con LVEF limitata. Quindi, la domanda sorge spontanea: Che dire dell’altro 50% di pazienti con insufficienza cardiaca, ma frazione di eiezione conservata, noti anche come pazienti HFpEF? Attualmente, c’è una mancanza di studi clinici su HFpEF che ha dimostrato benefici terapeutici con agenti comunemente utilizzati in pazienti con frazione di eiezione ridotta. Di conseguenza, le terapie per l’HFpEF sono dirette alla gestione dei sintomi e dei fattori di rischio cardiovascolare. Tuttavia, tra i pazienti con HFpEF, sacubitril/valsartan ha mostrato risultati di sicurezza ed efficacia promettenti in uno studio di fase 2. Lo studio PARAMOUNT era uno studio randomizzato, in doppio cieco, a gruppi paralleli, a controllo attivo, che confrontava sacubitril/valsartan con il solo valsartan.9 L’endpoint primario era un cambiamento dal basale nell’NT-proBNP a 12 settimane. I gruppi avevano caratteristiche basali simili. La maggior parte dei pazienti erano anziani, di sesso femminile, in sovrappeso e classificati in classe NYHA II. Una maggiore riduzione di NT-proBNP è stata rilevata alla settimana 4 nel gruppo sacubitril/valsartan rispetto al gruppo valsartan, ma non ha raggiunto la significatività (P = .063). A 12 settimane, NT-proBNP era significativamente ridotto nel gruppo sacubitril/valsartan rispetto al valsartan (P = .005). I risultati di PARAMOUNT hanno suggerito che sacubitril/valsartan potrebbe avere effetti favorevoli nei pazienti con HFpEF. Ulteriori indagini sulla popolazione HFpEF sono in corso nello studio PARAGON, uno studio multicentrico, randomizzato, in doppio cieco, a gruppi paralleli, controllato attivamente. Questo studio mira a valutare l’efficacia e la sicurezza di sacubitril/valsartan rispetto al valsartan sulla morbilità e la mortalità nei pazienti con insufficienza cardiaca (classe NYHA II-IV) e frazione di eiezione preservata.
Infine, ma non meno importante, molto recentemente, la neprilisina solubile circolante (sNEP) è stata proposta come biomarcatore putativo.2 Attualmente, i dati su sNEP hanno suggerito che può svolgere un ruolo prognostico sia nell’insufficienza cardiaca cronica10 che in quella acutamente scompensata,11 ma nell’HFpEF i risultati sono controversi.12 È interessante notare che la sNEP circolante ha dimostrato di essere cataliticamente attiva.13 Inoltre, un rapporto recente ha dimostrato che sNEP potrebbe persino essere superiore a NT-proBNP come biomarcatore prognostico surrogato dell’asse neuro-ormonale nell’insufficienza cardiaca.14 Ulteriori perfezionamenti nei test sNEP sono obbligatori prima della sua introduzione nella pratica clinica. Tuttavia, i dati riportati fino ad oggi suggeriscono che potrebbe diventare uno strumento prezioso per la prognostica del paziente ed eventualmente la guida della terapia.
Come epilogo, il costo del trattamento con questo nuovo agente rappresenta probabilmente una barriera al suo utilizzo nella pratica clinica quotidiana della vita reale, poiché il costo di agenti efficaci come l’ACEI enalapril è molto basso (paragonabile al costo della gomma da masticare in molti paesi). Concepibilmente, l’implementazione di una strategia guidata da biomarcatori può essere proposta per passare preferenzialmente dal trattamento con ACEI a Entresto nei pazienti più malati. Su questa linea, è degno di nota che l’uso dei peptidi natriuretici era tra i criteri di inclusione nello studio PARADIGM-HF. Il rapporto costo-efficacia e il costo per anno di vita aggiunto alla qualità guadagnato di sacubitril/valsartan rispetto all’enalapril per il trattamento dell’HFrEF meritano una ricerca intensiva in scenari del mondo reale adeguati per paese e sistema sanitario.15
CONFLITTI DI INTERESSE
A. Bayes-Genis e J. Lupón hanno richiesto un brevetto per sNEP come biomarcatore prognostico, che è in attesa di approvazione. A. Bayes-Genis ha tenuto conferenze e ha partecipato a comitati consultivi di Novartis.
.