Ci sono molte modalità diverse che possono essere utilizzate per l’imaging molecolare non invasivo. Ognuno ha i suoi diversi punti di forza e di debolezza e alcuni sono più abili nell’imaging di obiettivi multipli rispetto ad altri.
Risonanza magnetica

La risonanza magnetica ha il vantaggio di avere una risoluzione spaziale molto alta ed è molto abile nell’imaging morfologico e funzionale. La risonanza magnetica ha però diversi svantaggi. In primo luogo, la MRI ha una sensibilità di circa 10-3 mol/L a 10-5 mol/L che, rispetto ad altri tipi di imaging, può essere molto limitante. Questo problema deriva dal fatto che la differenza tra gli atomi nello stato di alta energia e nello stato di bassa energia è molto piccola. Per esempio, a 1,5 Tesla, un’intensità di campo tipica per la risonanza magnetica clinica, la differenza tra gli stati di alta e bassa energia è di circa 9 molecole su 2 milioni. I miglioramenti per aumentare la sensibilità della risonanza magnetica includono l’aumento dell’intensità del campo magnetico e l’iperpolarizzazione tramite il pompaggio ottico, la polarizzazione nucleare dinamica o la polarizzazione indotta dal parahydrogen. Ci sono anche una varietà di schemi di amplificazione del segnale basati sullo scambio chimico che aumentano la sensibilità.
Per ottenere l’imaging molecolare dei biomarcatori delle malattie usando la risonanza magnetica, sono necessari agenti di contrasto mirati con alta specificità e alta relaxività (sensibilità). Ad oggi, molti studi sono stati dedicati allo sviluppo di agenti di contrasto MRI mirati per ottenere l’imaging molecolare tramite MRI. Comunemente, peptidi, anticorpi, o piccoli ligandi, e piccoli domini proteici, come gli affibbi HER-2, sono stati applicati per ottenere il targeting. Per aumentare la sensibilità degli agenti di contrasto, queste società di targeting sono solitamente collegate ad agenti di contrasto MRI ad alto carico utile o ad agenti di contrasto MRI con alta rilassatezza. In particolare, il recente sviluppo di particelle di dimensioni micron di ossido di ferro (MPIO) ha permesso di raggiungere livelli senza precedenti di sensibilità per rilevare le proteine espresse da arterie e vene.
Optical imagingModifica
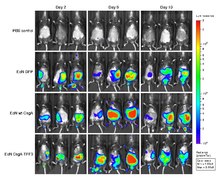
Ci sono diversi approcci utilizzati per l’imaging ottico. I vari metodi dipendono dalla fluorescenza, dalla bioluminescenza, dall’assorbimento o dalla riflettanza come fonte di contrasto.
L’attributo più prezioso dell’imaging ottico è che esso e gli ultrasuoni non hanno forti problemi di sicurezza come le altre modalità di imaging medico.
Lo svantaggio dell’imaging ottico è la mancanza di profondità di penetrazione, specialmente quando si lavora a lunghezze d’onda visibili. La profondità di penetrazione è legata all’assorbimento e alla dispersione della luce, che è principalmente una funzione della lunghezza d’onda della sorgente di eccitazione. La luce viene assorbita dai cromofori endogeni che si trovano nei tessuti viventi (per esempio emoglobina, melanina e lipidi). In generale, l’assorbimento e la dispersione della luce diminuiscono con l’aumentare della lunghezza d’onda. Al di sotto di ~700 nm (ad esempio le lunghezze d’onda visibili), questi effetti si traducono in profondità di penetrazione di pochi millimetri. Quindi, nella regione visibile dello spettro, è possibile solo una valutazione superficiale delle caratteristiche del tessuto. Sopra i 900 nm, l’assorbimento dell’acqua può interferire con il rapporto segnale-sfondo. Poiché il coefficiente di assorbimento del tessuto è notevolmente inferiore nella regione del vicino infrarosso (NIR) (700-900 nm), la luce può penetrare più profondamente, a profondità di diversi centimetri.
Imaging nel vicino infrarossoModifica
Sonde ed etichette fluorescenti sono uno strumento importante per l’imaging ottico. Alcuni ricercatori hanno applicato l’imaging NIR nel modello di ratto di infarto miocardico acuto (AMI), utilizzando una sonda peptidica che può legarsi alle cellule apoptotiche e necrotiche. Un certo numero di fluorofori nel vicino infrarosso (NIR) sono stati impiegati per l’imaging in vivo, tra cui Kodak X-SIGHT Dyes and Conjugates, Pz 247, DyLight 750 e 800 Fluors, Cy 5.5 e 7 Fluors, Alexa Fluor 680 e 750 Dyes, IRDye 680 e 800CW Fluors. I punti quantici, con la loro fotostabilità ed emissioni luminose, hanno generato un grande interesse; tuttavia, le loro dimensioni precludono un’efficiente clearance dal sistema circolatorio e renale, mentre mostrano una tossicità a lungo termine.
Diversi studi hanno dimostrato l’uso di sonde marcate con coloranti infrarossi nell’imaging ottico.
- In un confronto tra scintigrafia gamma e imaging NIR, un ciclopentapeptide marcato con 111
In e un fluoroforo NIR è stato usato per l’immagine di xenotrapianti di melanoma αvβ3-integrina positivi. - L’RGD marcato nel vicino infrarosso che punta all’αvβ3-integrina è stato usato in numerosi studi per colpire una varietà di tumori.
- Un fluoroforo NIR è stato coniugato al fattore di crescita epidermico (EGF) per l’imaging della progressione tumorale.
- Un fluoroforo NIR è stato confrontato con Cy5.5, suggerendo che i coloranti a lunghezza d’onda più lunga possono produrre agenti di targeting più efficaci per l’imaging ottico.
- Pamidronato è stato etichettato con un fluoroforo NIR e usato come agente di imaging osseo per rilevare l’attività osteoblastica in un animale vivo.
- Un GPI marcato con un fluoroforo NIR, un potente inibitore del PSMA (antigene di membrana specifico della prostata).
- Uso di albumina di siero umano marcata con un fluoroforo NIR come agente di tracciamento per la mappatura dei linfonodi sentinella.
- 2-Deossi-D-glucosio marcato con un fluoroforo NIR.
È importante notare che l’aggiunta di una sonda NIR a qualsiasi vettore può alterare la biocompatibilità e la biodistribuzione del vettore. Pertanto, non si può assumere inequivocabilmente che il vettore coniugato si comporterà in modo simile alla forma nativa.
Tomografia computerizzata a emissione di fotoniModifica
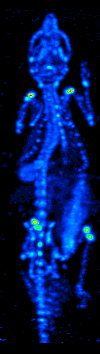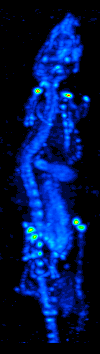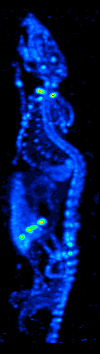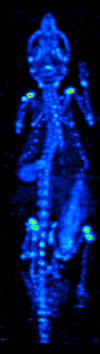
Lo sviluppo della tomografia computerizzata negli anni 70 ha permesso la mappatura della distribuzione dei radioisotopi nell’organo o nel tessuto, e ha portato alla tecnica ora chiamata tomografia computerizzata a emissione di fotoni singoli (SPECT).
L’agente di imaging usato nella SPECT emette raggi gamma, al contrario degli emettitori di positroni (come il 18
F) usati nella PET. Esiste una gamma di radiotraccianti (come 99m
Tc, 111
In, 123
I, 201
Tl) che possono essere usati, a seconda dell’applicazione specifica.
Il gas xeno (133
Xe) è uno di questi radiotraccianti. Ha dimostrato di essere prezioso per studi diagnostici di inalazione per la valutazione della funzione polmonare; per l’imaging dei polmoni; e può anche essere usato per valutare il rCBF. Il rilevamento di questo gas avviene tramite una gamma camera, che è un rivelatore a scintillazione composto da un collimatore, un cristallo NaI e una serie di tubi fotomoltiplicatori.
Rotando la gamma camera intorno al paziente, un’immagine tridimensionale della distribuzione del radiotracciante può essere ottenuta utilizzando la retroproiezione filtrata o altre tecniche tomografiche.I radioisotopi usati nella SPECT hanno emivite relativamente lunghe (da poche ore a pochi giorni) che li rendono facili da produrre e relativamente economici. Questo rappresenta il principale vantaggio della SPECT come tecnica di imaging molecolare, dal momento che è significativamente più economico di PET o fMRI. Tuttavia manca una buona risoluzione spaziale (cioè, dove si trova esattamente la particella) o temporale (cioè, il segnale del mezzo di contrasto è avvenuto in questo millisecondo o in quel millisecondo). Inoltre, a causa della radioattività dell’agente di contrasto, ci sono aspetti di sicurezza riguardanti la somministrazione di radioisotopi al soggetto, soprattutto per studi seriali.
Tomografia a emissione di positroniModifica
Play media
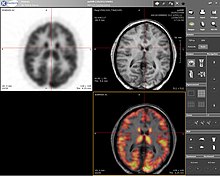
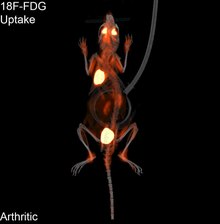
La tomografia a emissione di positroni (PET) è una tecnica di imaging della medicina nucleare che produce un’immagine tridimensionale o un quadro dei processi funzionali nel corpo. La teoria dietro la PET è abbastanza semplice. Per prima cosa una molecola viene etichettata con un isotopo che emette positroni. Questi positroni si annichilano con gli elettroni vicini, emettendo due fotoni da 511 keV, diretti a 180 gradi in direzioni opposte. Questi fotoni sono poi rilevati dallo scanner, che può stimare la densità delle annichilazioni di positroni in un’area specifica. Quando si sono verificate abbastanza interazioni e annichilazioni, la densità della molecola originale può essere misurata in quell’area. Gli isotopi tipici includono 11
C, 13
N, 15
O, 18
F, 64
Cu, 62
Cu, 124
I, 76
Br, 82
Rb, 89
Zr e 68
Ga, con 18
F che è il più utilizzato clinicamente. Uno dei maggiori svantaggi della PET è che la maggior parte delle sonde deve essere realizzata con un ciclotrone. La maggior parte di queste sonde ha anche un’emivita misurata in ore, costringendo il ciclotrone ad essere sul posto. Questi fattori possono rendere la PET proibitivamente costosa. L’imaging PET ha però molti vantaggi. Il primo e più importante è la sua sensibilità: un tipico scanner PET può rilevare concentrazioni comprese tra 10-11 mol/L e 10-12 mol/L.