La solfonazione del metilbenzene
Il metilbenzene è più reattivo del benzene a causa della tendenza del gruppo metile a “spingere” gli elettroni verso l’anello.
L’effetto di questa maggiore reattività è che il metilbenzene reagirà con l’acido solforico fumante a 0°C, e con l’acido solforico concentrato se vengono riscaldati sotto riflusso per circa 5 minuti.
Oltre all’effetto sulla velocità di reazione, con il metilbenzene bisogna anche pensare a dove il gruppo acido solfonico finisce sull’anello rispetto al gruppo metile. I gruppi metilici hanno la tendenza a “dirigere” nuovi gruppi nelle posizioni 2- e 4- dell’anello (supponendo che il gruppo metilico sia in posizione 1-). I gruppi metilici sono detti 2,4-dirigenti.
Così si ottiene una miscela che consiste principalmente di due isomeri. Solo il 5-10% circa dell’isomero 3 si forma. Le reazioni principali sono:
![]()
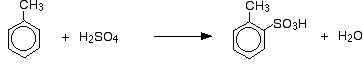
e:
![]()
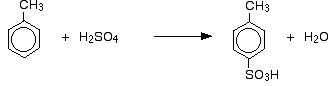
Nel caso della solfonazione, la proporzione esatta degli isomeri formati dipende dalla temperatura della reazione. All’aumentare della temperatura, si ottengono proporzioni crescenti dell’isomero 4- e meno dell’isomero 2-. Questo perché la solfonazione è reversibile. Il gruppo acido solfonico può staccarsi nuovamente dall’anello e riattaccarsi da qualche altra parte. Questo tende a favorire la formazione dell’isomero più stabile termodinamicamente. Questo scambio avviene di più a temperature più alte.
L’isomero 4- è più stabile perché non c’è ingombro nella molecola come ci sarebbe se il gruppo metile e il gruppo acido solfonico fossero uno accanto all’altro.