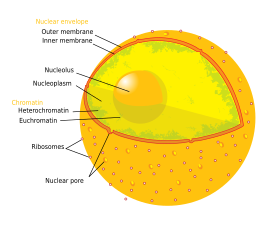
A sejtmag tartalmazza a sejt csaknem teljes DNS-ét, amelyet rostos köztes filamentumok hálózata vesz körül, és amelyet egy kettős membrán, az úgynevezett “magburkolat” vesz körül. A magburkolat választja el a sejtmag belsejében lévő folyadékot, az úgynevezett nukleoplazmát a sejt többi részétől. A sejtmag mérete a benne lévő sejt méretétől függ, a sejtmag jellemzően a teljes sejttérfogat mintegy 8%-át foglalja el. A sejtmag az állati sejtek legnagyobb organellája. 12 Az emlősök sejtjeiben a sejtmag átlagos átmérője körülbelül 6 mikrométer (µm).
Nukleáris burok és pórusok

A magburkot két membrán, egy belső és egy külső magmembrán alkotja:649 Ezek a membránok együttesen a sejt genetikai anyagának a sejt többi tartalmától való elkülönítését szolgálják, és lehetővé teszik, hogy a sejtmag a sejt többi részétől elkülönülő környezetet tartson fenn. Annak ellenére, hogy a sejtmag nagy része körül szorosan egymás mellett helyezkednek el, a két membrán alakja és tartalma jelentősen különbözik egymástól. A belső membrán körülveszi a sejtmag tartalmát, biztosítva annak meghatározó peremét.:14 A belső membránba ágyazva különböző fehérjék kötik meg a sejtmag szerkezetét adó köztes filamentumokat.:649 A külső membrán körülveszi a belső membránt, és folytonos a szomszédos endoplazmatikus retikulum membránjával.:649 Az endoplazmatikus retikulum membránjának részeként a külső magmembrán riboszómákkal van tele, amelyek aktívan fordítják a fehérjéket a membránon keresztül.:649 A két membrán közötti tér, az úgynevezett “perinukleáris tér” folyamatos az endoplazmatikus retikulum lumenével.:649
A nukleáris pórusok, amelyek vizes csatornákat biztosítanak a burkon keresztül, több fehérjéből állnak, amelyeket együttesen nukleoporinoknak neveznek. A pórusok molekulatömege körülbelül 60-80 millió dalton, és körülbelül 50 (élesztőben) és több száz fehérjéből (gerincesekben) állnak.:622-4 A pórusok teljes átmérője 100 nm, azonban a rés, amelyen keresztül a molekulák szabadon diffundálnak, csak körülbelül 9 nm széles, ami a pórus közepén található szabályozó rendszerek jelenlétének köszönhető. Ez a méret szelektíven lehetővé teszi a kis vízben oldódó molekulák áthaladását, miközben megakadályozza a nagyobb molekulák, például a nukleinsavak és a nagyobb fehérjék nem megfelelő be- vagy kilépését a sejtmagba. Ehelyett ezeket a nagy molekulákat aktívan kell a magba szállítani. Egy tipikus emlőssejt sejtmagjának burkában körülbelül 3000-4000 pórus található, amelyek mindegyike egy nyolcszorosan szimmetrikus, gyűrű alakú szerkezetet tartalmaz azon a helyen, ahol a belső és a külső membrán összeolvad. A gyűrűhöz kapcsolódik egy nukleáris kosárnak nevezett szerkezet, amely a nukleoplazmába nyúlik, valamint egy sor rostos nyúlvány, amelyek a citoplazmába nyúlnak. Mindkét struktúra a nukleáris transzportfehérjékhez való kötődés közvetítésére szolgál.:509-10
A legtöbb fehérje, riboszómális alegység és néhány RNS a póruskomplexeken keresztül a karyopherineknek nevezett transzportfaktorok családja által közvetített folyamat során szállítódik. Azokat a karyopherineket, amelyek a sejtmagba történő mozgást közvetítik, importinoknak is nevezik, míg azokat, amelyek a sejtmagból történő mozgást közvetítik, exportinoknak. A legtöbb karyopherin közvetlenül lép kölcsönhatásba rakományával, bár egyesek adaptorfehérjéket használnak. Az olyan szteroid hormonok, mint a kortizol és az aldoszteron, valamint más, a sejtek közötti jelátvitelben részt vevő kis, lipidben oldódó molekulák képesek a sejtmembránon keresztül a citoplazmába diffundálni, ahol nukleáris receptorfehérjékhez kötődnek, amelyek a sejtmagba szállítódnak. Ott ligandjukhoz kötődve transzkripciós faktorokként szolgálnak; ligand hiányában sok ilyen receptor hiszton-deacetilázként működik, amely elnyomja a génexpressziót.:488
Nukleáris lamina
Az állati sejtekben két köztes filamentumhálózat biztosítja a sejtmag mechanikai támaszát: A maglamina szervezett hálót alkot a burok belső oldalán, míg a kevésbé szervezett támaszt a burok citoszolikus oldalán. Mindkét rendszer strukturális támaszt nyújt a magburoknak, valamint rögzítési helyeket a kromoszómák és a nukleáris pórusok számára.
A nukleáris lamina nagyrészt lamin fehérjékből áll. Mint minden fehérje, a laminok is a citoplazmában szintetizálódnak, majd a sejtmag belsejébe szállítódnak, ahol összeállnak, mielőtt beépülnek a nukleáris lamina meglévő hálózatába. A membrán citoszolikus oldalán található laminok, mint például az emerin és a nesprin, a citoszkeletonhoz kötődnek, hogy strukturális támaszt nyújtsanak. A laminok a nukleoplazma belsejében is megtalálhatók, ahol egy másik szabályos struktúrát, az úgynevezett nukleoplazmatikus fátylat alkotják, amely fluoreszcens mikroszkópiával látható. A fátyol tényleges funkciója nem világos, bár a nukleoluszból kizáródik, és az interfázis alatt jelen van. A fátylat alkotó lamin struktúrák, mint például a LEM3, kötik a kromatint, és szerkezetük megbontása gátolja a fehérjéket kódoló gének transzkripcióját.
A többi intermedier filamentum összetevőihez hasonlóan a lamin monomer tartalmaz egy alfa-hélix domént, amelyet két monomer arra használ, hogy egymás köré tekeredjen, egy dimer szerkezetet, úgynevezett tekercset alkotva. Két ilyen dimer szerkezet aztán egymás mellett, antiparallel elrendeződésben csatlakozik, hogy egy protofilamentumnak nevezett tetramert alkosson. Ezekből a protofilamentumokból nyolc alkot oldalirányú elrendeződést, amelyek csavarodva kötélszerű filamentumot alkotnak. Ezek a filamentumok dinamikusan tudnak összeállni vagy szétszerelődni, ami azt jelenti, hogy a filamentum hosszának változása a filamentumok hozzáadásának és eltávolításának versengő sebességétől függ.
A lamin génekben bekövetkező, a filamentumok összeállásának hibájához vezető mutációk a ritka genetikai rendellenességek egy csoportját, az úgynevezett laminopátiákat okozzák. A legjelentősebb laminopátia a progéria néven ismert betegségcsalád, amely a korai öregedés megjelenését okozza az érintettekben. A pontos mechanizmus, amellyel a társuló biokémiai változások az öregedő fenotípust előidézik, nem jól ismert.
Kromoszómák
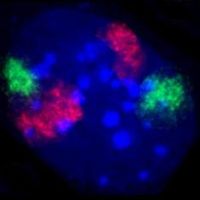
A sejtmag a sejt genetikai anyagának nagy részét többszörös lineáris DNS-molekulák formájában tartalmazza, amelyek kromoszómáknak nevezett struktúrákba szerveződnek. Minden emberi sejt nagyjából két méternyi DNS-t tartalmaz.405 A sejtciklus nagy részében ezek egy kromatin nevű DNS-fehérje komplexbe szerveződnek, és a sejtosztódás során a kromatin láthatóan a kariotípusból ismert, jól körülhatárolt kromoszómákat alkotja. A sejt génjeinek egy kis része ehelyett a mitokondriumokban található.:438
A kromatinnak két típusa van. Az euchromatin a DNS kevésbé kompakt formája, és olyan géneket tartalmaz, amelyeket a sejt gyakran expresszál. A másik típus, a heterokromatin a kompaktabb forma, és olyan DNS-t tartalmaz, amelyet ritkán írnak át. Ezt a struktúrát tovább kategorizáljuk fakultatív heterokromatinra, amely olyan génekből áll, amelyek csak bizonyos sejttípusokban vagy a fejlődés bizonyos szakaszaiban szerveződnek heterokromatinná, és konstitutív heterokromatinra, amely olyan kromoszóma szerkezeti elemekből áll, mint a telomerek és centromerek. Az interfázis során a kromatin diszkrét egyedi foltokká, úgynevezett kromoszóma-területekké szerveződik. Az aktív gének, amelyek általában a kromoszóma euchromatikus régiójában találhatók, általában a kromoszóma territóriumhatára felé helyezkednek el.
A kromatinszerveződés bizonyos típusai, különösen a nukleoszómák elleni antitesteket számos autoimmun betegséggel, például a szisztémás lupus erythematosussal hozták összefüggésbe. Ezek az antinukleáris antitestek (ANA) néven ismertek, és a szklerózis multiplexszel együtt is megfigyelték őket az immunrendszer általános működési zavarának részeként.
Nukleolus

A nukleolus a legnagyobb a sejtmagban található diszkrét, sűrűn festett, membrán nélküli struktúrák, az úgynevezett magtestek közül. Az rDNS, a riboszomális RNS-t (rRNS) kódoló DNS tandem ismétlődései körül alakul ki. Ezeket a régiókat nukleoláris szervező régióknak (NOR) nevezik. A nukleolus fő szerepe az rRNS szintézise és a riboszómák összeszerelése. A nukleolus szerkezeti kohéziója a nukleolus aktivitásától függ, mivel a riboszómák összeszerelése a nukleolusban a nukleoláris komponensek átmeneti asszociációját eredményezi, ami megkönnyíti a további riboszóma-összeszerelést, és ezáltal a további asszociációt. Ezt a modellt támasztják alá azok a megfigyelések, hogy az rDNS inaktiválása a nukleoláris struktúrák összekeveredését eredményezi.
A riboszóma-összeszerelés első lépésében az RNS-polimeráz I nevű fehérje átírja az rDNS-t, amely egy nagy pre-rRNS prekurzort alkot. Ezt két nagy rRNS alegységre – 5,8S, és 28S – és egy kis rRNS alegységre, a 18S-re hasítják. 328 Az rRNS átírása, poszt-transzkripciós feldolgozása és összeszerelése a nukleoluszban történik, amit kis nukleoláris RNS (snoRNS) molekulák segítenek, amelyek közül néhány a riboszóma működésével kapcsolatos géneket kódoló hírvivő RNS-ek spliced intronjaiból származik. Az összerakott riboszóma alegységek a legnagyobb szerkezetek, amelyek áthaladnak a nukleáris pórusokon.:526
Elektronmikroszkópos megfigyeléskor látható, hogy a nukleolus három jól elkülöníthető régióból áll: a legbelső fibrilláris központok (FC), amelyeket a sűrű fibrilláris komponens (DFC) vesz körül (amely fibrillarint és nukleolint tartalmaz), amelyet viszont a granuláris komponens (GC) határol (amely a nukleofoszmin fehérjét tartalmazza). Az rDNS transzkripciója vagy az FC-ben, vagy az FC-DFC határon történik, és ezért, ha a sejtben az rDNS transzkripciója fokozódik, több FC-t észlelünk. Az rRNS-ek hasításának és módosításának nagy része a DFC-ben történik, míg az utóbbi, a riboszómális alegységekre történő fehérje-összeszereléssel járó lépések a GC-ben történnek.
Más magtestek
| Szerkezet neve | Szerkezet átmérője | Ref. |
|---|---|---|
| Cajal testek | 0,2-2,0 µm | |
| Klasztoszómák | 0,2-0.5 µm | |
| PIKA | 5 µm | |
| PML testek | 0.2-1.0 µm | |
| Paraspeckles | 0.5-1,0 µm | |
| Speckles | 20-25 nm |
A magmagban a nukleolusz mellett számos más magtest is található. Ezek közé tartoznak a Cajal-testek, a Gemini of Cajal-testek, a polimorf interfázisú karyoszóma-asszociáció (PIKA), a promyelocita leukémia (PML) testek, a paraspeckle és a splicing speckle. Bár számos ilyen doménről keveset tudunk, mégis jelentősek, mivel azt mutatják, hogy a nukleoplazma nem egységes keverék, hanem szervezett funkcionális szubdoméneket tartalmaz.
Más szubnukleáris struktúrák kóros betegségfolyamatok részeként jelennek meg. Például kis intranukleáris pálcikák jelenlétéről számoltak be a nemalin myopathia egyes eseteiben. Ez az állapot jellemzően az aktin mutációjának következménye, és maguk a pálcikák mutáns aktinból, valamint más citoszkeletális fehérjékből állnak.
Cajal-testek és drágakövek
A sejtmagban jellemzően egy és tíz közötti kompakt struktúra található, amelyeket Cajal-testeknek vagy tekervényes testeknek (CB) neveznek, és amelyek átmérője 0,2 µm és 2,0 µm között van sejttípustól és fajtól függően. Elektronmikroszkóp alatt vizsgálva ezek a gömbök kusza fonalakra hasonlítanak, és a coilin nevű fehérje sűrű eloszlási gócai. A CB-k számos különböző szerepben vesznek részt az RNS-feldolgozással kapcsolatban, különösen a kis nukleoláris RNS (snoRNS) és a kis nukleáris RNS (snRNS) érlelésében, valamint a hiszton mRNS módosításában.
A Cajal-testekhez hasonlóak a Gemini of Cajal-testek, vagy gemmák, amelyek neve az Ikrek csillagképről származik, utalva a CB-kkel való szoros “iker” kapcsolatukra. A drágakövek méretükben és alakjukban hasonlóak a CB-khez, sőt, mikroszkóp alatt gyakorlatilag megkülönböztethetetlenek. A CB-ktől eltérően az ékkövek nem tartalmaznak kis nukleáris ribonukleoproteineket (snRNP-ket), de tartalmaznak egy SMN (survival of motor neuron) nevű fehérjét, amelynek funkciója az snRNP biogeneziséhez kapcsolódik. Úgy gondolják, hogy a drágakövek segítik a CB-ket az snRNP biogenezisében, bár mikroszkópos bizonyítékok alapján azt is feltételezik, hogy a CB-k és a drágakövek ugyanazon struktúra különböző megnyilvánulásai. Későbbi ultrastrukturális vizsgálatok azt mutatták, hogy a gems a Cajal-testek ikrei, a különbség a coilin komponensben van; a Cajal-testek SMN pozitívak és coilin pozitívak, a gems pedig SMN pozitív és coilin negatív.
PIKA és PTF domének
A PIKA doméneket, vagy polimorf interfázisú karyoszóma társulásokat először 1991-ben írták le mikroszkópos vizsgálatokban. Funkciójuk továbbra is tisztázatlan, bár úgy gondolták, hogy nem kapcsolódnak aktív DNS-replikációhoz, transzkripcióhoz vagy RNS-feldolgozáshoz. Úgy találták, hogy gyakran társulnak a kis nukleáris RNS (snRNS) átírását elősegítő PTF transzkripciós faktor sűrű lokalizációja által meghatározott diszkrét doménekhez.
PML-testek
A PML-testek (PML-testek) a nukleoplazmában elszórtan található gömb alakú, körülbelül 0,1-1,0 µm méretű testek. Számos más néven is ismertek, többek között nukleáris domén 10 (ND10), Kremer-testek és PML onkogén domének. A PML-testek az egyik fő komponensükről, a promielocitás leukémiás fehérjéről (PML) kapták a nevüket. Gyakran láthatók a sejtmagban a Cajal-testekkel és a hasadótestekkel együtt. A PML-testek létrehozására képtelen Pml-/- egerek normálisan, nyilvánvaló káros hatások nélkül fejlődnek, ami azt mutatja, hogy a PML-testek nem szükségesek a legtöbb alapvető biológiai folyamathoz.
Splicing speckles
A speckles olyan szubnukleáris struktúrák, amelyek pre-messenger RNS splicing faktorokban gazdagodnak, és az emlős sejtek nukleoplazmájának interkromatin régióiban helyezkednek el. Fluoreszcencia-mikroszkópos szinten szabálytalan, pontszerű struktúrákként jelennek meg, amelyek mérete és alakja változó, elektronmikroszkópos vizsgálat során pedig interkromatin granulumok csoportjaiként jelennek meg. A pöttyök dinamikus struktúrák, és mind fehérje-, mind RNS-fehérje komponenseik folyamatosan ciklizálhatnak a pöttyök és más nukleáris helyek, köztük az aktív transzkripciós helyek között. A speckle-k összetételének, szerkezetének és viselkedésének tanulmányozása modellel szolgált a sejtmag funkcionális kompartmentalizációjának és a génexpressziós gépezet szerveződésének megértéséhez, amely az snRNP-ket és más, a pre-mRNS feldolgozásához szükséges splicing-fehérjéket splicingeli. A sejt változó igényei miatt e testek összetétele és elhelyezkedése az mRNS-átírásnak és a specifikus fehérjék foszforilációján keresztül történő szabályozásnak megfelelően változik. A splicing speckles más néven nukleáris speckles (nukleáris speckles), splicing factor compartments (SF compartments), interchromatin granule clusters (IGCs) és B snurposomák. b snurposomák a kétéltűek petesejtmagjaiban és a Drosophila melanogaster embrióiban találhatók. A B snurposzómák a kétéltűmagok elektronmikroszkópos felvételein önmagukban vagy a Cajal-testekhez kapcsolódva jelennek meg. Az IGC-k a splicing faktorok tárolóhelyeiként funkcionálnak.
Paraspeckles
A 2002-ben Fox et al. által felfedezett paraspeckle-k szabálytalan alakú rekeszek a sejtmag interchromatin terében. Először a HeLa sejtekben dokumentálták, ahol általában 10-30 van sejtmagonként, de ma már ismert, hogy a paraspeckle-k minden humán primer sejtben, transzformált sejtvonalakban és szöveti metszetekben is léteznek. Nevüket a sejtmagban való eloszlásukról kapták; a “para” a párhuzamos rövidítése, a “speckles” pedig a splicing speckles-re utal, amelyekhez mindig közel vannak.
A paraspekklok magfehérjéket és RNS-t szekvenálnak, és így úgy tűnik, hogy molekuláris szivacsként működnek, amely részt vesz a génexpresszió szabályozásában. A paraspeckle-ek továbbá dinamikus struktúrák, amelyek a sejtek metabolikus aktivitásának változásaira reagálva módosulnak. Transzkripciófüggőek, és az RNS Pol II transzkripció hiányában a paraspeckle eltűnik, és az összes kapcsolódó fehérjekomponens (PSP1, p54nrb, PSP2, CFI(m)68 és PSF) félhold alakú perinukleoláris sapkát alkot a nukleoluszban. Ez a jelenség a sejtciklus során kimutatható. A sejtciklusban a paraspeckle az interfázisban és a mitózis minden szakaszában jelen van, kivéve a telofázist. A telofázis alatt, amikor a két leánymag kialakul, nincs RNS Pol II transzkripció, így a fehérjekomponensek ehelyett perinukleoláris sapkát képeznek.
Perikromatin fibrillumok
A perikromatin fibrillumok csak elektronmikroszkóp alatt láthatók. A transzkripcionálisan aktív kromatin mellett helyezkednek el, és feltételezhetően az aktív pre-mRNS-feldolgozás helyszínei.
Klastoszómák
A klastoszómák kis magtestek (0,2-0,5 µm), amelyeket az e testeket körülvevő perifériás kapszula miatt vastag gyűrű alakúnak írnak le. Ez az elnevezés a görög klastosz, tört és soma, test szóból származik. A klasztoszómák jellemzően nincsenek jelen a normális sejtekben, ezért nehéz kimutatni őket. Magas proteolitikus körülmények között alakulnak ki a sejtmagban, és lebomlanak, amint csökken az aktivitásuk, vagy ha a sejteket proteaszóma-inhibitorokkal kezelik. A klasztoszómák ritkasága a sejtekben arra utal, hogy a proteaszóma működéséhez nincs rájuk szükség. Kimutatták, hogy az ozmotikus stressz is klasztoszómák képződését okozza. Ezek a magtestek a proteaszóma katalitikus és szabályozó alegységeit és szubsztrátjait tartalmazzák, ami arra utal, hogy a klasztoszómák a fehérjék lebontásának helyszínei.