Hírlevél
2020. december 28., hétfő
A NIH és a BARDA által finanszírozott vizsgálatba legfeljebb 30 000 önkéntes jelentkezését várják.
A vizsgálatban való részvétel iránt érdeklődő 18 éves vagy idősebb személyek a coronaviruspreventionnetwork.org, a ClinicalTrials.gov és az NCT04611802 azonosítóra való keresés, vagy a Novavax.com/PREVENT-19 oldalon találnak részleteket. Kérjük, ne keresse a NIAID médiatelefonszámát vagy e-mail címét, hogy jelentkezzen erre a vizsgálatra.
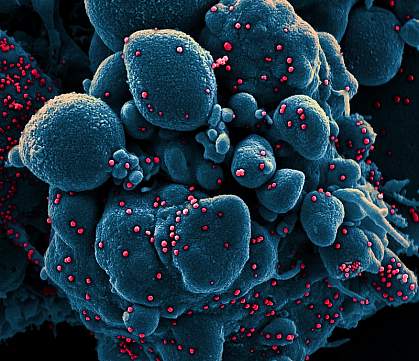 Egy betegmintából izolált, SARS-COV-2 vírusrészecskékkel (piros) fertőzött apoptotikus sejt (kék) színezett pásztázó elektronmikroszkópos felvétele.NIAID
Egy betegmintából izolált, SARS-COV-2 vírusrészecskékkel (piros) fertőzött apoptotikus sejt (kék) színezett pásztázó elektronmikroszkópos felvétele.NIAID Egy másik vizsgált koronavírusos betegség 2019 (COVID-19) vakcina 3. fázisú vizsgálata megkezdődött felnőtt önkéntesek felvételével. A randomizált, placebo-kontrollált vizsgálatba körülbelül 30 000 embert fognak bevonni az Egyesült Államok és Mexikó mintegy 115 helyszínén. A vizsgálatban a marylandi Gaithersburgben működő Novavax, Inc. által kifejlesztett NVX-CoV2373 vakcinajelölt biztonságosságát és hatékonyságát fogják értékelni. A Novavax vezeti a vizsgálatot, mint a hatósági szponzor. A kísérletet a National Institute of Allergy and Infectious Diseases (NIAID), a National Institutes of Health része, valamint a Biomedical Advanced Research and Development Authority (BARDA), az Egyesült Államok Egészségügyi és Emberi Szolgálatok Minisztériumának a felkészültségért és reagálásért felelős miniszterhelyettesi hivatalának része finanszírozza.
“A COVID-19 példátlan egészségügyi válságának kezelése rendkívüli erőfeszítéseket igényelt a kormányzat, a tudományos élet, az ipar és a közösség részéről” – mondta Anthony S. NIAID igazgatója. Dr. Anthony Fauci. “E vizsgálat elindítása – az ötödik olyan vizsgált COVID-19 vakcinajelölt, amelyet az Egyesült Államokban 3. fázisú vizsgálatban tesztelnek – bizonyítja elszántságunkat, hogy a világjárványnak több biztonságos és hatékony vakcina kifejlesztése révén véget vessünk.”
A vizsgálatot az Operation Warp Speed (OWS) együttműködésében végzik, amely a HHS és a Védelmi Minisztérium által felügyelt, több ügynökséget érintő együttműködés, amelynek célja a COVID-19 elleni orvosi ellenintézkedések fejlesztésének, gyártásának és terjesztésének felgyorsítása. A részt vevő egyesült államokbeli kísérleti helyszínek közül néhány a NIAID által támogatott COVID-19 megelőzési hálózat (CoVPN) része. A CoVPN a NIAID által támogatott, meglévő, fertőző betegségekkel foglalkozó klinikai kutatási hálózatokat foglalja magában, és a COVID-19 megelőzésére szolgáló vakcinajelöltek és monoklonális antitestek gyors és alapos értékelésére jött létre.
Az önkéntesektől a vizsgálatban való részvétel előtt tájékozott beleegyezést kérnek. Két csoportba sorolják őket: 18-64 évesek és 65 évesek vagy idősebbek, azzal a céllal, hogy az önkéntesek legalább 25%-a 65 éves vagy idősebb legyen. A vizsgálat szervezői hangsúlyt fektetnek azon személyek toborzására is, akiknél magasabb a súlyos COVID-19 betegség kockázata, beleértve a fekete bőrűeket (beleértve az afroamerikaiakat is), az amerikai őslakosokat, a latin vagy spanyolajkúakat, valamint azokat, akiknek olyan alapbetegségeik vannak, mint az elhízás, krónikus vesebetegség vagy cukorbetegség.
“Ilyen messzire jutottunk, ilyen gyorsan, de el kell jutnunk a célvonalig” – mondta Dr. Francis S. Collins, az NIH igazgatója, “Ehhez több vakcinára lesz szükség, különböző megközelítéseket alkalmazva, hogy mindenki biztonságosan és hatékonyan védve legyen ettől a halálos betegségtől.”
Az alapszintű orrgarat- és vérminta megadása után a résztvevők véletlenszerűen kapják meg a vizsgált vakcina intramuszkuláris injekcióját vagy egy sóoldatos placebót. A randomizálás 2:1 arányban történik úgy, hogy két önkéntes kapja a vizsgált vakcinát minden egyes placebót kapó önkéntes után. Mivel a vizsgálat vakon zajlik, sem a vizsgálók, sem a résztvevők nem fogják tudni, hogy ki kapja a jelölt vakcinát. A második injekciót 21 nappal az első után adják be.
A résztvevőket szorosan figyelemmel kísérik a vakcina esetleges mellékhatásai miatt, és arra kérik őket, hogy minden egyes injekciót követően és a következő két évben meghatározott időpontokban adjanak vérmintát. A tudósok elemezni fogják a vérmintákat, hogy kimutassák és számszerűsítsék a SARS-CoV-2-re, a COVID-19-et okozó vírusra adott immunválaszt. Megjegyzendő, hogy speciális vizsgálatokat fognak alkalmazni a természetes fertőzésből eredő immunitás és a vakcina által kiváltott immunitás megkülönböztetésére. A vizsgálat elsődleges végpontja annak meghatározása, hogy az NVX-CoV2373 képes-e megelőzni a tüneteket okozó COVID-19 megbetegedést hét vagy több nappal a második injekció beadása után a placebóhoz képest.
A Novavax vizsgálati vakcinája, az NVX-CoV2373 a koronavírus spike fehérjének stabilizált formájából készül a vállalat rekombináns fehérje nanorészecske technológiájának felhasználásával. A vakcinában lévő tisztított fehérjeantigének nem képesek szaporodni és nem képesek COVID-19-et okozni. A vakcina egy szabadalmaztatott adjuvánst, a MatrixM™-t is tartalmazza. Az adjuvánsok olyan adalékanyagok, amelyek fokozzák a vakcinára adott kívánt immunrendszeri válaszokat. Az NVX-CoV2373 folyékony formában kerül beadásra, és fagypont feletti hőmérsékleten (35° és 46°F között) tárolható, kezelhető és forgalmazható. Egyetlen vakcinaadag 5 mikrogramm (mcg) fehérjét és 50 mcg adjuvánst tartalmaz.
Az NVX-CoV2373 vakcinázás állatkísérletekben olyan antitesteket termelt, amelyek megakadályozták, hogy a koronavírus spike fehérje a vírus által megcélzott sejtfelszíni receptorokhoz kötődjön, megakadályozva a vírusfertőzést. A New England Journal of Medicine folyóiratban közzétett 1. fázisú klinikai vizsgálat eredményei szerint az NVX-CoV2373 általában jól tolerálható volt, és magasabb antitestszintet váltott ki, mint a klinikailag jelentős COVID-19-ből felépült emberektől vett vérmintákban. Az NVX-CoV2373-at egy dél-afrikai 2b fázisú vizsgálatban is értékelik, amelybe jelenleg 4.422 önkéntes bevonásával teljes mértékben bevonták, és az Egyesült Államokban és Ausztráliában végzett 1/2 fázisú folytatásos vizsgálat adatai már 2021 első negyedévében várhatóak. A Novavax nemrég fejezte be több mint 15 000 önkéntes bevonását a vakcinajelölt 3. fázisú vizsgálatába az Egyesült Királyságban, ahol szintén két injekciót tesztelnek, 5 mcg fehérjét és 50 mcg Matrix-M adjuvánst 21 nap különbséggel beadva.
A vizsgálat biztonságos és etikus lefolytatását egy független adat- és biztonsági ellenőrző bizottság (DSMB) felügyeli. Az OWS által támogatott valamennyi 3. fázisú vakcinajelölt klinikai vizsgálatot egy közös DSMB felügyeli, amelyet az NIH Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV) kezdeményezéssel konzultálva dolgoztak ki.
A vizsgálatban való részvétel iránt érdeklődő felnőttek a Coronaviruspreventionnetwork.org, a Novavax.com/PREVENT-19 vagy a ClinicalTrials.gov oldalon az NCT04611802 azonosítót keresve.
A COVID-19 Prevenciós Hálózatról: A COVID-19 Megelőzési Hálózatot (CoVPN) az Egyesült Államok Nemzeti Egészségügyi Intézeteinek Allergia és Fertőző Betegségek Nemzeti Intézete (NIAID) hozta létre a globális világjárványra való reagálás érdekében. A CoVPN-en keresztül az NIAID a meglévő kutatási hálózatainak és globális partnereinek fertőző betegségekkel kapcsolatos szakértelmét használja fel a SARS-CoV-2 elleni vakcinák és antitestek iránti sürgető igény kielégítésére. A CoVPN a COVID-19 megelőzésére szolgáló vakcinák és antitestek gyors és alapos értékelését biztosító tanulmányok kidolgozásán és lefolytatásán fog dolgozni. A CoVPN központja a Fred Hutchinson Rákkutató Központban található. A CoVPN-ről további információkért látogasson el a következő weboldalra: coronaviruspreventionnetwork.org.
A HHS-ről, az ASPR-ről és a BARDA-ról: A HHS minden amerikai egészségének és jólétének javításán és védelmén dolgozik, hatékony egészségügyi és humán szolgáltatásokat nyújtva, és elősegítve az orvostudomány, a közegészségügy és a szociális szolgáltatások fejlődését. Az ASPR küldetése az életek megmentése és az amerikaiak védelme a 21. századi egészségügyi biztonsági fenyegetésekkel szemben. Az ASPR-en belül a BARDA az innovációba, a fejlett kutatásba és fejlesztésbe, az orvosi ellenintézkedések – vakcinák, gyógyszerek, terápiák, diagnosztikai eszközök és az egészségügyi biztonsági fenyegetések elleni küzdelemhez szükséges nem gyógyszerészeti termékek – beszerzésébe és gyártásába fektet be. Eddig a BARDA által támogatott termékek 55 FDA jóváhagyást, engedélyt vagy engedélyt kaptak. Ha többet szeretne megtudni az országos COVID-19 válaszlépéshez nyújtott szövetségi támogatásról, látogasson el a www.coronavirus.gov.
Az Operation Warp Speedről: Az OWS az Egészségügyi és Emberi Szolgálatok Minisztériumának és a Védelmi Minisztériumnak a magánvállalatokkal és más szövetségi ügynökségekkel való együttműködés, valamint a HHS-szerte meglévő erőfeszítések összehangolása a COVID-19 vakcinák, terápiák és diagnosztikumok fejlesztésének, gyártásának és forgalmazásának felgyorsítása érdekében.
A National Institute of Allergy and Infectious Diseasesről: Az NIAID kutatásokat folytat és támogat – az NIH-ban, az Egyesült Államokban és világszerte – a fertőző és immunmediált betegségek okainak tanulmányozása, valamint e betegségek megelőzésére, diagnosztizálására és kezelésére szolgáló jobb eszközök kifejlesztése érdekében. Hírközlemények, adatlapok és egyéb, a NIAID-del kapcsolatos anyagok a NIAID weboldalán érhetők el.
A National Institutes of Health (NIH) szervezetről:Az NIH, a nemzet orvosi kutatási ügynöksége 27 intézetet és központot foglal magában, és az Egyesült Államok Egészségügyi és Humán Szolgáltatások Minisztériumának része. Az NIH az elsődleges szövetségi ügynökség, amely alap-, klinikai és transzlációs orvosi kutatásokat végez és támogat, és a gyakori és ritka betegségek okait, kezeléseit és gyógymódjait kutatja. Az NIH-ról és programjairól további információkért látogasson el a www.nih.gov weboldalra.
NIH…Turning Discovery Into Health®
###