A metilbenzol szulfonálása
A metilbenzol reaktívabb, mint a benzol, mivel a metilcsoport hajlamos az elektronokat a gyűrű felé “tolni”.
Ez a nagyobb reakcióképesség azt eredményezi, hogy a metilbenzol 0°C-on füstölgő kénsavval reagál, tömény kénsavval pedig akkor, ha kb. 5 percig reflux alatt melegítjük.
A reakció sebességére gyakorolt hatás mellett a metilbenzol esetében arra is gondolnunk kell, hogy a szulfonsavcsoport a metilcsoporthoz képest hol helyezkedik el a gyűrűn. A metilcsoportok hajlamosak új csoportokat “irányítani” a gyűrű 2- és 4-helyzetébe (feltételezve, hogy a metilcsoport az 1-helyzetben van). A metilcsoportokról azt mondják, hogy 2,4-irányítóak.
Így olyan elegyet kapunk, amely főként két izomerből áll. A 3-izomerből csak kb. 5-10% keletkezik. A főbb reakciók:
![]()
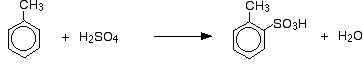
és:
![]()
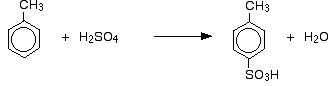
A szulfonálás esetében a keletkező izomerek pontos aránya a reakció hőmérsékletétől függ. A hőmérséklet növekedésével egyre nagyobb arányban keletkezik a 4-izomer és egyre kevesebb a 2-izomer. Ennek oka, hogy a szulfonálás reverzibilis. A szulfonsavcsoport újra leeshet a gyűrűről, és máshol kapcsolódhat újra. Ez a termodinamikailag legstabilabb izomer kialakulásának kedvez. Ez a felcserélődés magasabb hőmérsékleten jobban megtörténik.
A 4-izomer azért stabilabb, mert a molekulában nincs olyan rendezetlenség, mintha a metilcsoport és a szulfonsavcsoport egymás mellett lenne.