Atomok és az arany
1911-ben Rutherford és munkatársai, Hans Geiger és Ernest Marsden olyan úttörő kísérletsorozatot kezdeményeztek, amely teljesen megváltoztatta az atom elfogadott modelljét. Nagyon vékony aranyfólia lapokat bombáztak gyors mozgású alfa-részecskékkel.


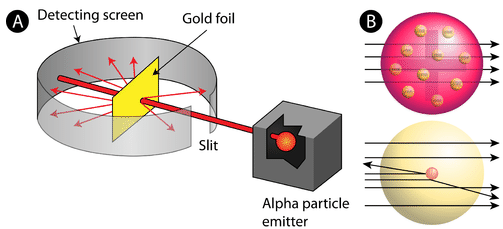
Ábra \(\PageIndex{2}\) (A) Rutherford aranyfóliás kísérletének kísérleti elrendezése: Egy radioaktív elemet, amely alfa-részecskéket bocsátott ki, egy vékony aranyfólia lap felé irányítottak, amelyet egy képernyő vett körül, amely lehetővé tette az eltérített részecskék kimutatását. (B) A szilvapuding modell szerint (fent) az összes alfa-részecskének át kellett volna haladnia az aranyfólián, kis eltérítéssel vagy anélkül. Rutherford azt találta, hogy az alfa-részecskék kis százaléka nagy szögben eltérült, ami egy olyan atommal magyarázható, amelynek középpontjában egy nagyon kicsi, sűrű, pozitív töltésű atommag van (alul).
Az elfogadott atommodell szerint, amelyben az atom tömege és töltése egyenletesen oszlik el az atomban, a tudósok arra számítottak, hogy az összes alfa-részecske csak kis eltérítéssel vagy egyáltalán nem halad át az aranyfólián. Meglepő módon, amint azt a \(\PageIndex{2}\) ábra mutatja (míg az alfa-részecskék többsége valóban eltérítetlen volt, egy nagyon kis százalékuk (körülbelül 1 részecske 8000-ből) nagyon nagy szögben visszapattant az aranyfóliáról. Néhányat még vissza is irányítottak a forrás felé. Erre a felfedezésre semmilyen előzetes tudás nem készítette fel őket. Egy híres idézetben Rutherford azt mondta, hogy ez olyan volt, “mintha egy 15 hüvelykes lövedéket lőttél volna ki egy szövetdarabra, és az visszajött volna, és eltalált volna téged.”
Rutherfordnak egy teljesen új atommodellt kellett kidolgoznia, hogy megmagyarázza az eredményeit. Mivel az alfa-részecskék túlnyomó többsége áthaladt az aranyon, arra következtetett, hogy az atom nagy része üres tér. Ezzel szemben a nagymértékben eltérített részecskéknek az atomon belül egy rendkívül nagy erejű erővel kellett találkozniuk. Arra a következtetésre jutott, hogy az atom összes pozitív töltése és tömegének nagy része az atom belsejében lévő nagyon kis térben koncentrálódik, amelyet ő magnak nevezett el. Az atommag az atom apró, sűrű, központi magja, amely protonokból és neutronokból áll.
Rutherford atommodellje atommodellként vált ismertté. Az atommagban a protonok és a neutronok, amelyek az atom majdnem teljes tömegét alkotják, az atommagban, az atom középpontjában helyezkednek el. Az elektronok az atommag körül helyezkednek el, és az atom térfogatának nagy részét elfoglalják. Érdemes hangsúlyozni, hogy az atommag milyen kicsi az atom többi részéhez képest. Ha fel tudnánk fújni egy atomot úgy, hogy az akkora legyen, mint egy nagy profi futballstadion, az atommag körülbelül akkora lenne, mint egy márványgolyó.
Rutherford modellje fontos lépésnek bizonyult az atom teljes megértése felé. Nem foglalkozott azonban teljes mértékben az elektronok természetével és azzal, hogy miként foglalják el az atommag körüli hatalmas teret. Ezért és más meglátásaiért Rutherford 1908-ban kémiai Nobel-díjat kapott. Sajnos Rutherford inkább a fizikai Nobel-díjat szerette volna megkapni, mert a fizikát a kémiánál magasabb rendűnek tartotta. Véleménye szerint “Minden tudomány vagy fizika, vagy bélyeggyűjtés.”